Clear Sky Science · it
Meccanismi molecolari della selettività del ligando nativo nei recettori accoppiati a proteine G per catecolamine
Come le cellule distinguono segnali simili
Il nostro cervello e il corpo si affidano a minuscoli messaggeri chimici — come dopamina e adrenalina — per trasmettere istruzioni tra le cellule. Queste molecole sono sorprendentemente simili, eppure ciascuna deve innescare la risposta corretta nel luogo giusto, che si tratti di migliorare l’attenzione, accelerare il battito cardiaco o elevare l’umore. Questo studio pone una domanda apparentemente semplice: come fanno molecole quasi identiche a "comporre" numeri cellulari diversi, e possiamo ricollegare deliberatamente questi numeri per la medicina e l’ingegneria biologica?
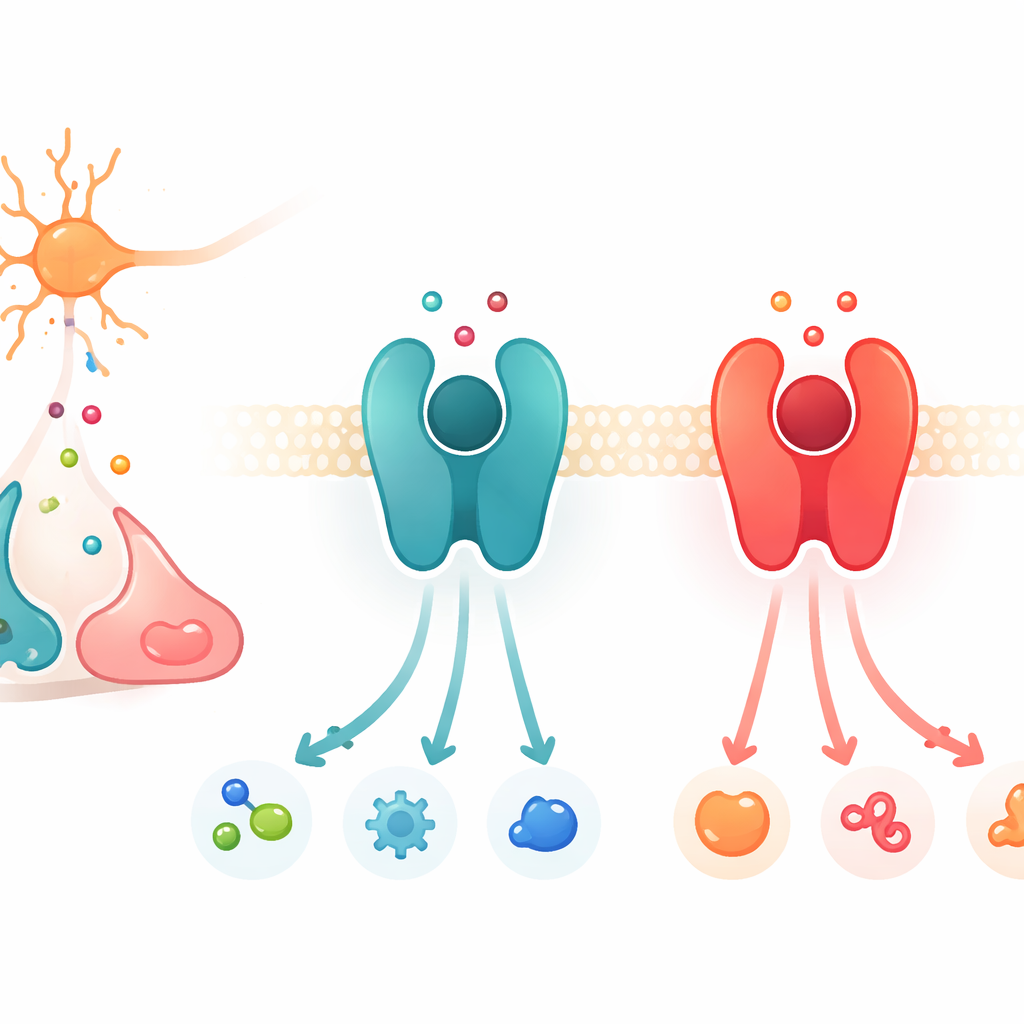
Centralini di segnale sulla superficie cellulare
Il lavoro si concentra su una grande famiglia di proteine chiamate recettori accoppiati a proteine G, o GPCR. Queste proteine si trovano nella membrana cellulare e funzionano come centralini: quando un messaggero chimico si lega all’esterno, il recettore cambia forma e attiva proteine partner all’interno, avviando una catena di segnali. Tra i molti GPCR, un sottoinsieme risponde alle catecolamine, i messaggeri strettamente correlati dopamina, adrenalina e noradrenalina. Due esempi chiave sono il recettore β2-adrenergico, che preferisce adrenalina e noradrenalina, e il recettore D1 della dopamina, che favorisce la dopamina. Sebbene questi recettori e le loro tasche di legame siano strutturalmente molto simili, ciascuno è estremamente selettivo rispetto al messaggero a cui risponde più fortemente.
Scambiare preferenze con pochi cambiamenti
I ricercatori hanno combinato confronti evolutivi, biologia strutturale e misure cellulari per individuare regioni “calde” che determinano questa preferenza chimica. Allineando centinaia di sequenze di recettori provenienti da molte specie e valutando dove le famiglie β2 e D1 differivano in modo costante, hanno ricavato una lista ristretta di posizioni aminoacidiche rilevanti. Alcuni di questi hotspot si trovano direttamente nella tasca di legame principale, dove si ancora il messaggero, mentre altri giacciono un po’ più in profondità nella proteina, lontano dal contatto diretto con la molecola. Il gruppo ha quindi mutato sistematicamente queste posizioni, testando oltre cento varianti di recettore per vedere quanto rispondevano a dopamina, adrenalina e noradrenalina usando letture cellulari dell’intensità del segnale.
Regolare le tasche e le manopole di controllo interne
Modificare solo i residui che toccano il messaggero cambiava la selettività, ma spesso a costo elevato: i recettori diventavano deboli o quasi non rispondenti, anche quando iniziavano a preferire un nuovo ligando. La vera svolta è arrivata combinando mutazioni nella tasca di legame con mutazioni in due regioni interne incastrate che agiscono come manopole di controllo interne. Nel recettore β2, aggiustamenti in un’interfaccia tri-elica aumentarono la sensibilità e lo inclinarono verso una modalità favorevole alla dopamina senza distruggerne la funzionalità. Nel recettore D1, modifiche in una diversa interfaccia interna riorganizzarono una rete di catene laterali che rimodellano indirettamente la tasca. Con le combinazioni giuste, i ricercatori invertirono completamente le preferenze: un β2 modificato ora preferiva la dopamina, mentre un D1 modificato favoriva adrenalina e noradrenalina — eppure entrambi continuavano a segnalare in modo robusto.
Uno sguardo sotto il cofano con strumenti ad alta risoluzione
Per vedere come questi cambiamenti operassero a livello atomistico, il team ha usato criomicroscopia elettronica per risolvere strutture 3D dei recettori ingegnerizzati legati ai loro nuovi messaggeri preferiti e ha eseguito ampie simulazioni di dinamica molecolare. Le strutture hanno mostrato che mutazioni chiave spostavano sottilmente parti della settima elica del recettore e un residuo "toggle" conservato, approfondendo o rendendo più superficiale la tasca e cambiando il modo in cui l’estremità amminica del messaggero si dispone. Gli hotspot distanti contribuirono a stabilizzare forme simili a quelle attive e rafforzarono le vie che trasmettono l’evento di legame all’interno della proteina. Le simulazioni confermarono che reti di residui interagenti collegano queste regioni esterne e interne, e che lo stesso piccolo insieme di posizioni può essere riutilizzato attraverso sottotipi correlati per invertire la selettività senza rendere i recettori ampiamente promiscui.
Cosa significa per la medicina e l’evoluzione
In termini semplici, lo studio mostra che una manciata di “atomi” ben scelti in questi recettori funziona come viti di regolazione che decidono se una proteina ascolta principalmente la dopamina o l’adrenalina. Queste viti non sono tutte in superficie dove si ancora il messaggero; alcune sono sepolte più in profondità e stabilizzano come l’intera struttura si flette quando arriva un segnale. Poiché la stessa logica progettuale ricorre nelle famiglie di recettori, l’evoluzione può ripetutamente riutilizzare impalcature proteiche simili per nuovi messaggeri prima aumentando la reattività tramite aggiustamenti interni e poi rifinendo la tasca. Per la scoperta di farmaci, questi insight indicano punti precisi — sia dentro che attorno al sito di legame — che i chimici possono mirare per sviluppare medicinali che colpiscano un sottotipo di recettore risparmiandone altri, e per progettare recettori su misura che rispondano solo a segnali ideati in terapie e biosensori.
Citazione: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
Parole chiave: Recettori accoppiati a proteine G, dopamina, adrenalina, selettività dei ligandi, progettazione di farmaci