Clear Sky Science · he
מנגנונים מולקולריים של סלקטיביות ליגנד יליד בקולטנים מצומדי חלבון G של קטכולאמינים
כיצד תאים מבחינים בין אותות דומים
המוח והגוף שלנו מסתמכים על משלחים כימיים זעירים — כגון דופמין ואדרנלין — כדי להעביר הוראות בין תאים. המולקולות האלה דומות באופן מפתיע, ובכל זאת כל אחת מהן חייבת להפעיל את התגובה הנכונה במקום הנכון, בין אם זה חידוד קשב, האצת קצב הלב או שיפור מצב הרוח. המחקר מתמודד עם שאלה שנראית פשוטה אך מטעה: כיצד מולקולות כמעט זהות מצליחות "לחייג" למספרי טלפון תאיים שונים, והאם אפשר לכוונן באופן מכוון את המספרים הללו לטובת רפואה ומהנדס ביולוגי?
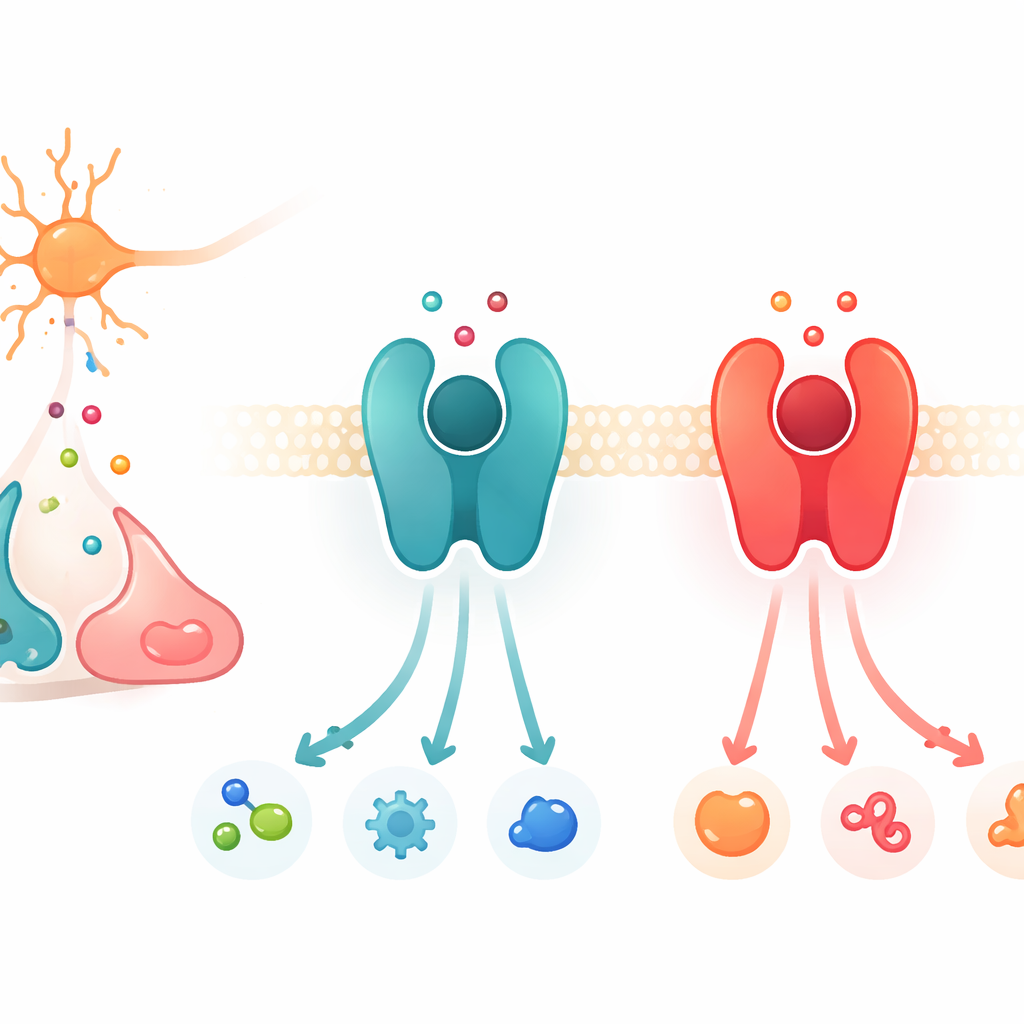
לוחות החלפה של אותות על פני התא
העבודה מתמקדת במשפחת חלבונים גדולה שנקראת קולטנים מצומדי חלבון G, או GPCR. חלבונים אלה שוכנים בממברנת התא ופועלים כמו לוחות החלפה: כאשר משלח כימי נקשר מבחוץ, הקולטן משנה צורה ומפעיל חלבונים שותפים מבפנים, מה שמצית שרשרת אותות. בין ה-GPCR הרבבּה, תת־קבוצה מגיבה לקטכולאמינים — המשלחים הקרובים דמיון דוגמת דופמין, אדרנלין ונוראדרנלין. שתי דוגמאות מרכזיות הן קולטן β2-אדרנרגי, המעדיף אדרנלין ונוראדרנלין, וקולטן D1 לדופמין, המעדיף דופמין. למרות שהקולטנים ותעלות הקשירה שלהם דומים באופן בולט במבנה, כל אחד מהם סלקטיבי במידה רבה לגבי המשלח שאליו הוא מגיב בחוזקה.
החלפת העדפות באמצעות כמה שינויים בודדים
החוקרים שילבו השוואות אבולוציוניות, ביולוגיה מבנית ומדידות בתאי־חי כדי לאתר אזורי "נקודות חמות" שקובעים את ההעדפה הכימית. באמצעות יישור של מאות רצפי קולטנים ממינים רבים ודירוג המקומות שבהם משפחות β2 ו-D1 שונות בעקביות, הם גיבשו רשימה קצרה של עמדות חומצות אמינו שבלטו. חלק מנקודות החימום נמצאו ישירות בכיס הקשירה הראשי, שם המשלח עוגן, בעוד אחרות ישבו מעט עמוק יותר בחלבון, הרחק ממגע ישיר עם המולקולה. הצוות אז ערך מוטציות שיטתיות בעמדות אלה, ובדק יותר ממאה וריאנטים של קולטנים לאופן שבו הם הגיבו לדופמין, אדרנלין ונוראדרנלין בעזרת מדדי איתות תאיים.
כיול כיסים וכפתורי בקרה פנימיים
שינוי רק של שיירים שנוגעים במשלח אכן שינה את הסלקטיביות, אך לעתים קרובות במחיר כבד: הקולטנים נעשו חלשים או כמעט בלתי־מגיבים, אפילו כאשר החלו להעדיף ליגנד חדש. הפריצת דרך האמיתית הגיעה כאשר מוטציות בכיס הקשירה שולבו עם מוטציות בשני אזורים פנימיים משולבי־תאר שפועלים ככפתורי בקרה פנימיים. בקולטן β2, התאמות בממשק של שלוש אלפות החזיקו בהגברת הרגישות והטייתו למצב ידידותי לדופמין מבלי להרוס את התפקוד. בקולטן D1, שינויים בממשק פנימי נפרד ארגנו מחדש רשת של שרשרות צד שמעצבת בעקיפין את הכיס. עם השילובים הנכונים, החוקרים החליפו לחלוטין את ההעדפות: קולטן β2 מותאם החל להעדיף דופמין, בעוד קולטן D1 מותאם העדיף אדרנלין ונוראדרנלין — וזאת כששניהם עדיין איתרו איתות בעוצמה.
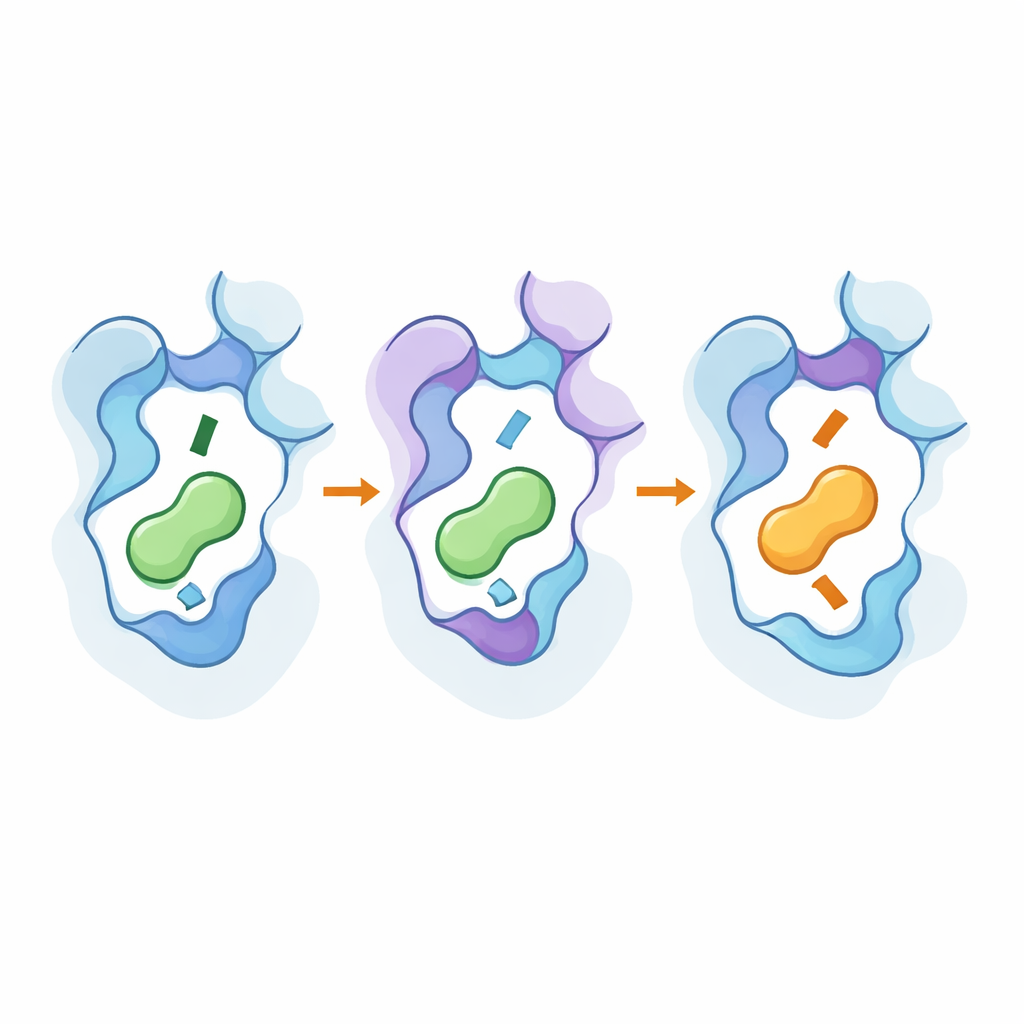
הסתכלות מתחת למכסה בעזרת כלים ברזולוציה גבוהה
כדי לראות כיצד השינויים פעלו ברמת האטום, הצוות השתמש במיקרוסקופ אלקטרונים קפוא (cryo-EM) כדי לפתור מבנים תלת־ממדיים של הקולטנים המהונדסים כשהם קשורים למשלחים המועדפים החדשים, והריץ סימולציות דינמיקת מולקולות נרחבות. המבנים הראו שמוטציות מפתח הזיזו בעדינות חלקים מההליקס השביעי של הקולטן ושייר "מתג" שמור, העמיקו או השטיחו את הכיס ושינו את מיקום קצה האמין של המשלח. נקודות החימום הרחוקות סייעו לייצב צורות דמויות־פעילות והחזיקו נתיבים שמעבירים את אירוע הקשירה למבנה הפנימי של החלבון. הסימולציות אישרו שרשתות של שיירים אינטראקטיביים מקשרות בין האזורים החיצוניים והפנימיים, ושאותן קבוצת עמדות קטנה ניתנת לשימוש חוזר בתתי־סוגים קשורים של קולטנים כדי להפוך את הסלקטיביות מבלי להפוך את הקולטנים לפוריטיים ברמה רחבה.
מה משמעות הדבר לרפואה ולאבולוציה
במונחים פשוטים, המחקר מראה שקבוצה קטנה של "אטומים" נבחרים בקולטנים אלה פועלים כבורגים מכוונים שמחליטים האם חלבון מאזין בעיקר לדופמין או לאדרנלין. הבורגים האלה לא כולם על המשטח שבו המשלח נקשר; חלקם קבורים עמוק יותר ומייצבים את אופן הגמישות של כל המבנה כשהאות מגיע. מאחר שהלוגיקה העיצובית חוזרת על עצמה במשפחות קולטנים, האבולוציה יכולה שוב ושוב לייעד מחדש שלדונים חלבוניים דומים למשלחים חדשים על ידי שיפור הרגישות באמצעות התאמות פנימיות, ולאחר מכן כיוונון מדויק של הכיס. עבור גילוי תרופות, התובנות האלו מצביעות על נקודות מדויקות — הן בתוך אתר הקשירה והן מסביבתו — שהכימאים יכולים ליעד כדי לעצב תרופות שפוגעות בתת־סוג אחד של קולטן בעוד הן משאירות אחרים, וכדי להנדס קולטנים מותאמים שמגיבים רק לאותות מתוכננים בטיפולים וחיישנים ביולוגיים.
ציטוט: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
מילות מפתח: קולטני חלבון G, דופמין, אדרנלין, סלקטיביות ליגנד, עיצוב תרופתי