Clear Sky Science · sv
Molekylära mekanismer bakom selektivitet för naturliga ligander i katekolamin-G-proteinkopplade receptorer
Hur celler skiljer åt snarlika signaler
Vår hjärna och kropp förlitar sig på små kemiska budbärare—som dopamin och adrenalin—för att överföra instruktioner mellan celler. Dessa molekyler ser förvånansvärt lika ut, ändå måste var och en framkalla rätt respons på rätt plats, oavsett om det handlar om att skärpa uppmärksamheten, öka hjärtfrekvensen eller höja sinnesstämningen. Denna studie ställer en bedrägligt enkel fråga: hur kan nästan identiska molekyler få olika cellulära ”telefonnummer” att ringa, och kan vi medvetet skriva om dessa nummer för medicin och bioengineering?
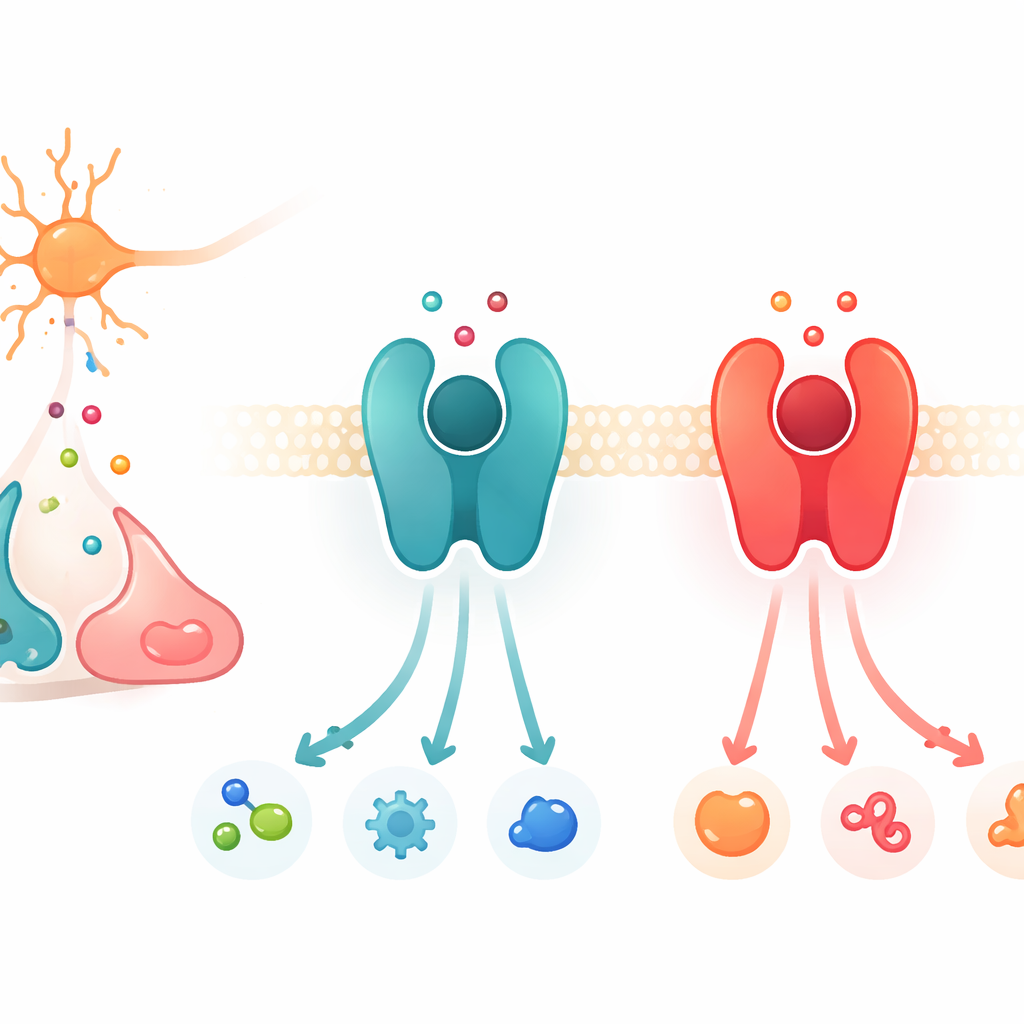
Signalväxlar på cellens yta
Arbetet fokuserar på en stor proteinfamilj kallad G-proteinkopplade receptorer, eller GPCR:er. Dessa proteiner sitter i cellmembranet och fungerar som växlar: när en kemisk budbärare binder på utsidan ändrar receptorn form och aktiverar partnerproteiner på insidan, vilket startar en signalkedja. Bland de många GPCR:erna svarar en undergrupp på katekolaminerna — de närbesläktade budbärarna dopamin, adrenalin och noradrenalin. Två viktiga exempel är β2-adrenerg receptor, som föredrar adrenalin och noradrenalin, och D1-dopaminreceptorn, som favoriserar dopamin. Trots att dessa receptorer och deras bindningsfickor är slående lika i struktur är var och en mycket kräsen när det gäller vilken budbärare den reagerar mest på.
Byta preferenser med bara några få förändringar
Forskarna kombinerade evolutionära jämförelser, strukturbiologi och cellbaserade mätningar för att spåra ”hotspot”-regioner som bestämmer denna kemiska preferens. Genom att justera hundratals receptorsekvenser från många arter och poängsätta var β2- och D1-familjerna konsekvent skiljer sig hittade de en kort lista aminosyrapositioner som stack ut. Några av dessa hotspots ligger direkt i huvudbindningsfickan, där budbäraren förankras, medan andra sitter något djupare i proteinet, bort från direkt kontakt med kemikalien. Teamet muterade sedan systematiskt dessa positioner och testade mer än hundra receptorvarianter för hur väl de svarade på dopamin, adrenalin och noradrenalin med hjälp av cellulära avläsningar av signalstyrka.
Ställa in fickor och djupa kontrollvred
Att ändra enbart de rester som rörde budbäraren förändrade visserligen selektiviteten, men ofta till ett högt pris: receptorerna blev svaga eller nästan oresponsiva, även när de började föredra en ny ligand. Det verkliga genombrottet kom när mutationer i bindningsfickan kombinerades med mutationer i två djupare sammanlänkade regioner som fungerar som interna kontrollvred. I β2-receptorn ökade justeringar i ett tri-helix-gränssnitt dess känslighet och lutade den mot ett dopaminvänligt läge utan att förstöra funktionen. I D1-receptorn omorganiserade förändringar i ett separat internt gränssnitt ett nätverk av sidokedjor som indirekt omformar fickan. Med rätt kombinationer bytte forskarna fullt ut preferenser: en modifierad β2-receptor föredrog nu dopamin, medan en modifierad D1-receptor gynnade adrenalin och noradrenalin—men båda signalerade fortfarande robust.
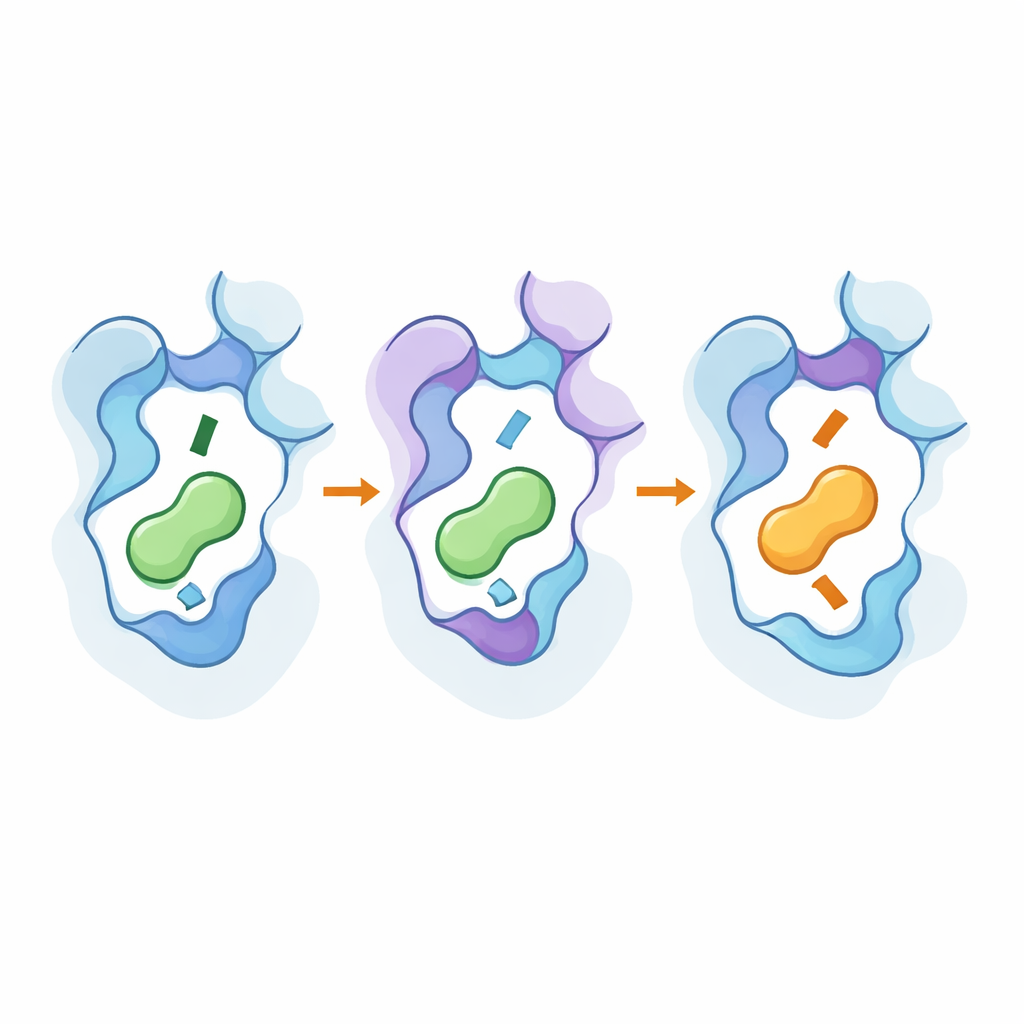
Titta under huven med högupplösta verktyg
För att se hur dessa förändringar fungerade på atomär nivå använde teamet kryoelektronmikroskopi för att lösa tredimensionella strukturer av de konstruerade receptorerna bundna till sina nya föredragna budbärare, och körde omfattande molekylär dynamik-simuleringar. Strukturerna visade att nyckelmutationer subtilt försköt delar av receptorernas sjunde helix och en konservativ ”toggle”-rest, vilket fördjupade eller grundade fickan och ändrade hur budbärarens amingrupp positioneras. De avlägsna hotspots hjälpte till att stabilisera aktiva-liknande former och stärkte vägar som förmedlar bindningshändelsen till proteinets insida. Simuleringar bekräftade att nätverk av interagerande rester länkar dessa yttre och inre regioner, och att samma lilla uppsättning positioner kan återanvändas över besläktade receptorsubtyper för att växla selektivitet utan att göra receptorerna brett promiskuösa.
Vad detta betyder för medicin och evolution
Enkelt uttryckt visar studien att en handfull väl valda ”atomer” i dessa receptorer fungerar som inställningsskruvar som bestämmer om ett protein främst lyssnar på dopamin eller på adrenalin. Dessa skruvar sitter inte bara vid ytan där budbäraren förankras; några är begravda djupare och stabiliserar hur hela strukturen böjer sig när en signal anländer. Eftersom samma designlogik återkommer i olika receptorfamiljer kan evolutionen upprepade gånger återanvända liknande proteinstommar för nya budbärare genom att först öka responsiviteten via interna justeringar och sedan finslipa fickan. För läkemedelsupptäckt pekar dessa insikter på precisa platser—både i och runt bindningsstället—som kemister kan rikta in sig på för att skapa läkemedel som träffar en receptorsubtyp samtidigt som andra spares, och för att konstruera skräddarsydda receptorer som bara reagerar på designade signaler i terapier och biosensorer.
Citering: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
Nyckelord: G-proteinkopplade receptorer, dopamin, adrenalin, ligandselektivitet, läkemedelsdesign