Clear Sky Science · ja
カテコラミンGタンパク質共役受容体における天然リガンド選択性の分子機構
細胞は似た信号をどう区別するか
私たちの脳や身体は、ドーパミンやアドレナリンのような小さな化学伝達物質に頼って細胞間の指示を伝えています。これらの分子は驚くほどよく似ていますが、注意力の鋭敏化、心拍の速化、気分の高揚など、適切な場所で適切な応答を引き起こさなければなりません。本研究は一見単純な問いを投げかけます:ほとんど同一の分子がどのようにして異なる細胞の電話番号を「ダイヤル」し、それらの番号を医学やバイオ工学のために意図的に書き換えられるかどうかは?
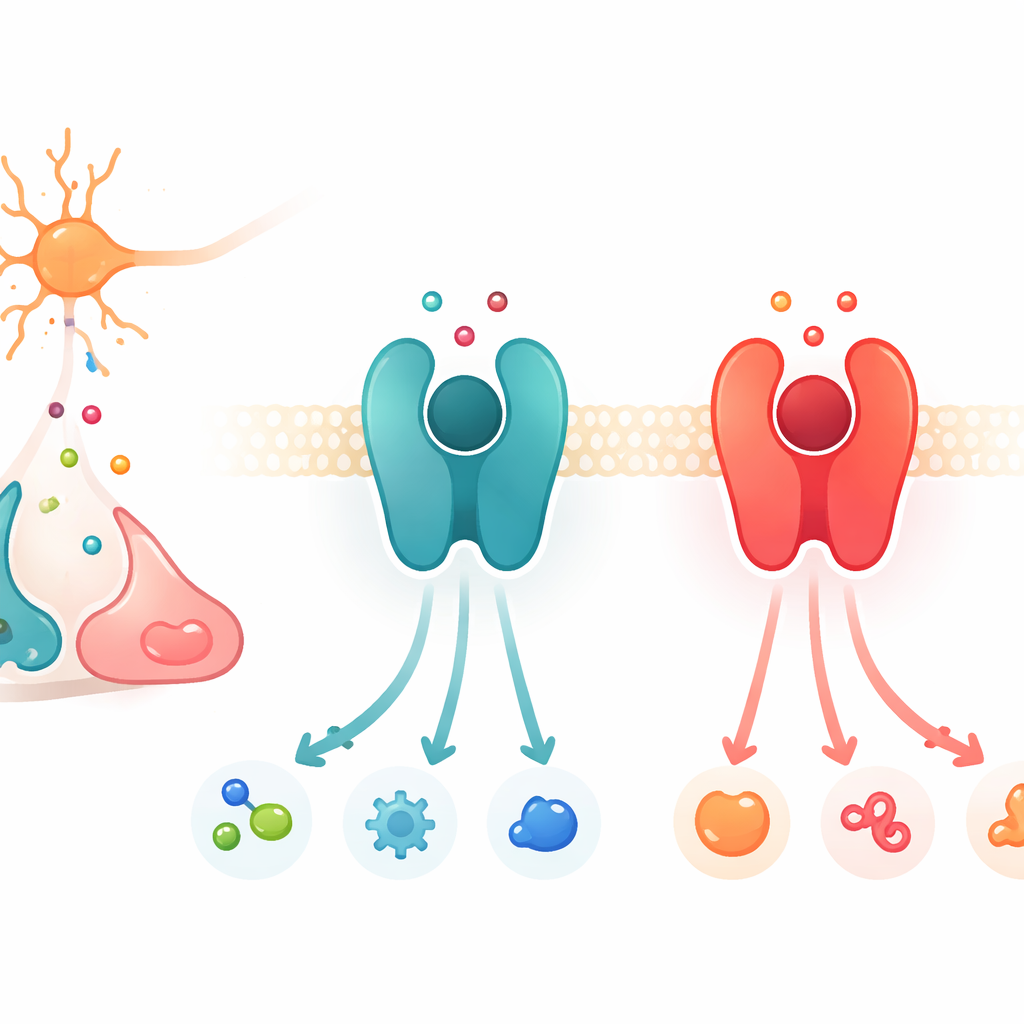
細胞表面の信号交換機
本研究はGタンパク質共役受容体(GPCR)と呼ばれる大きなタンパク質ファミリーに焦点を当てています。これらのタンパク質は細胞膜に位置し、外側で化学伝達物質が結合すると形を変えて内側のパートナータンパク質を活性化し、一連の信号を開始するスイッチボードのように働きます。多くのGPCRの中で、カテコラミン(ドーパミン、アドレナリン、ノルアドレナリン)に応答するサブセットがあります。代表例として、アドレナリンとノルアドレナリンを好むβ2アドレナリン受容体と、ドーパミンを好むD1ドーパミン受容体が挙げられます。これらの受容体とその結合ポケットは構造的に非常に類似していますが、それぞれは最も強く反応する伝達物質に対して非常に選択的です。
わずかな変化で好みを入れ替える
研究者たちは進化的比較、構造生物学、細胞ベースの計測を組み合わせて、この化学的嗜好を決める「ホットスポット」領域を特定しました。多くの種から集めた何百もの受容体配列を整列し、β2族とD1族が一貫して違う位置をスコアリングすることで、注目すべきアミノ酸残基の短いリストを見つけました。これらのホットスポットの一部は伝達物質が結合する主要なポケットの直接的な位置にあり、他は化学物質と直接接触しないやや深い内部に位置していました。次にチームはこれらの位置を系統的に変異させ、細胞内のシグナル強度の指標を用いて100以上の受容体バリアントがドーパミン、アドレナリン、ノルアドレナリンにどの程度応答するかをテストしました。
ポケットと深部の調整ノブ
伝達物質に接する残基だけを変えると選択性は変わりましたが、多くの場合大きな代償が伴いました:受容体は弱くなったりほとんど応答しなくなったりし、それでも新しいリガンドを好むようになることがありました。本当の突破口は、結合ポケットの変異を内部の二つの相互に絡む領域の変異と組み合わせたときに訪れました。これらの内部領域は内部の調整ノブのように働きます。β2受容体では、三本のヘリックスが交わるインターフェースの調整が感受性を高め、機能を損なうことなくドーパミンに親和的なモードへと傾けました。D1受容体では別の内部インターフェースの編集が側鎖のネットワークを再編し、間接的にポケットの形を変えました。適切な組み合わせで研究者たちは嗜好を完全に入れ替えました:改変されたβ2はドーパミンを好み、改変されたD1はアドレナリンとノルアドレナリンを好むようになり、それでも両者とも強力にシグナルを伝えました。
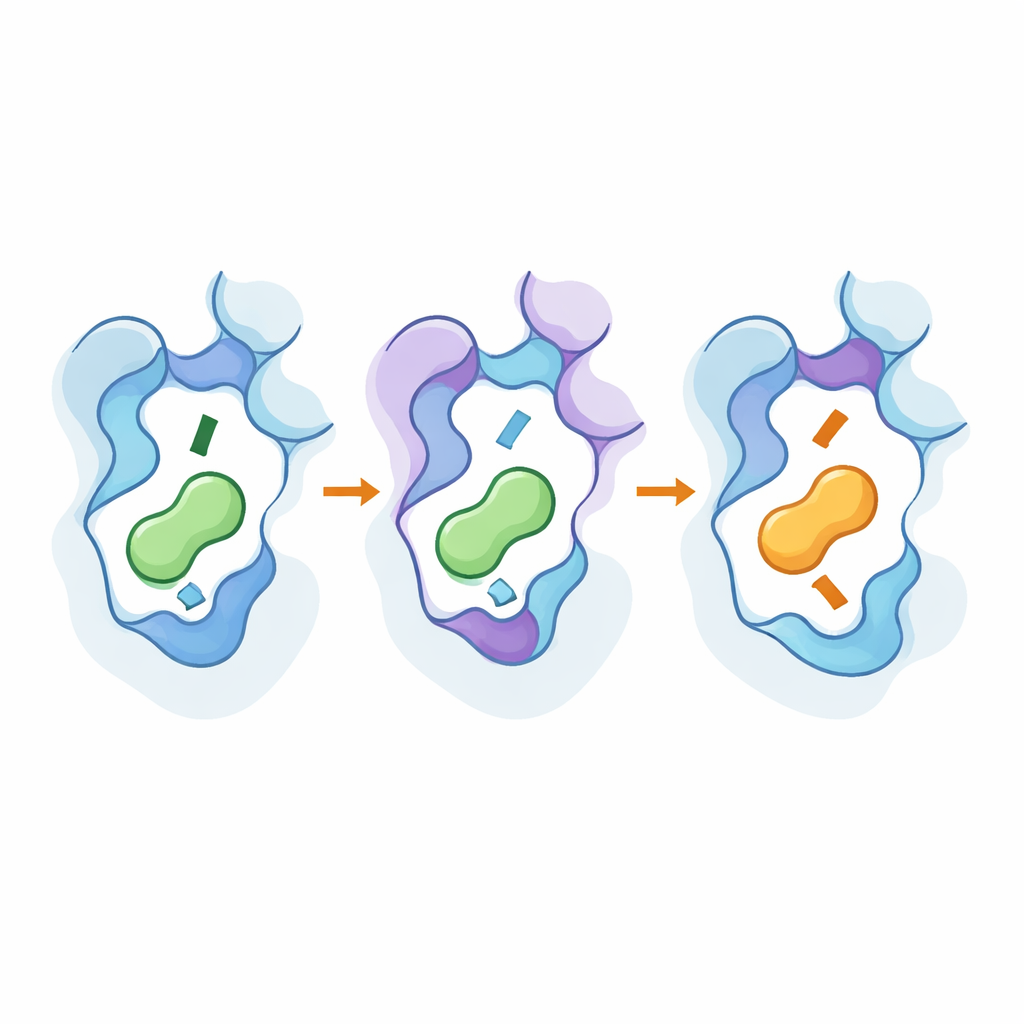
高解像度ツールで内部をのぞく
これらの変化が原子レベルでどのように働くかを明らかにするため、チームはクライオ電子顕微鏡を用いて設計した受容体が新たに好む伝達物質と結合した3次元構造を解き、広範な分子動力学シミュレーションを行いました。構造は、重要な変異が受容体の第七ヘリックスの一部と保存された「トグル」残基の位置を微妙にシフトさせ、ポケットを深くしたり浅くしたりして伝達物質のアミン末端の収まり方を変えることを示しました。遠位のホットスポットはアクティブ様の形状を安定化し、結合イベントをタンパク質内部へ伝える経路を強化しました。シミュレーションは、これらの外側と内側の領域を結ぶ残基間相互作用のネットワークが存在すること、そして同じ少数の位置が関連する受容体サブタイプ間で再利用され、受容体を広く多掛けにすることなく選択性を反転させ得ることを確認しました。
医学と進化にとっての意味
平たく言えば、この研究は受容体中のごく少数の「原子」が調整ネジのように働き、タンパク質が主にドーパミンに耳を傾けるかアドレナリンに耳を傾けるかを決めることを示しています。これらのネジはすべて伝達物質が結合する表面にあるわけではなく、中に埋まって全体の構造が信号到来時にどう曲がるかを安定化します。同じ設計論理が受容体ファミリー全体で繰り返されるため、進化は内部の調整によってまず応答性を高め、その後ポケットを微調整することで類似したタンパク質骨格を何度も新しい伝達物質へと転用できます。創薬にとっては、これらの知見は結合部位の内外にある正確なスポットを示しており、化学者が特定の受容体サブタイプだけを狙う薬を設計したり、治療やバイオセンサー用に設計された信号にのみ反応するカスタム受容体を構築したりする際の指針となります。
引用: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
キーワード: Gタンパク質共役受容体, ドーパミン, アドレナリン, リガンド選択性, 創薬