Clear Sky Science · ar
الآليات الجزيئية لاختيار الرباطات الأصلية في مستقبلات البروتين G المرتبطة بالكاثيكولامين
كيف تميز الخلايا إشارات متشابهة
يعتمد دماغنا وجسمنا على رسولين كيميائيين دقيقين—مثل الدوبامين والأدرينالين—لحمل التعليمات بين الخلايا. تبدو هذه الجزيئات متشابهة بشكل لافت، ومع ذلك يجب على كلٍ منها إطلاق الاستجابة الصحيحة في المكان المناسب، سواءً كان ذلك في حدة الانتباه أو تسريع القلب أو رفع المزاج. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكنه خادع: كيف تدير جزيئات شبه متطابقة عملياً «الاتصال» بأرقام خلوية مختلفة، وهل يمكننا إعادة توصيل تلك الأرقام عمداً لأغراض طبية وهندسية حيوية؟
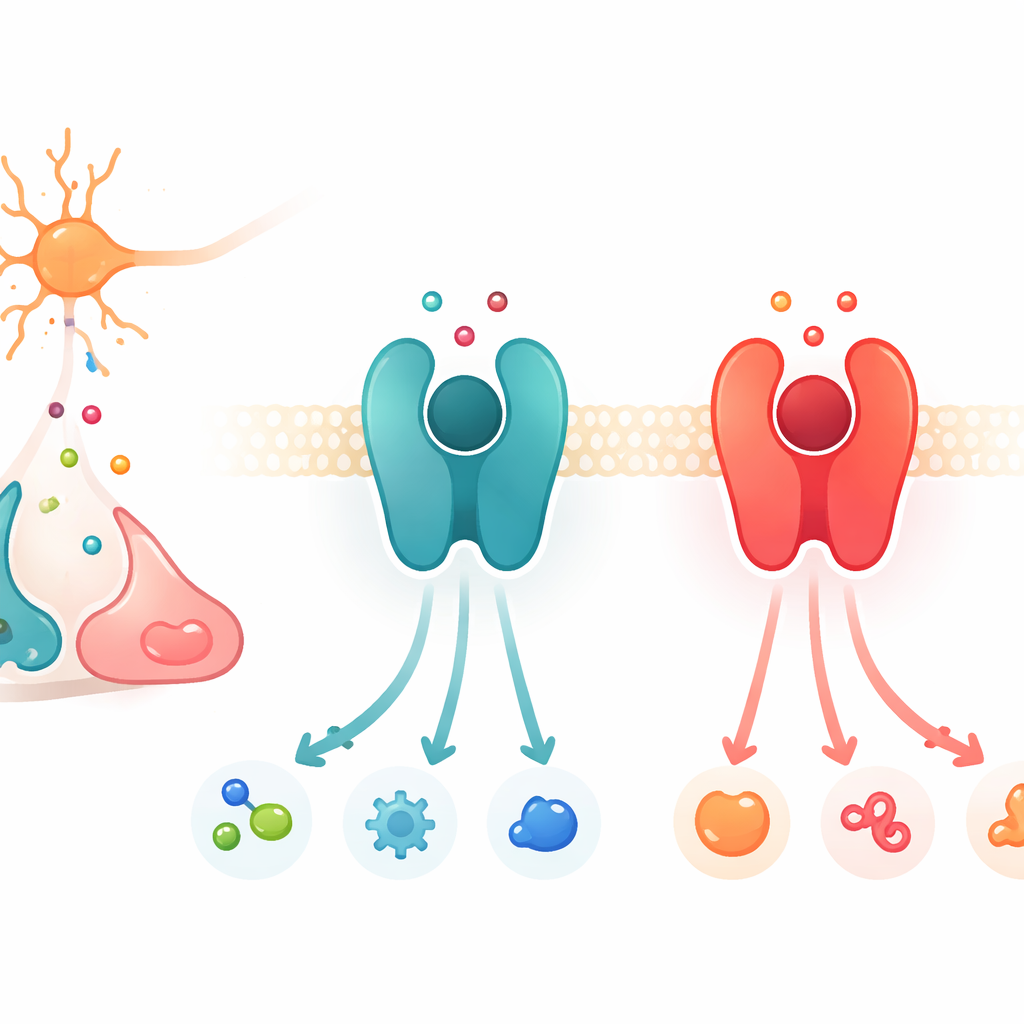
مفاتيح تبديل الإشارات على أسطح الخلايا
تركز الدراسة على عائلة بروتينية كبيرة تسمى مستقبلات البروتين G المرتبطة، أو GPCRs. تجلس هذه البروتينات في غشاء الخلية وتعمل كمفاتيح تبديل: عندما يرتبط رسول كيميائي من الخارج، يغير المستقبل شكله وينشط بروتينات شريكة من الداخل، مطلقاً سلسلة من الإشارات. من بين العديد من مستقبلات GPCR، يستجيب جزء لها للكاثيكولامينات، المرسالين المتقاربين الدوبامين والأدرينالين والنورأدرينالين. من الأمثلة الرئيسية مستقبل β2-الأدرينيرجي، الذي يفضل الأدرينالين والنورأدرينالين، ومستقبل D1 للدوبامين، الذي يميل إلى الدوبامين. بالرغم من أن هذه المستقبلات وجيوب الارتباط فيها متشابهة بشكل لافت في البنية، فإن كل واحد منها صارم جداً في اختيار المرسل الذي يستجيب له بقوة أكبر.
تبديل التفضيلات بعدد قليل من التغييرات
جمع الباحثون بين المقارنات التطورية والبيولوجيا البُنائية والقياسات الخلوية لتتبع مناطق «نقاط ساخنة» تحدد هذا التفضيل الكيميائي. عبر محاذاة مئات تسلسلات المستقبلات من أنواع عديدة وتسجيل مواقع الاختلاف المستمرة بين عائلتي β2 وD1، وجدوا قائمة قصيرة من مواقع الأحماض الأمينية البارزة. تقع بعض هذه النقاط الساخنة مباشرة في جيب الارتباط الرئيسي حيث يرسو الرسول، بينما تقع أخرى أعمق قليلاً داخل البروتين بعيداً عن الاتصال المباشر بالمادة الكيميائية. ثم طوَّف الفريق هذه المواقع منهجياً، مختبراً أكثر من مائة متغيِّر للمستقبل لرصد مدى استجابتهم للدوبامين والأدرينالين والنورأدرينالين باستخدام قراءات خلوية لقوة الإشارة.
ضبط الجيوب ومقابض التحكم العميقة
تغيير البقايا التي تلامس الرسول وحدها غيّر الانتقائية، لكنه غالباً ما جاء بتكلفة كبيرة: أصبحت المستقبلات ضعيفة أو شبه غير مستجيبة، حتى عندما بدأت تُظهر تفضيلاً لرباط جديد. جاء الاختراق الحقيقي عندما رُكّبت طفرات في جيب الارتباط مع طفرات في منطقتين داخليتين متشابكتين تعملان كمقابض تحكم داخلية. في مستقبل β2، عززت تعديلات في واجهة ثلاثية الحلزونين حساسيته ودفعته نحو وضع صديق للدوبامين دون تدمير الوظيفة. في مستقبل D1، أعادت تعديلات في واجهة داخلية منفصلة تنظيم شبكة من سلاسل الجانبية التي تعيد تشكيل الجيب بشكل غير مباشر. مع التوليفات الصحيحة، استبدل الباحثون التفضيلات بالكامل: أصبح مستقبل β2 المعدَّل يفضل الدوبامين، بينما آثر مستقبل D1 المعدَّل الأدرينالين والنورأدرينالين—ومع ذلك استمر كلاهما في الإشارة بقوة.
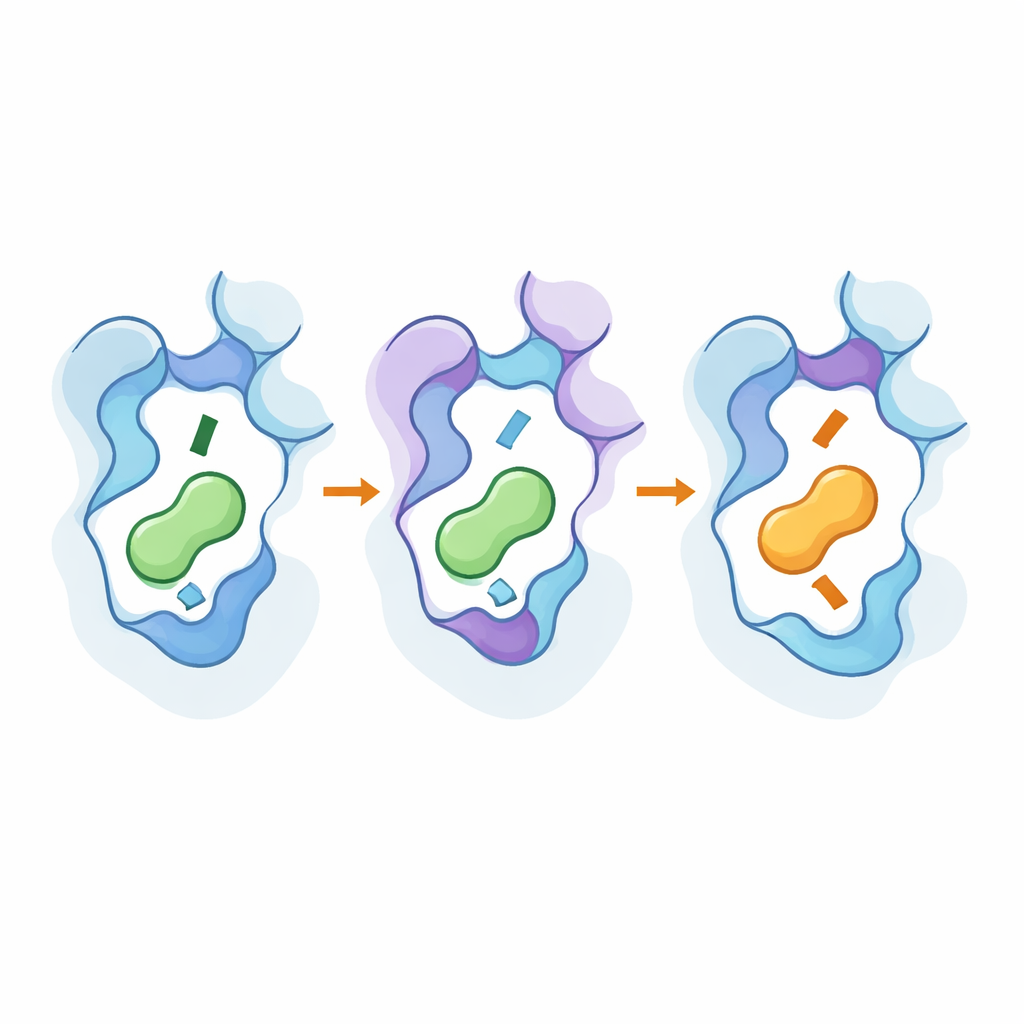
إلقاء نظرة تحت الغطاء بأدوات عالية الدقة
لرؤية كيفية عمل هذه التغييرات على المستوى الذري، استخدم الفريق مجهرًا إلكترونياً بالتبريد لحل الهياكل ثلاثية الأبعاد للمستقبلات المهندَسة المرتبطة بالمرسلات المفضلة الجديدة، وأجرى محاكيات ديناميكية جزيئية موسعة. أظهرت الهياكل أن الطفرات الرئيسية حرَّكت أجزاء من الحلزون السابع وبقايا «مفتاح التبديل» المحفوظة بشكل دقيق، مما عمّق أو جعل الجيب أضيق وغير ذلك وغير موضعية كيفية جلوس الطرف الأميني للمرسل. ساعدت النقاط الساخنة البعيدة على تثبيت أشكال شبيهة بالنشطة وتقوية مسارات تنقل حدث الارتباط إلى داخل البروتين. وأكدت المحاكيات أن شبكات البقايا المتفاعلة تربط هذه المناطق الخارجية والداخلية، وأن نفس المجموعة الصغيرة من المواقع يمكن إعادة استخدامها عبر أنواع مستقبلية قريبة لقلب الانتقائية دون أن تجعل المستقبلات مسرفة في الارتباط.
ماذا يعني هذا للطب وللتطور
بعبارات بسيطة، تُظهر الدراسة أن حفنة من «الذرات» المنتقاة بعناية في هذه المستقبلات تعمل كمسامير ضبط تقرر ما إذا كان البروتين يستمع أساساً إلى الدوبامين أو إلى الأدرينالين. هذه المسامير ليست جميعها على السطح حيث يرسو الرسول؛ فبعضها مدفون أعمق، يثبت كيفية انثناء البنية بأكملها عند وصول الإشارة. وبما أن نفس منطق التصميم يتكرر عبر عائلات المستقبلات، يمكن للتطور أن يعيد استخدام هياكل بروتينية متشابهة مراراً لرسائل جديدة عن طريق زيادة الاستجابة عبر تعديلات داخلية أولاً، ثم ضبط الجيب لاحقاً. بالنسبة لاكتشاف الأدوية، تشير هذه الرؤى إلى نقاط دقيقة—داخل موقع الارتباط وحوله—يمكن للكيميائيين استهدافها لصنع أدوية تضرب نوع مستقبل فرعي واحد مع ترك الأخرى سليمة، ولتصميم مستقبلات مخصصة تستجيب فقط لإشارات مصممة في العلاجات وأجهزة الاستشعار الحيوية.
الاستشهاد: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
الكلمات المفتاحية: مستقبلات البروتين G المرتبطة, دوبامين, أدرينالين, انتقائية الرباط, تصميم الأدوية