Clear Sky Science · fr
Mécanismes moléculaires de la sélectivité des ligands natifs dans les récepteurs couplés aux protéines G des catécholamines
Comment les cellules distinguent des signaux similaires
Notre cerveau et notre corps dépendent de petits messagers chimiques — comme la dopamine et l’adrénaline — pour transmettre des instructions entre les cellules. Ces molécules se ressemblent étonnamment, et pourtant chacune doit déclencher la bonne réponse au bon endroit, qu’il s’agisse d’affiner l’attention, d’accélérer le cœur ou d’améliorer l’humeur. Cette étude pose une question apparemment simple : comment des molécules presque identiques parviennent-elles à « composer » des numéros cellulaires différents, et peut-on délibérément réorienter ces numéros pour la médecine et le génie biologique ?
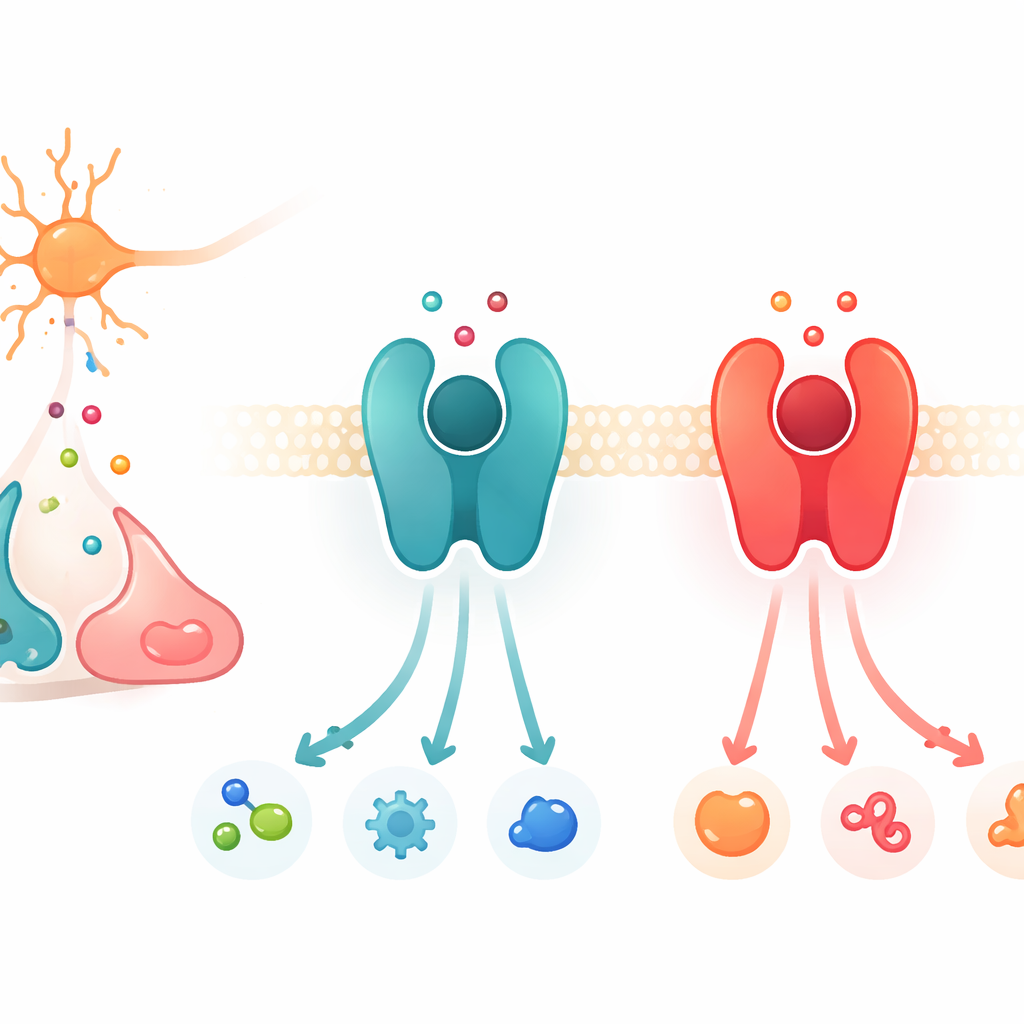
Tableaux de commutation des signaux à la surface des cellules
Le travail se concentre sur une grande famille de protéines appelées récepteurs couplés aux protéines G, ou RCPG (GPCR en anglais). Ces protéines sont intégrées dans la membrane cellulaire et fonctionnent comme des tableaux de commutation : lorsqu’un messager chimique se lie à l’extérieur, le récepteur change de conformation et active des protéines partenaires à l’intérieur, lançant une cascade de signaux. Parmi les nombreux RCPG, un sous-ensemble répond aux catécholamines, les messagers étroitement apparentés que sont la dopamine, l’adrénaline et la noradrénaline. Deux exemples clés sont le récepteur β2-adrénergique, qui préfère l’adrénaline et la noradrénaline, et le récepteur D1 de la dopamine, qui favorise la dopamine. Bien que ces récepteurs et leurs poches de liaison soient remarquablement similaires sur le plan structural, chacun est très sélectif quant au messager auquel il répond le plus fortement.
Changer les préférences avec seulement quelques modifications
Les chercheurs ont combiné des comparaisons évolutives, la biologie structurale et des mesures en cellules pour identifier des régions « chaudes » déterminant cette préférence chimique. En alignant des centaines de séquences de récepteurs issues de nombreuses espèces et en repérant où les familles β2 et D1 diffèrent de façon constante, ils ont dégagé une courte liste de positions d’acides aminés saillantes. Certaines de ces positions se situent directement dans la poche principale de liaison, où le messager s’ancre, tandis que d’autres sont légèrement plus profondes dans la protéine, à l’écart du contact direct avec la molécule. L’équipe a ensuite muté systématiquement ces positions, testant plus d’une centaine de variantes de récepteurs pour évaluer leur réponse à la dopamine, à l’adrénaline et à la noradrénaline à l’aide de mesures cellulaires de l’intensité du signal.
Ajuster les poches et les boutons de contrôle profonds
Modifier uniquement les résidus qui touchent le messager a effectivement changé la sélectivité, mais souvent au prix d’un coût élevé : les récepteurs devenaient faibles ou presque non réactifs, même lorsqu’ils commençaient à favoriser un nouveau ligand. La véritable percée est survenue lorsque les mutations de la poche de liaison ont été combinées avec des mutations dans deux régions internes imbriquées qui agissent comme des boutons de réglage internes. Dans le récepteur β2, des ajustements à une interface tri-hélice ont augmenté sa sensibilité et l’ont orienté vers un mode favorable à la dopamine sans détruire sa fonction. Dans le récepteur D1, des modifications d’une interface interne distincte ont réorganisé un réseau de chaînes latérales qui remodèlent indirectement la poche. Avec les bonnes combinaisons, les chercheurs ont complètement inversé les préférences : un récepteur β2 modifié préférait désormais la dopamine, tandis qu’un récepteur D1 modifié favorisait l’adrénaline et la noradrénaline — et les deux signalaient toujours de manière robuste.
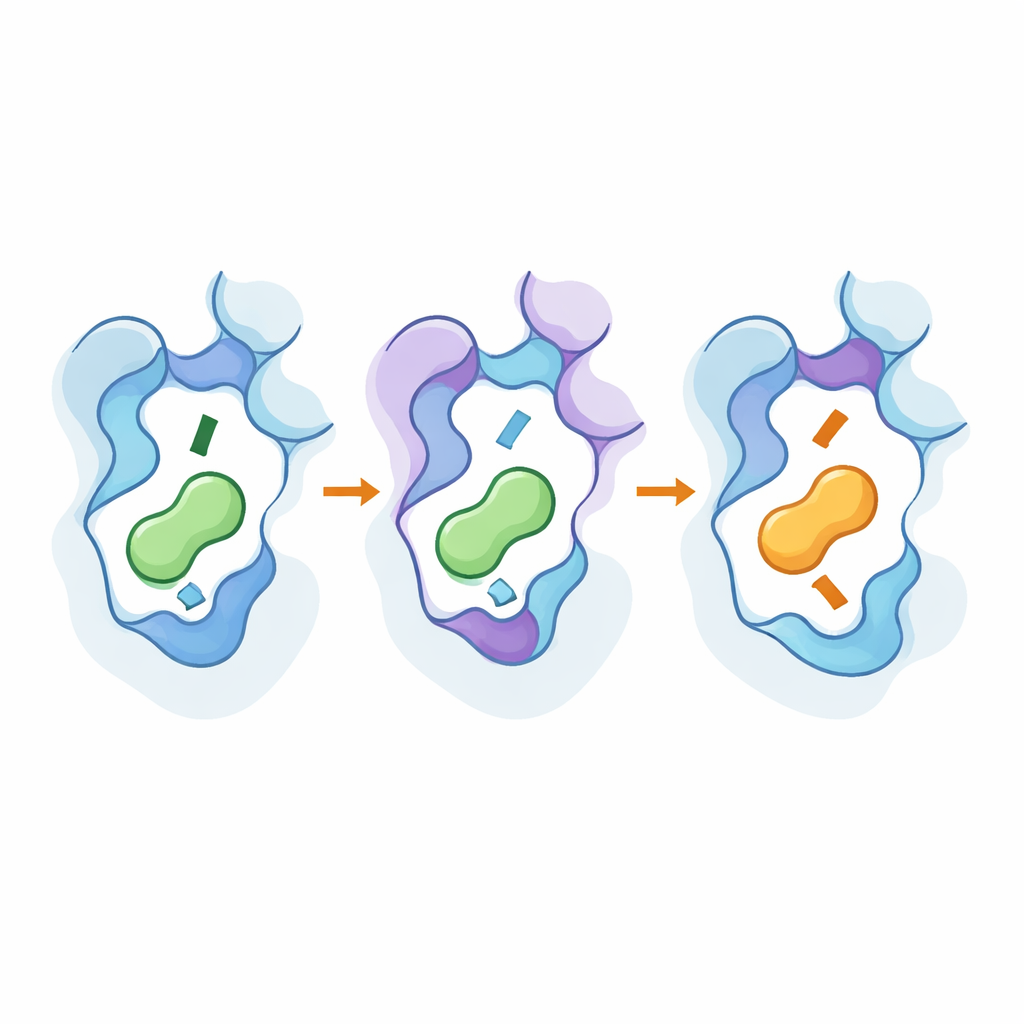
Observer le mécanisme en détail avec des outils haute résolution
Pour comprendre comment ces changements opéraient au niveau atomique, l’équipe a utilisé la cryo-microscopie électronique pour résoudre des structures 3D des récepteurs ingénierés liés à leurs nouveaux messagers préférés, et a réalisé de longues simulations de dynamique moléculaire. Les structures ont montré que des mutations clés déplaçaient subtilement des portions du septième hélice du récepteur et un résidu « bascule » conservé, approfondissant ou affaissant la poche et modifiant la façon dont l’extrémité amine du messager se positionne. Les hotspots éloignés ont contribué à stabiliser des conformations proches de l’état actif et ont renforcé des voies qui transmettent l’événement de liaison vers l’intérieur de la protéine. Les simulations ont confirmé que des réseaux de résidus en interaction relient ces régions externes et internes, et qu’un petit ensemble de positions peut être réutilisé à travers des sous-types de récepteurs apparentés pour inverser la sélectivité sans rendre les récepteurs largement promiscuous.
Ce que cela signifie pour la médecine et l’évolution
En termes simples, l’étude montre qu’une poignée d’« atomes » bien choisis dans ces récepteurs agissent comme des vis de réglage qui déterminent si une protéine écoute principalement la dopamine ou l’adrénaline. Ces vis ne sont pas toutes à la surface où le messager s’ancre ; certaines sont enfouies plus profondément et stabilisent la façon dont l’ensemble de la structure fléchit à l’arrivée d’un signal. Parce que la même logique de conception se répète au sein des familles de récepteurs, l’évolution peut réutiliser à plusieurs reprises des échafaudages protéiques similaires pour de nouveaux messagers en augmentant d’abord la réactivité par des ajustements internes, puis en affinant la poche. Pour la découverte de médicaments, ces connaissances pointent vers des emplacements précis — à l’intérieur et autour du site de liaison — que les chimistes peuvent cibler pour concevoir des médicaments qui frappent un sous-type de récepteur tout en épargnant les autres, et pour concevoir des récepteurs sur mesure qui répondent uniquement à des signaux conçus dans des thérapies et des biosenseurs.
Citation: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
Mots-clés: Récepteurs couplés aux protéines G, dopamine, adrénaline, sélectivité des ligands, conception de médicaments