Clear Sky Science · es
Mecanismos moleculares de la selectividad de ligando nativo en los receptores acoplados a proteínas G para catecolaminas
Cómo las células distinguen señales parecidas
Nuestro cerebro y cuerpo dependen de diminutos mensajeros químicos —como la dopamina y la adrenalina— para transmitir instrucciones entre células. Estas moléculas son sorprendentemente parecidas, pero cada una debe desencadenar la respuesta correcta en el lugar adecuado, ya sea agudizar la atención, acelerar el corazón o elevar el estado de ánimo. Este estudio plantea una pregunta aparentemente sencilla: ¿cómo consiguen moléculas casi idénticas «marcar» distintos números celulares, y podemos reprogramar deliberadamente esos números para la medicina y la bioingeniería?
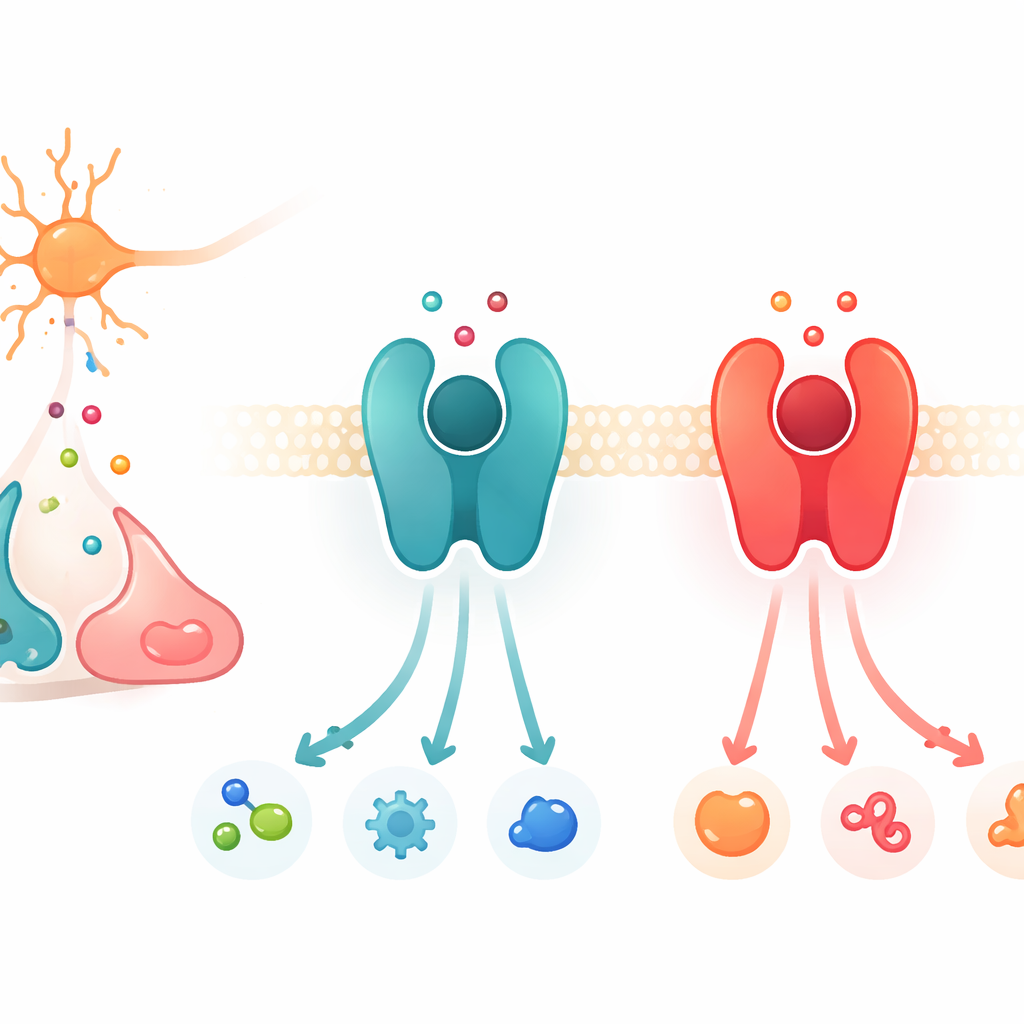
Centralitas de señales en la superficie celular
El trabajo se centra en una gran familia de proteínas llamadas receptores acoplados a proteínas G, o GPCR. Estas proteínas se encuentran en la membrana celular y actúan como centralitas: cuando un mensajero químico se une por fuera, el receptor cambia de forma y activa proteínas asociadas en el interior, iniciando una cascada de señales. Entre los muchos GPCR, un subconjunto responde a catecolaminas, los mensajeros estrechamente relacionados dopamina, adrenalina y noradrenalina. Dos ejemplos clave son el receptor β2-adrenérgico, que prefiere adrenalina y noradrenalina, y el receptor D1 de dopamina, que favorece la dopamina. Aunque estos receptores y sus bolsillos de unión son estructuralmente muy similares, cada uno es extraordinariamente selectivo respecto a qué mensajero responde con mayor intensidad.
Intercambiar preferencias con solo unos pocos cambios
Los investigadores combinaron comparaciones evolutivas, biología estructural y medidas celulares para localizar regiones «críticas» que determinan esta preferencia química. Alineando cientos de secuencias de receptores de muchas especies y puntuando dónde las familias β2 y D1 difieren de forma consistente, hallaron una lista corta de posiciones de aminoácidos destacadas. Algunas de estas posiciones se encuentran directamente en el bolsillo de unión principal, donde atraca el mensajero, mientras que otras están algo más profundas en la proteína, alejadas del contacto directo con la molécula. El equipo mutó sistemáticamente estas posiciones, probando más de un centenar de variantes de receptores para evaluar cómo respondían a dopamina, adrenalina y noradrenalina mediante lecturas celulares de la intensidad de la señalización.
Ajustando bolsillos y mandos de control internos
Alterar solo los residuos que tocan el mensajero sí cambió la selectividad, pero a menudo con un coste elevado: los receptores se volvieron débiles o casi insensibles, incluso cuando empezaban a favorecer un nuevo ligando. El verdadero avance llegó cuando las mutaciones en el bolsillo de unión se combinaron con cambios en dos regiones internas entrelazadas que funcionan como mandos de control. En el receptor β2, ajustes en una interfaz de tres hélices aumentaron su sensibilidad y lo empujaron hacia un modo más afín a la dopamina sin destruir su función. En el receptor D1, ediciones en otra interfaz interna reorganizaron una red de cadenas laterales que remodela indirectamente el bolsillo. Con las combinaciones adecuadas, los investigadores intercambiaron por completo las preferencias: un β2 modificado pasó a preferir dopamina, mientras que un D1 modificado favoreció adrenalina y noradrenalina —y ambos siguieron señalando con solidez.
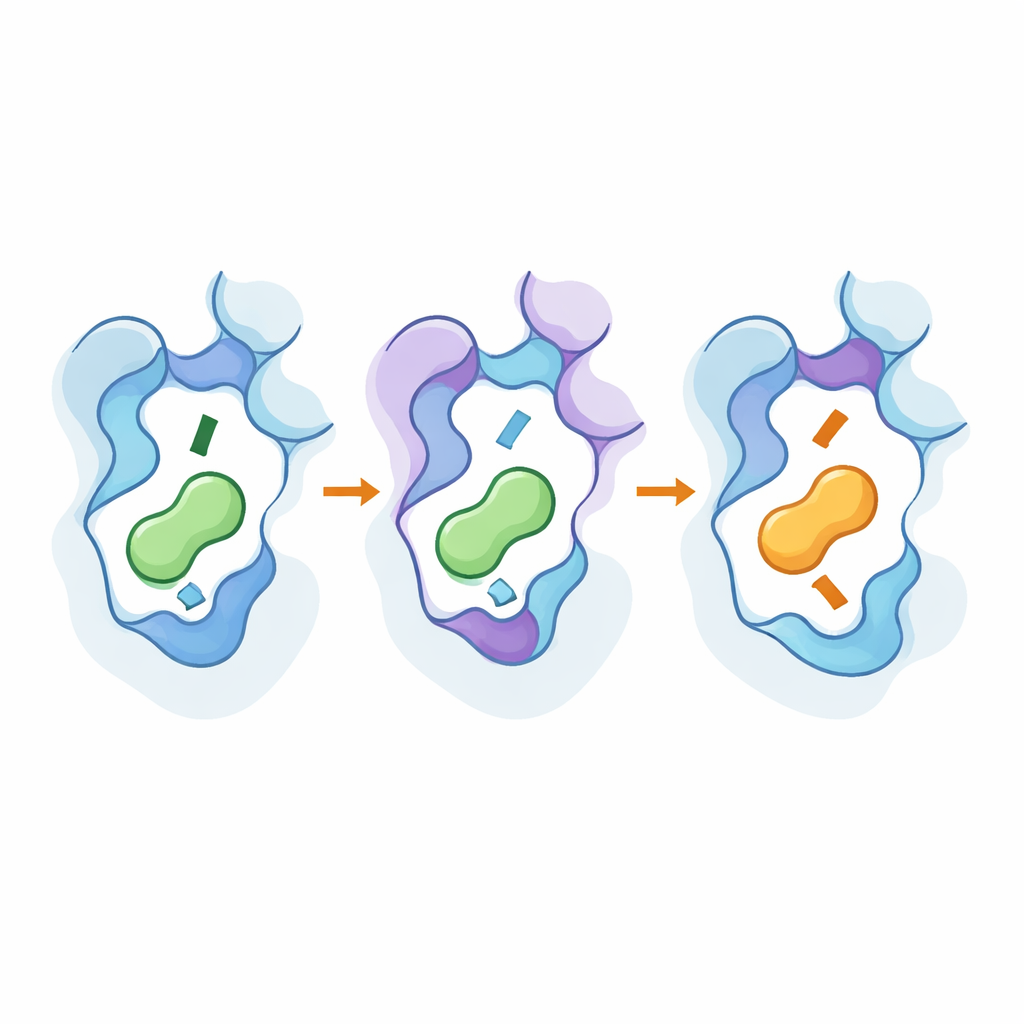
Mirar bajo el capó con herramientas de alta resolución
Para ver cómo funcionaban estos cambios a nivel atómico, el equipo usó criomicroscopía electrónica para resolver estructuras 3D de los receptores diseñados unidos a sus nuevos mensajeros preferidos, y realizó extensas simulaciones de dinámica molecular. Las estructuras mostraron que mutaciones clave desplazaron sutilmente partes de la séptima hélice del receptor y un residuo «conmutador» conservado, profundizando o haciendo más superficial el bolsillo y cambiando cómo se posiciona el extremo amina del mensajero. Los puntos críticos lejanos ayudaron a estabilizar conformaciones similares a las activas y reforzaron las vías que transmiten el evento de unión hacia el interior de la proteína. Las simulaciones confirmaron que redes de residuos en interacción enlazan estas regiones externas e internas, y que el mismo pequeño conjunto de posiciones puede reutilizarse entre subtipos de receptores relacionados para invertir la selectividad sin volver a los receptores ampliamente promíscuos.
Qué significa esto para la medicina y la evolución
En términos sencillos, el estudio muestra que un puñado de «átomos» bien escogidos en estos receptores actúan como tornillos de ajuste que deciden si una proteína escucha principalmente dopamina o adrenalina. Esos tornillos no están todos en la superficie donde se une el mensajero; algunos están enterrados más profundamente, estabilizando cómo toda la estructura se flexiona cuando llega una señal. Dado que la misma lógica de diseño se repite entre familias de receptores, la evolución puede reutilizar de forma recurrente andamios proteicos similares para nuevos mensajeros, primero aumentando la capacidad de respuesta mediante ajustes internos y luego afinando el bolsillo. Para el descubrimiento de fármacos, estos hallazgos señalan puntos precisos —tanto dentro como alrededor del sitio de unión— que los químicos pueden atacar para diseñar medicamentos que afecten a un subtipo de receptor y respeten a otros, y para crear receptores a medida que respondan solo a señales diseñadas en terapias y biosensores.
Cita: Kahlous, N.A., Rinne, M.K., Zhang, X. et al. Molecular mechanisms of native ligand selectivity in catecholamine G protein-coupled receptors. Nat Commun 17, 4112 (2026). https://doi.org/10.1038/s41467-026-71361-8
Palabras clave: Receptores acoplados a proteínas G, dopamina, adrenalina, selectividad de ligando, diseño de fármacos