Clear Sky Science · zh
粘附G蛋白偶联受体中GAIN结构域自切割与抗切割的结构基础
细胞表面受体如何像微小的自切割机器一样工作
我们的细胞表面布满复杂的受体蛋白,用以感知外界环境。其中一些被称为粘附型G蛋白偶联受体(aGPCRs),行为类似微小的自切割机器:蛋白质的一段可以自行切断,改变受体的信号传递方式。本研究提出了一个看似简单但对大脑功能和药物设计影响深远的问题:为什么有些受体很容易自切,而紧密相关的受体却顽固地抗切?
黏附受体上的隐性开关
粘附型G蛋白偶联受体帮助细胞与周围环境粘附并与邻近细胞交流。这类受体的一个特征是体积较大的外部区域,其中包含所谓的GAIN结构域。埋藏在该结构域内部的是一段短的“系留激动剂”片段,当暴露时可激活受体。在许多aGPCR中,GAIN结构域中的一小段蛋白链能够在特定位点自行切割,将受体的外部部分分为N端和C端片段。切割发生在包含组氨酸和丝氨酸或苏氨酸的特定残基序列旁,人们认为该序列充当内建的化学刀。
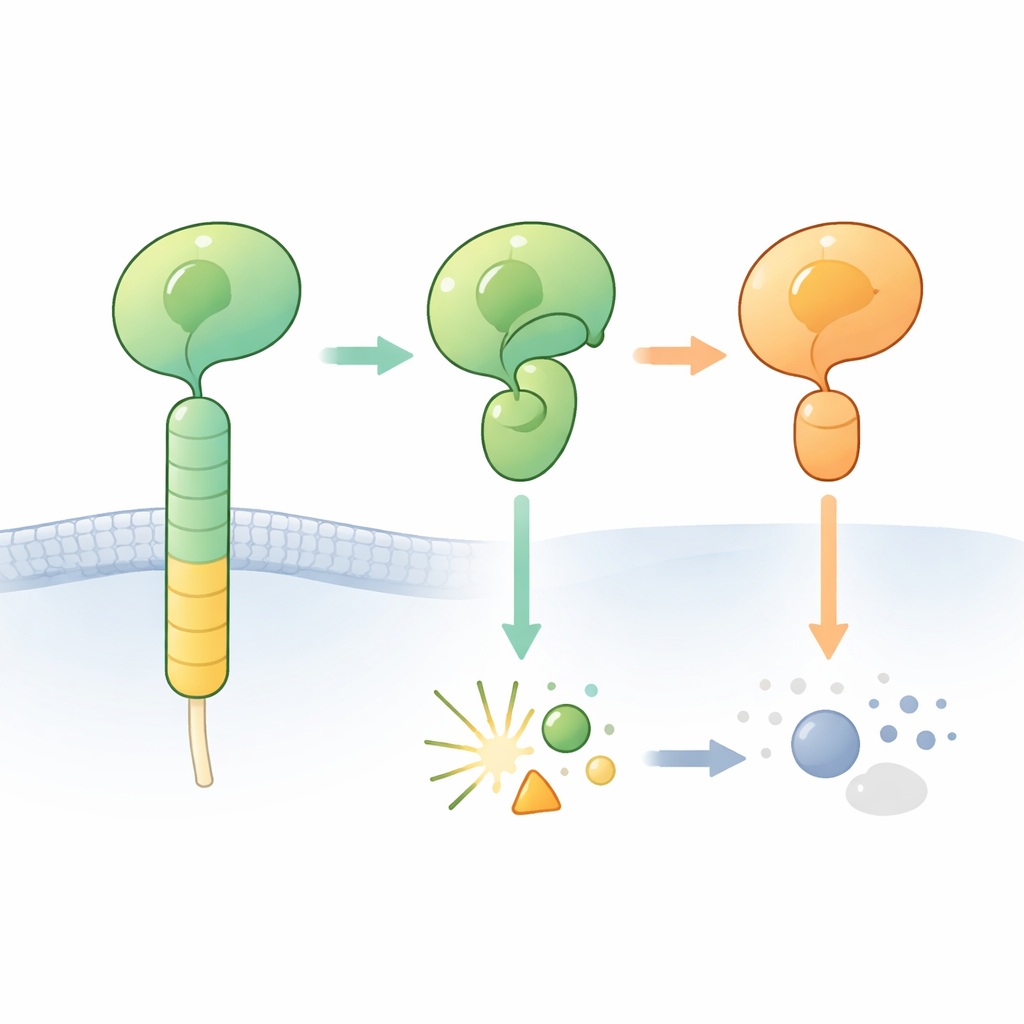
当预期的切割未发生时
研究人员聚焦于一种脑部受体ADGRB2(亦称BAI2),其GAIN结构域带有“合适”的组氨酸–亮氨酸–丝氨酸序列,但令人费解地难以被切割。他们解析了人类ADGRB2中激素受体样域与GAIN区域的高分辨率晶体结构。出人意料的是,切割位点位于一个水分子可到达的开放沟槽中,但关键的组氨酸和丝氨酸侧链朝向并不利于发生化学反应:它们需要扭转到不同的位置才能启动反应。加热纯化蛋白或加入通常能促使停滞自切反应完成的化学物质也未能触发切割,证实在这些条件下ADGRB2天生具有抗切割性。
细小的芳环相互作用引导化学打击
为理解是什么让其他受体更“易切”,团队将ADGRB2与那些高效切割的家族成员进行比较,并开展了大量分子动力学模拟,让原子在计算机上自由抖动移动。一个关键见解浮现:在具备切割能力的受体中,切割位点的组氨酸会靠在附近的苯丙氨酸或酪氨酸侧链上,形成一种T形的芳环对芳环相互作用。这种轻微的推挤将组氨酸锁定在一种优先取向,使其能够从丝氨酸或苏氨酸上抽取质子,将该基团转变为对肽键具有强烈进攻性的核亲电体。在ADGRB2中,该位点的苯丙氨酸被丝氨酸替代,并且附近的主链区域被更大侧链扭曲,因此组氨酸处于“攻击准备”姿态的时间远低于切割能手。模拟还显示,在有效切割的受体中,待断裂的肽键常常略有扭曲,储存了有利于断裂的应变能。
可调节的柔性环作为杠杆
除芳环相互作用外,GAIN结构域还包含松软的环状区域或“襟翼”,它们围绕切割沟槽。这些环在不同受体间差异很大,进化上并不高度保守,但事实证明它们对完全活性至关重要。通过在一个通常具备切割能力的受体(ADGRL1)与ADGRB2之间替换襟翼片段,作者能够调节切割速率的高低。在合适位置引入类似苯丙氨酸的残基使得通常不活跃的近亲ADGRB3恢复了一定的自切割能力,尤其是在催化位点存在组氨酸时。相反,在活性受体中突变稳定组氨酸取向的苯丙氨酸或移植ADGRB2样的襟翼则削弱了切割能力。这些实验表明,精确的局部化学环境与长而可动的环共同协作,将蛋白推入一种带应变的反应性构象。
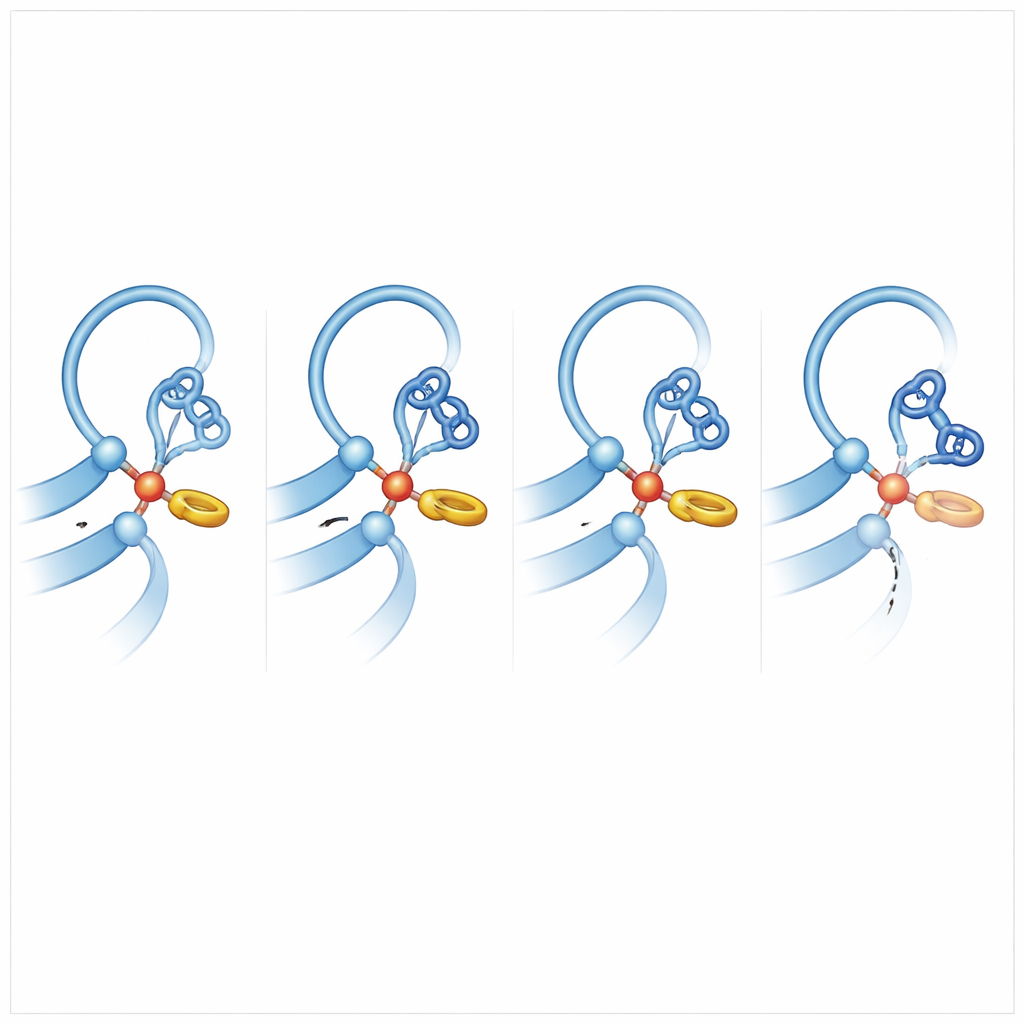
为什么一些受体保持完整
在接近150个哺乳动物ADGRB2同源物的比较中,团队发现大多数缺乏理想的切割位点组氨酸,而且它们的襟翼和附近残基高度可变。结合纯化ADGRB2中约100天的切割半衰期测定,这表明许多BAI2样受体被设计为避免快速自切。相反,它们可能在从未切割的情况下发挥信号功能,或通过在特定组织中发生非常缓慢或依赖情境的切割来传递信号。更广泛地讲,这项工作表明这些受体中的自处理并非由三字母动机简单控制的开/关开关。相反,它源自侧链堆积、主链应变和可动环的微妙平衡,共同调节GAIN结构域是充当内建刀刃还是保持安全锁定。理解这种平衡最终或可让研究者设计出能在稳定与自切割状态之间切换受体的药物,从而改变细胞感知机械力和化学信号的方式。
引用: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
关键词: 粘附型GPCR, GAIN结构域, 自切割, 蛋白质结构, 分子动力学