Clear Sky Science · nl
Structurele basis van GAIN-domeinautoproteolyse en snij‑resistentie in adhesie G‑proteïnegekoppelde receptoren
Hoe celmembraanreceptoren als kleine zelfsnijdende machines functioneren
Onze cellen zijn bedekt met complexe receptorproteïnen die de buitenwereld waarnemen. Sommige daarvan, adhesie G‑proteïnegekoppelde receptoren genoemd, gedragen zich als kleine zelfsnijdende machines: een deel van het eiwit kan zichzelf doorsnijden, waardoor het signaalgedrag van de receptor verandert. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote implicaties voor hersenfunctie en geneesmiddelontwerp: waarom snijden sommige van deze receptoren zichzelf gemakkelijk, terwijl nauwverwante exemplaren hardnekkig weerstand bieden?
Een verborgen schakel op plakkerige celreceptoren
Adhesie G‑proteïnegekoppelde receptoren (aGPCR’s) helpen cellen zich aan hun omgeving te hechten en met burencellen te communiceren. Een kenmerk van deze receptoren is een omvangrijke buitenste regio die het zogeheten GAIN‑domein bevat. Verborgen in dit domein ligt een korte “gebonden agonist”‑sectie die de receptor kan inschakelen wanneer die blootgelegd wordt. In veel aGPCR’s kan een klein segment van de eiwitketen in het GAIN‑domein zichzelf op een specifieke plaats doorsnijden, waarbij het buitenste deel van de receptor in een N‑terminaal en een C‑terminaal fragment splitst. De knip vindt plaats naast een bepaalde opeenvolging van bouwstenen die een histidine en een serine of threonine bevat en waarvan wordt gedacht dat die functioneert als een ingebouwde chemische scalpel.
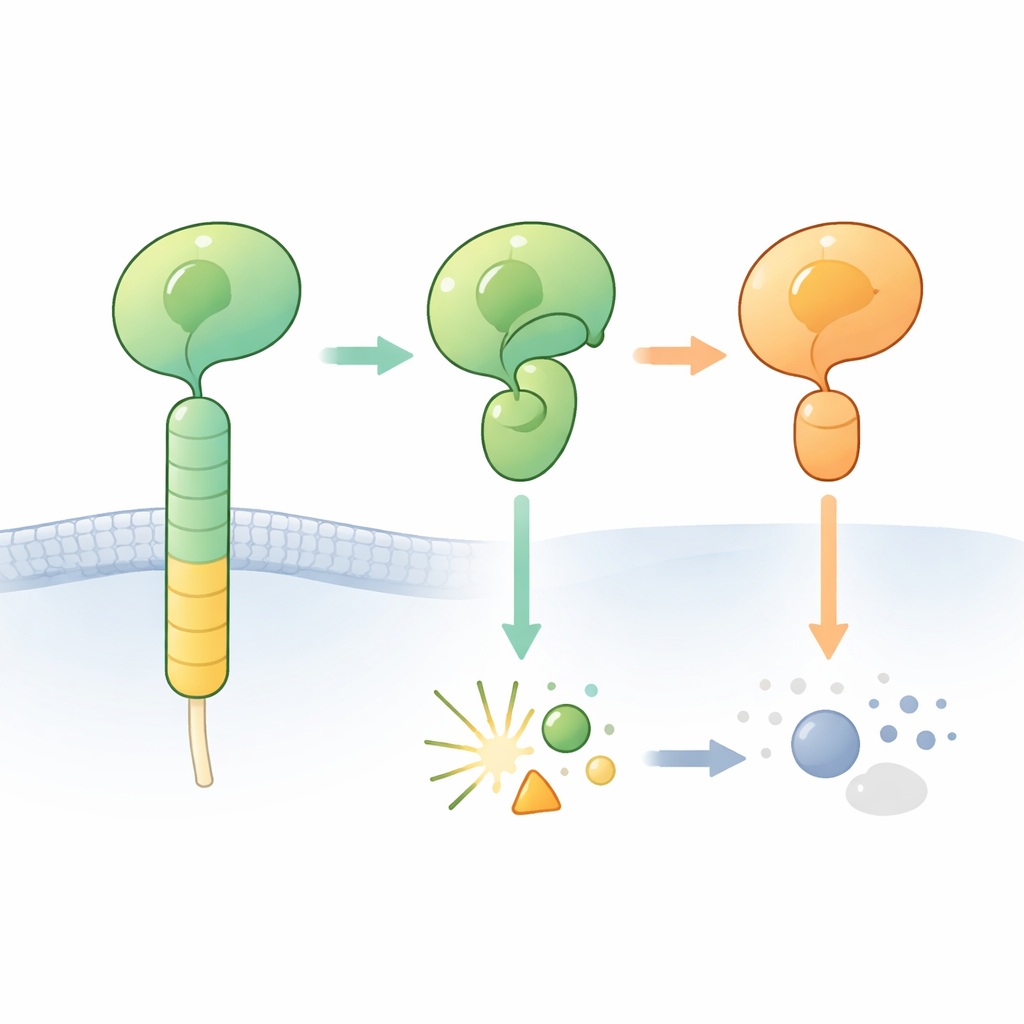
Wanneer de verwachte knip uitblijft
De onderzoekers zoomen in op één hersenreceptor, ADGRB2 (ook bekend als BAI2), waarvan het GAIN‑domein de “juiste” histidine‑leucine‑serine‑volgorde draagt maar opmerkelijk moeilijk te knippen is. Ze bepaalden een hoogresolutie‑kristalstructuur van de hormoonreceptor‑achtige en GAIN‑regio’s van menselijk ADGRB2. Verrassend genoeg ligt de knipplaats in een open groef die toegankelijk is voor watermoleculen, maar de sleutel‑zijketens van histidine en serine zijn georiënteerd op een manier die niet klaar is voor chemie: ze zouden moeten draaien naar andere posities om de reactie te starten. Verhitting van het gezuiverde eiwit of toevoeging van chemicaliën die normaal vastgelopen zelfknipreacties voltooien, activeerde de knip niet, wat bevestigt dat ADGRB2 onder deze omstandigheden van nature knip‑resistent is.
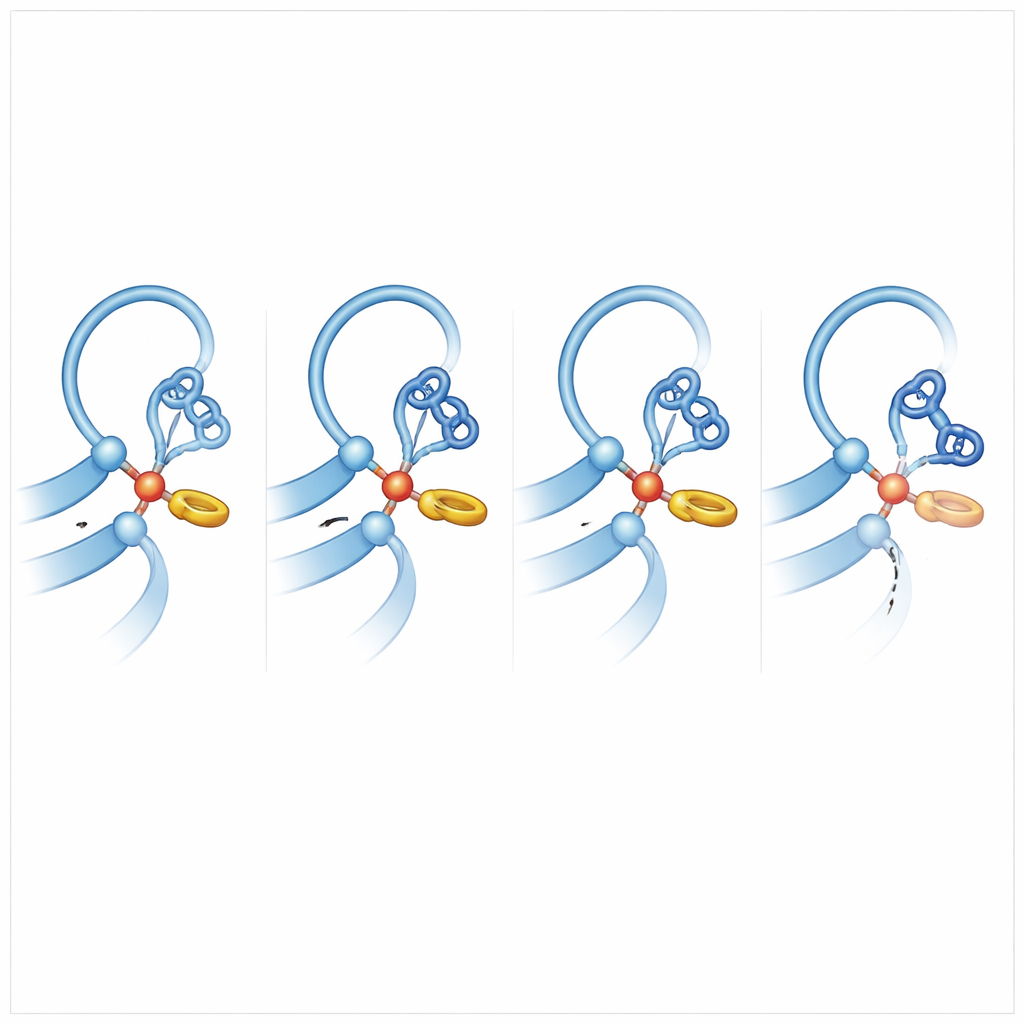
Subtiele ringinteracties sturen de chemische slag
Om te begrijpen wat andere receptoren meer “snijlustig” maakt, vergeleek het team ADGRB2 met familieleden die efficiënt knippen en voerden uitgebreide moleculaire dynamicasimulaties uit, waarbij atomen op de computer konden trillen en verschuiven. Een belangrijke inzicht kwam naar voren: bij knip‑competente receptoren nestelt de histidine bij de knipplaats zich tegen een nabijgelegen fenylalanine‑ of tyrosine‑zijketen in een T‑vormige ring‑tot‑ringinteractie. Deze zachte duw vergrendelt de histidine in een voorkeurshouding die hem uitlijnt om een proton van de serine of threonine af te trekken, waardoor die groep verandert in een krachtige aanvaller van de peptidebinding. In ADGRB2 is deze fenylalanine vervangen door een serine, en het omliggende ruggegraatgebied is vervormd door een bulkier zijketen, waardoor de histidine veel minder tijd in de “aanval‑klare” houding doorbrengt. Simulaties toonden ook dat bij efficiënte knippers de peptidebinding die verbroken moet worden vaak lichtelijk verdraaid is, waardoor er spanning ontstaat die het knappen vergemakkelijkt.
Flexibele lussen als verstelbare hefbomen
Buiten deze ringinteractie bevat het GAIN‑domein losse lusregio’s, of “kleppen”, die de snijgroef omlijsten. Deze lussen variëren sterk tussen receptoren en zijn evolutionair niet sterk geconserveerd, maar blijken cruciaal voor volledige activiteit. Door klepsegmenten te wisselen tussen een normaal knip‑competente receptor (ADGRL1) en ADGRB2 konden de auteurs de knipsnelheden omhoog of omlaag regelen. Het introduceren van fenylalanine‑achtige residuen op de juiste plek herstelde enige zelfknipactiviteit in een normaal inactieve verwant, ADGRB3, vooral wanneer dit gecombineerd werd met een histidine op de katalytische positie. Omgekeerd verzwakte het muteren van de stabiliserende fenylalanine in de actieve receptor of het inbrengen van ADGRB2‑achtige kleppen de knip. Deze experimenten tonen aan dat zowel precieze lokale chemie als lange, beweeglijke lussen samenwerken om het eiwit in een gespannen, reactieve toestand te duwen.
Waarom sommige receptoren intact blijven
Bij het vergelijken van bijna 150 zoogdier‑versies van ADGRB2 vond het team dat de meeste niet de ideale histidine op de knipplaats hebben, en hun kleppen en nabijgelegen residuen zijn sterk variabel. Samen met de gemeten halfwaardetijd van ongeveer 100 dagen voor knip in gezuiverd ADGRB2 suggereert dit dat veel BAI2‑achtige receptoren ontworpen zijn om snelle zelfknip te vermijden. In plaats daarvan kunnen ze signaleren zonder ooit te knippen of door zeer langzame of context‑afhankelijke knip in specifieke weefsels te gebruiken. Breder gezien laat het werk zien dat zelfverwerking in deze receptoren geen simpele aan‑uit‑schakelaar is die door een drietalige motief wordt bestuurd. Het ontstaat eerder uit een delicate balans van zijketenpakking, ruggegraatspanning en mobiele lussen die gezamenlijk afstemmen of het GAIN‑domein als een ingebouwd mes fungeert of veilig vergrendeld blijft. Inzicht in deze balans kan onderzoekers uiteindelijk in staat stellen geneesmiddelen te ontwerpen die receptoren tussen stabiele en zelfknipende toestanden verschuiven, waarmee ze veranderen hoe cellen mechanische krachten en chemische signalen waarnemen.
Bronvermelding: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
Trefwoorden: adhesie GPCR, GAIN-domein, autoproteolyse, eiwitstructuur, moleculaire dynamica