Clear Sky Science · es
Base estructural de la autoproteólisis del dominio GAIN y la resistencia al corte en los receptores de adhesión acoplados a proteínas G
Cómo los receptores de la superficie celular actúan como pequeñas máquinas que se cortan solas
Nuestras células están cubiertas de complejos receptores proteicos que perciben el mundo exterior. Algunos de estos, llamados receptores de adhesión acoplados a proteína G, se comportan como diminutas máquinas que se cortan a sí mismas: una porción de la proteína puede separarse, cambiando la forma en que el receptor transmite señales. Este estudio plantea una pregunta aparentemente simple con grandes implicaciones para la función cerebral y el diseño de fármacos: ¿por qué algunos de estos receptores se cortan con facilidad, mientras que otros estrechamente relacionados se resisten obstinadamente?
Un interruptor oculto en receptores celulares adhesivos
Los receptores de adhesión acoplados a proteína G (aGPCRs) ayudan a las células a adherirse al entorno y a comunicarse con las células vecinas. Una característica distintiva de estos receptores es una región externa voluminosa que incluye el denominado dominio GAIN. Enterrado dentro de este dominio hay un corto segmento de “agonista tethered” que puede activar el receptor cuando queda expuesto. En muchos aGPCRs, una pequeña sección de la cadena proteica en el dominio GAIN puede cortarse a sí misma en un sitio específico, dividiendo la porción externa del receptor en un fragmento N‑terminal y otro C‑terminal. El corte ocurre junto a una secuencia de bloques constructores particular que incluye una histidina y una serina o treonina, y se piensa que actúa como un cuchillo químico integrado.
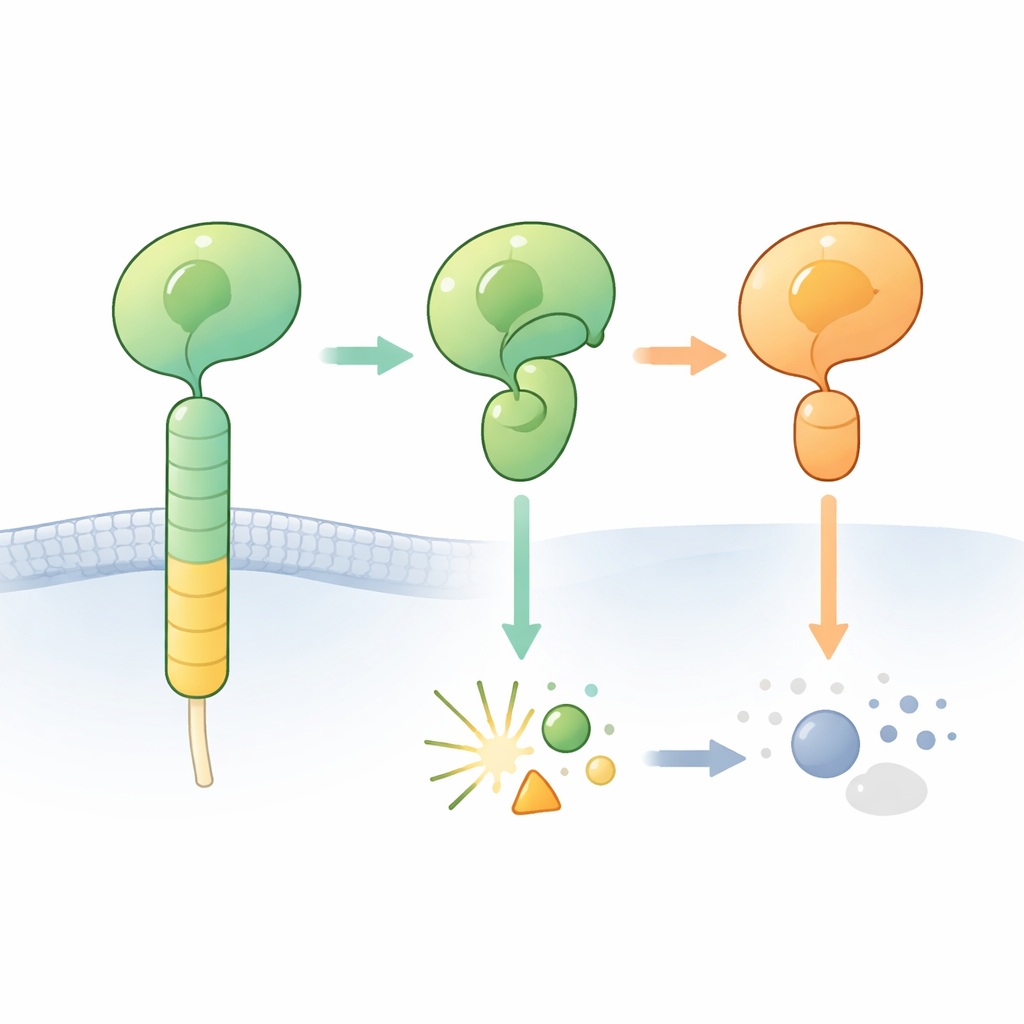
Cuando el corte esperado nunca ocurre
Los investigadores se centraron en un receptor cerebral, ADGRB2 (también conocido como BAI2), cuyo dominio GAIN contiene la secuencia “correcta” histidina‑leucina‑serina pero que, de forma intrigante, es difícil de cortar. Determinaron la estructura cristalina de alta resolución de las regiones tipo receptor de hormonas y GAIN de ADGRB2 humana. Sorprendentemente, el sitio de escisión se sitúa en una ranura abierta accesible al agua, pero las cadenas laterales clave de la histidina y la serina están orientadas de un modo que no es químicamente competente: necesitarían girar a posiciones diferentes para iniciar la reacción. Calentar la proteína purificada o añadir químicos que normalmente empujan reacciones de autocorte estancadas hacia su conclusión no provocó la escisión, confirmando que ADGRB2 es naturalmente resistente al corte bajo estas condiciones.
Interacciones sutiles entre anillos dirigen el ataque químico
Para entender qué hace que otros receptores sean más proclives al corte, el equipo comparó ADGRB2 con miembros de la familia que se escinden con eficacia y realizó extensas simulaciones de dinámica molecular, dejando que los átomos se bamboleen y reorganicen en el ordenador. Surgió una idea clave: en los receptores competentes para el corte, la histidina en el sitio de escisión se apoya contra una cadena lateral cercana de fenilalanina o tirosina en una interacción anillo‑a‑anillo en forma de T. Este empujón sutil bloquea la histidina en una orientación preferida que la alinea para extraer un protón de la serina o treonina, convirtiendo ese grupo en un atacante potente del enlace peptídico. En ADGRB2, esta fenilalanina está sustituida por una serina, y la región del esqueleto cercana está distorsionada por una cadena lateral más voluminosa, por lo que la histidina pasa mucho menos tiempo en la pose «lista para atacar». Las simulaciones también mostraron que en los rompientes eficientes, el enlace peptídico a romper suele estar ligeramente torsionado, acumulando tensión que facilita su ruptura.
Bucle flexibles como palancas ajustables
Más allá de esta interacción entre anillos, el dominio GAIN contiene regiones de bucles flexibles, o “solapas”, que enmarcan la ranura de corte. Estos bucles varían ampliamente entre receptores y no están fuertemente conservados evolutivamente, sin embargo resultan cruciales para la actividad completa. Al intercambiar segmentos de solapa entre un receptor normalmente competente para el corte (ADGRL1) y ADGRB2, los autores pudieron aumentar o disminuir las velocidades de escisión. Introducir residuos tipo fenilalanina en el lugar adecuado restauró cierta capacidad de autocorte a un pariente normalmente inactivo, ADGRB3, especialmente cuando se combinó con una histidina en la posición catalítica. Por el contrario, mutar la fenilalanina estabilizadora en el receptor activo o introducir solapas similares a las de ADGRB2 debilitó la escisión. Estos experimentos muestran que tanto la química local precisa como los bucles largos y móviles cooperan para empujar la proteína hacia un estado tenso y reactivo.
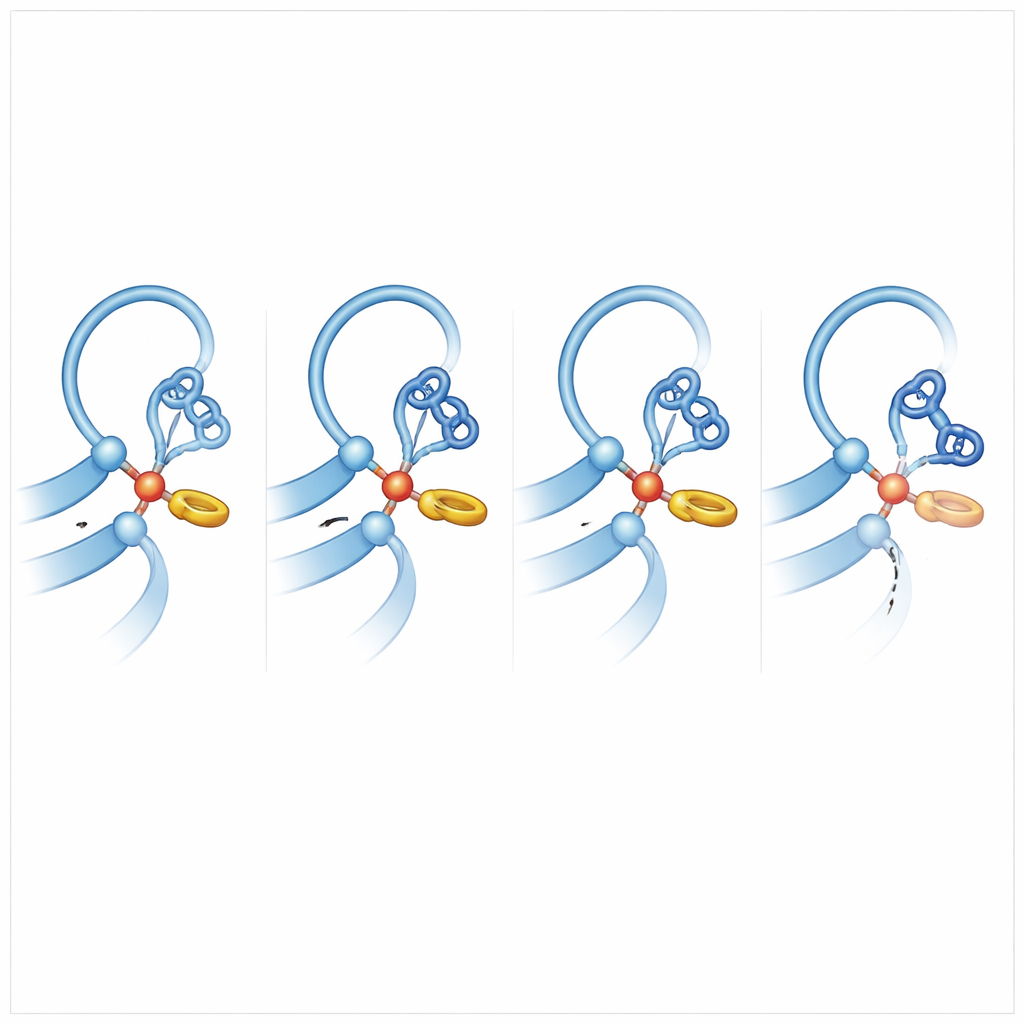
Por qué algunos receptores permanecen intactos
Al analizar casi 150 versiones mamíferas de ADGRB2, el equipo encontró que la mayoría carece de la histidina ideal en el sitio de escisión, y sus solapas y residuos cercanos son altamente variables. Junto con la vida media medida de aproximadamente 100 días para la escisión en ADGRB2 purificado, esto sugiere que muchos receptores del tipo BAI2 están diseñados para evitar un autocorte rápido. En su lugar, pueden señalizar sin llegar a escindirse o mediante un corte muy lento o dependiente del contexto en tejidos específicos. De forma más general, el trabajo muestra que el autoprocese en estos receptores no es un simple interruptor controlado por un motivo de tres letras. Más bien, surge de un delicado equilibrio entre el empaquetamiento de cadenas laterales, la tensión del esqueleto y los bucles móviles que en conjunto ajustan si el dominio GAIN actúa como un cuchillo integrado o permanece seguro y bloqueado. Comprender este equilibrio podría permitir a los investigadores diseñar fármacos que desplacen los receptores entre estados estables y de autocorte, cambiando la forma en que las células perciben fuerzas mecánicas y señales químicas.
Cita: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
Palabras clave: receptor de adhesión GPCR, dominio GAIN, autoproteólisis, estructura de proteínas, dinámica molecular