Clear Sky Science · fr
Base structurale de l'autoclivage du domaine GAIN et résistance à la coupure chez les récepteurs adhésifs couplés aux protéines G
Comment des récepteurs de surface cellulaire agissent comme de petites machines qui se coupent elles‑mêmes
Nos cellules sont couvertes de récepteurs protéiques élaborés qui perçoivent le monde extérieur. Certains d’entre eux, appelés récepteurs adhésifs couplés aux protéines G, se comportent comme de petites machines s’auto‑coupant : un segment de la protéine peut se scinder lui‑même, modifiant la façon dont le récepteur transmet un signal. Cette étude pose une question apparemment simple mais aux grandes implications pour le fonctionnement du cerveau et la conception de médicaments : pourquoi certains de ces récepteurs se coupent‑ils facilement, tandis que d’autres, très proches, résistent obstinément ?
Un interrupteur caché sur des récepteurs cellulaires collants
Les récepteurs adhésifs couplés aux protéines G (aGPCR) aident les cellules à s’attacher à leur environnement et à communiquer avec leurs voisines. Une caractéristique de ces récepteurs est une région externe volumineuse qui inclut le soi‑disant domaine GAIN. Enfoui à l’intérieur de ce domaine se trouve un court segment « agoniste lié » qui, une fois exposé, peut activer le récepteur. Dans de nombreux aGPCR, une minuscule portion de la chaîne protéique du domaine GAIN peut se couper elle‑même en un site spécifique, scindant la partie externe du récepteur en un fragment N‑terminal et un fragment C‑terminal. La coupure se produit à côté d’une séquence particulière d’acides aminés comprenant une histidine et une sérine ou thréonine et est considérée comme agissant comme un couteau chimique intégré.
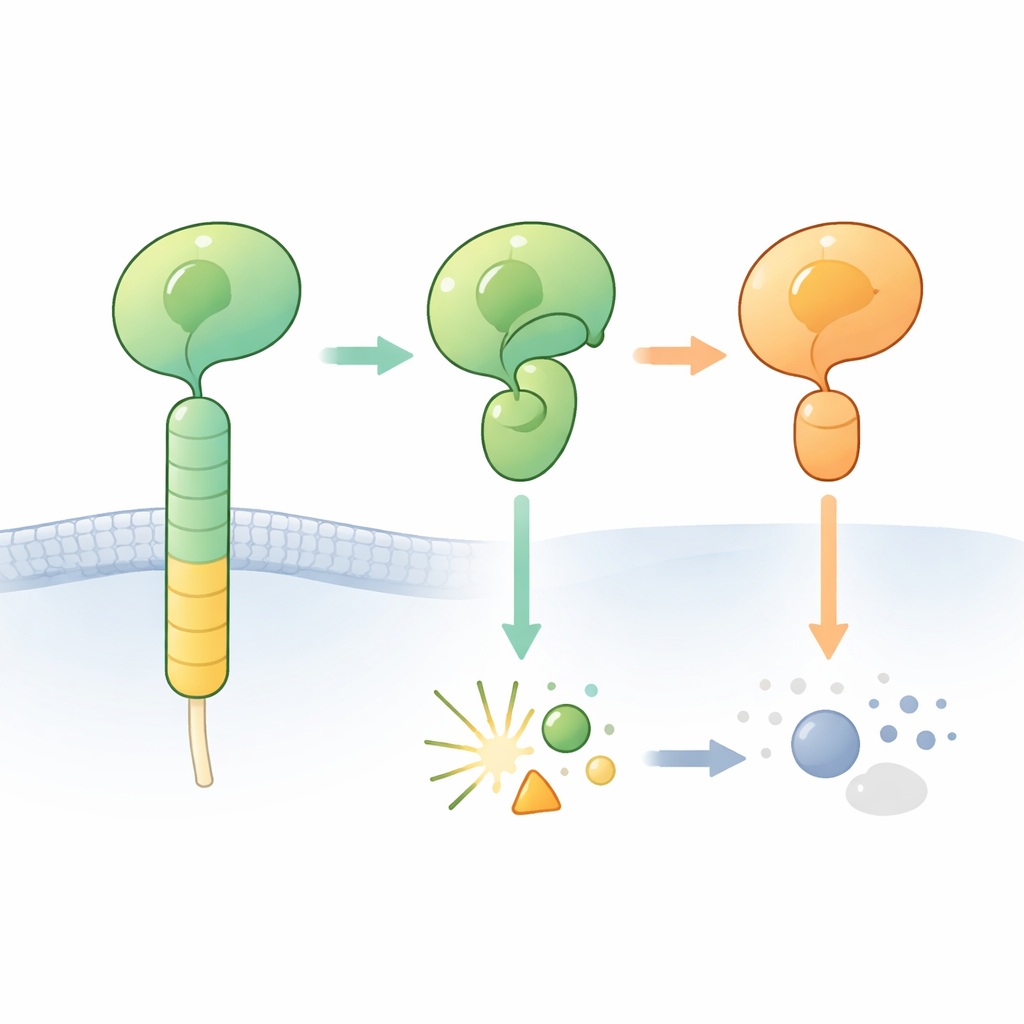
Quand la coupure attendue n’a jamais lieu
Les chercheurs se sont focalisés sur un récepteur cérébral, ADGRB2 (également connu sous le nom BAI2), dont le domaine GAIN contient la séquence « correcte » histidine–leucine–sérine mais qui, de manière intrigante, est difficile à cliver. Ils ont déterminé une structure cristalline à haute résolution des régions de type récepteur d’hormone et du domaine GAIN d’ADGRB2 humain. De façon surprenante, le site de coupure se trouve dans une gorge ouverte accessible à des molécules d’eau, mais les chaînes latérales clés de l’histidine et de la sérine sont orientées d’une manière non propice à la réaction : elles devraient se réorienter pour initier la réaction. Chauffer la protéine purifiée ou ajouter des réactifs qui favorisent normalement l’achèvement d’autoclivages bloqués n’a pas déclenché la coupure, confirmant qu’ADGRB2 est naturellement résistant à la coupure dans ces conditions.
Des interactions d’anneaux subtiles dirigent la frappe chimique
Pour comprendre ce qui rend d’autres récepteurs plus enclins à se couper, l’équipe a comparé ADGRB2 à des membres de la famille qui se clivent efficacement et a exécuté de longues simulations de dynamique moléculaire, laissant les atomes vibrer et se réarranger sur l’ordinateur. Un insight clé a émergé : dans les récepteurs compétents pour la coupure, l’histidine au site de clivage s’appuie contre une chaîne latérale voisine de phénylalanine ou de tyrosine dans une interaction anneau‑à‑anneau en T. Cette poussée douce verrouille l’histidine dans une orientation préférée qui la met en position d’arracher un proton à la sérine ou à la thréonine, transformant ce groupe en un attaquant puissant de la liaison peptidique. Dans ADGRB2, cette phénylalanine est remplacée par une sérine, et la région du squelette peptidique à proximité est déformée par une chaîne latérale plus volumineuse, de sorte que l’histidine passe beaucoup moins de temps en position « prête à attaquer ». Les simulations ont aussi montré que, chez les coupeurs efficaces, la liaison peptidique à rompre est souvent légèrement tordue, accumulant une contrainte qui facilite la rupture.
Boucles flexibles comme leviers ajustables
Au‑delà de cette interaction d’anneaux, le domaine GAIN contient des régions de boucles souples, ou « rabats », qui encadrent la gorge de clivage. Ces boucles varient largement entre les récepteurs et ne sont pas fortement conservées au cours de l’évolution, pourtant elles s’avèrent cruciales pour l’activité complète. En échangeant des segments de rabats entre un récepteur normalement compétent pour la coupure (ADGRL1) et ADGRB2, les auteurs ont pu régler les taux de clivage à la hausse ou à la baisse. L’introduction de résidus semblables à la phénylalanine au bon endroit a restauré une certaine capacité d’autoclivage à une cousine normalement inactive, ADGRB3, en particulier lorsqu’elle était combinée avec une histidine à la position catalytique. Inversement, muter la phénylalanine stabilisante dans le récepteur actif ou greffer des rabats de type ADGRB2 a affaibli la coupure. Ces expériences montrent que la chimie locale précise et de longues boucles mobiles coopèrent pour pousser la protéine dans un état contraint et réactif.
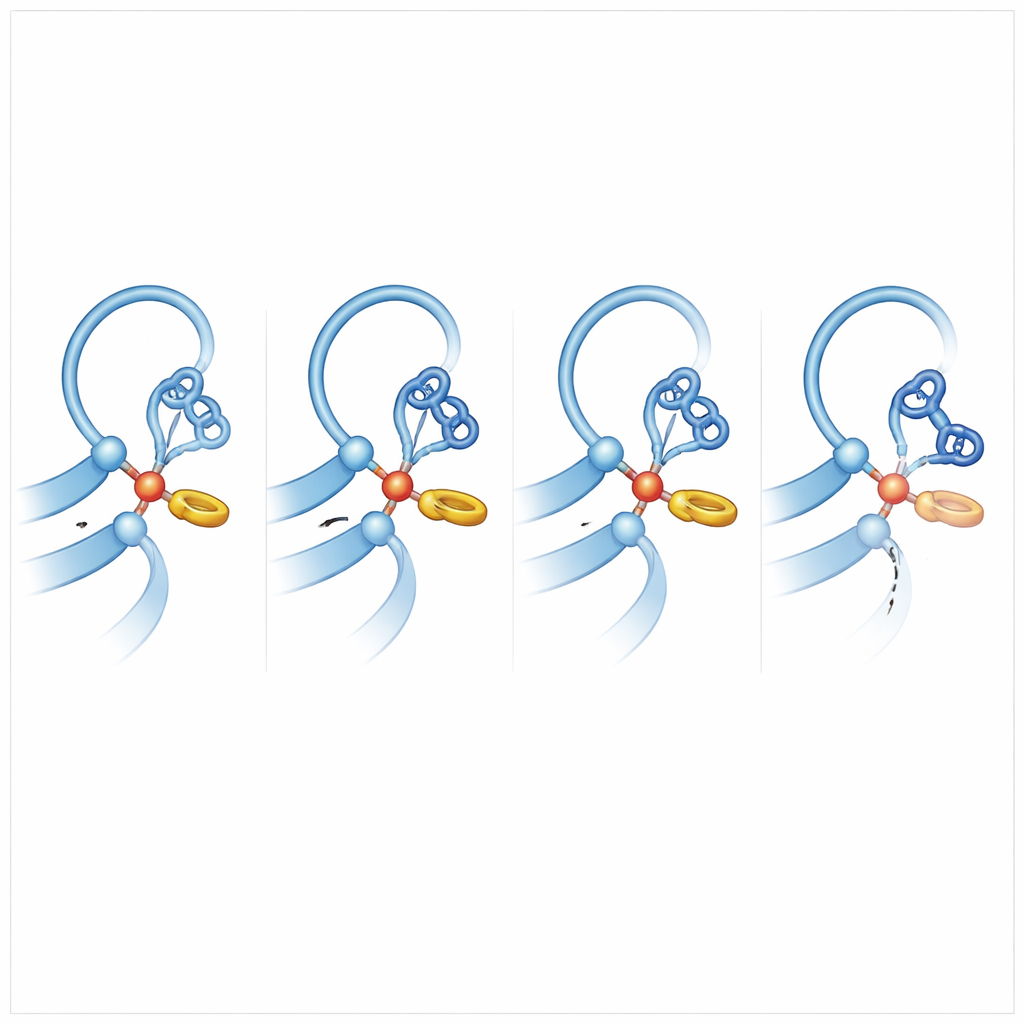
Pourquoi certains récepteurs restent intacts
En analysant près de 150 versions mammifères d’ADGRB2, l’équipe a constaté que la plupart n’ont pas l’histidine idéale au site de coupure, et que leurs rabats et résidus proches sont très variables. Conjugué à la demi‑vie mesurée d’environ 100 jours pour le clivage de la protéine ADGRB2 purifiée, cela suggère que nombre de récepteurs de type BAI2 sont conçus pour éviter un autoclivage rapide. Ils peuvent plutôt signaler sans jamais se cliver ou utiliser un clivage très lent ou dépendant du contexte dans certains tissus. De façon plus générale, le travail montre que le traitement autonome de ces récepteurs n’est pas un simple interrupteur tout‑ou‑rien contrôlé par un motif de trois lettres. Il émerge plutôt d’un équilibre délicat d’empilement de chaînes latérales, de contrainte du squelette et de boucles mobiles qui, collectivement, règlent si le domaine GAIN agit comme un couteau intégré ou reste solidement verrouillé. Comprendre cet équilibre pourrait éventuellement permettre aux chercheurs de concevoir des médicaments qui déplacent les récepteurs entre des états stables et des états autocoupants, modifiant la façon dont les cellules détectent les forces mécaniques et les signaux chimiques.
Citation: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
Mots-clés: récepteur GPCR adhésif, domaine GAIN, autoclivage, structure protéique, dynamique moléculaire