Clear Sky Science · pl
Podstawy strukturalne autoproteolizy domeny GAIN i odporności na cięcie w adhezyjnych receptorach sprzężonych z białkiem G
Jak receptory powierzchni komórkowych działają jak maleńkie samorozcinające się maszyny
Powierzchnia naszych komórek jest pokryta złożonymi białkami receptorowymi, które wyczuwają świat zewnętrzny. Niektóre z nich, zwane adhezyjnymi receptorami sprzężonymi z białkiem G, zachowują się jak maleńkie samorozcinające się maszyny: fragment białka może sam przeciąć siebie, zmieniając sposób, w jaki receptor przekazuje sygnał. W tym badaniu postawiono pozornie proste pytanie o dalekosiężnych konsekwencjach dla funkcji mózgu i projektowania leków: dlaczego niektóre z tych receptorów chętnie się tną, podczas gdy blisko spokrewnione opierają się temu?
Ukryty przełącznik na lepkich receptorach komórkowych
Adhezyjne receptory sprzężone z białkiem G (aGPCR) pomagają komórkom przyczepiać się do otoczenia i komunikować z sąsiednimi komórkami. Charakterystyczną cechą tych receptorów jest masywna zewnętrzna część zawierająca tzw. domenę GAIN. W tej domenie ukryty jest krótki segment „związany agonista”, który po odsłonięciu może włączyć receptor. W wielu aGPCR niewielki odcinek łańcucha białkowego w domenie GAIN może przeciąć się w określonym miejscu, dzieląc zewnętrzną część receptora na fragment N‑terminalny i C‑terminalny. Cięcie zachodzi obok charakterystycznego układu reszt budulcowych obejmującego histydynę oraz serynę lub treoninę i uważa się, że pełni rolę wbudowanego chemicznego noża.
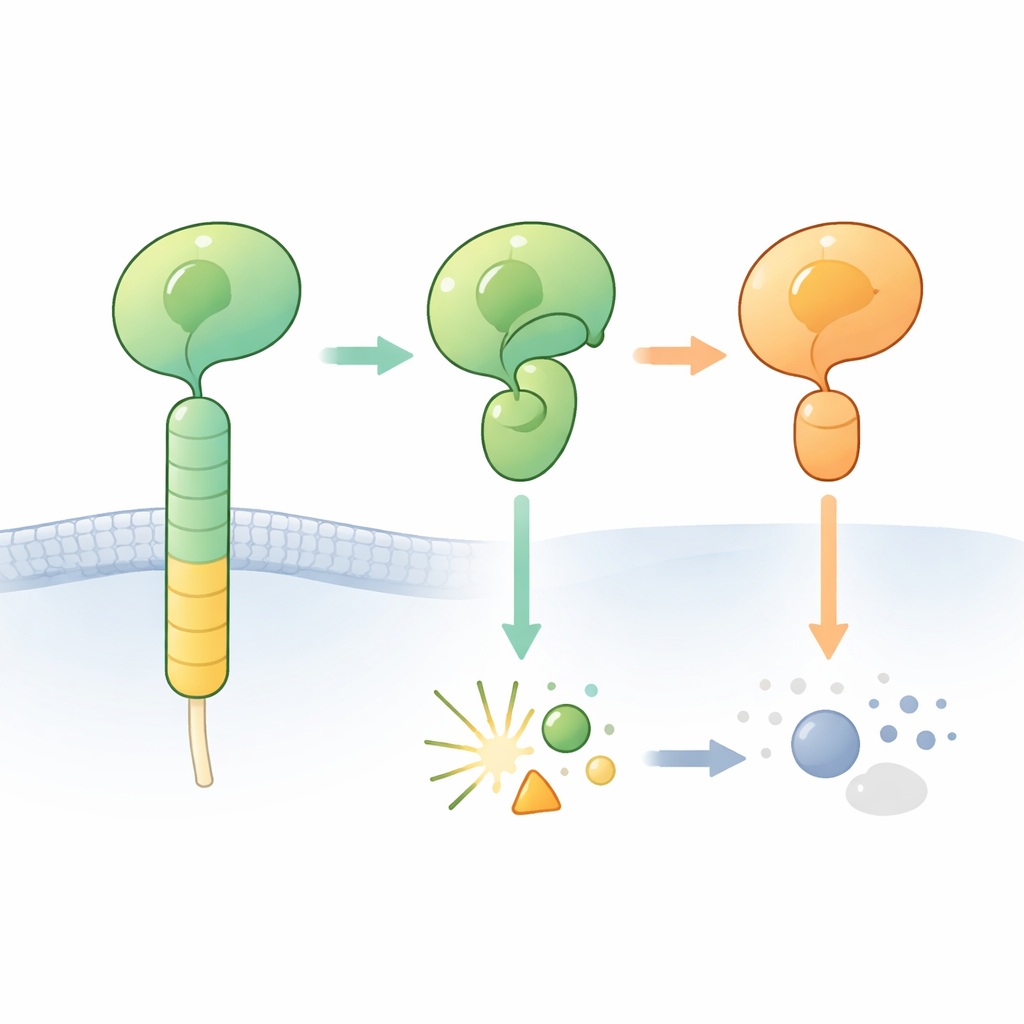
Kiedy oczekiwane cięcie nigdy nie następuje
Naukowcy przyjrzeli się z bliska jednemu receptorowi mózgowemu, ADGRB2 (znanemu też jako BAI2), którego domena GAIN zawiera „właściwy” wzorzec histydyna–leucyna–seryna, ale który dziwnie opiera się rozcięciu. Określili wysokorozdzielczą strukturę krystaliczną regionów przypominających receptory hormonów i domeny GAIN ludzkiego ADGRB2. Ku zaskoczeniu, miejsce cięcia leży w otwartej szczelinie dostępnej dla cząsteczek wody, lecz kluczowe łańcuchy boczne histydyny i seryny są ustawione w sposób niegotowy do reakcji: musiałyby się przekręcić w inne pozycje, by zainicjować reakcję. Podgrzewanie oczyszczonego białka lub dodanie związków chemicznych, które zwykle doprowadzają zatrzymane reakcje samocięcia do końca, nie wywołało rozcięcia, co potwierdza, że ADGRB2 jest naturalnie oporny na cięcie w tych warunkach.
Subtelne interakcje pierścieni kierują chemicznym atakiem
Aby zrozumieć, co sprawia, że inne receptory chętniej się „tną”, zespół porównał ADGRB2 z członkami rodziny, które efektywnie się przecinają, i przeprowadził obszerne symulacje dynamiki molekularnej, pozwalając atomom na komputerowe drgania i przemieszczenia. Wyłoniło się kluczowe spostrzeżenie: w receptorach zdolnych do cięcia histydyna w miejscu cięcia przylega do pobliskiego łańcucha bocznego fenyloalaniny lub tyrozyny w T‑kształtnej interakcji pierścień–pierścień. Delikatne pchnięcie blokuje histydynę w preferowanej orientacji, ustawiając ją tak, by mogła oderwać proton od seryny lub treoniny, przekształcając tę grupę w silnego napastnika wiązania peptydowego. W ADGRB2 fenyloalanina została zastąpiona seryną, a pobliski fragment szkieletu jest zdeformowany przez większy łańcuch boczny, więc histydyna spędza znacznie mniej czasu w pozycji „gotowej do ataku”. Symulacje pokazały też, że w wydajnych tnących receptorach wiązanie peptydowe do zerwania jest często nieco skręcone, co magazynuje naprężenie ułatwiające pęknięcie.
Elastyczne pętle jako regulowane dźwignie
Poza tą interakcją pierścieniową, domena GAIN zawiera luźne regiony pętlowe, czy „klapy”, które otaczają szczelinę cięcia. Te pętle różnią się znacznie między receptorami i nie są silnie zachowane ewolucyjnie, a jednak okazują się kluczowe dla pełnej aktywności. Poprzez wymianę segmentów klap między zwykle zdolnym do cięcia receptorem (ADGRL1) a ADGRB2 autorzy mogli zwiększać lub zmniejszać tempo cięcia. Wprowadzenie reszt przypominających fenyloalaninę we właściwym miejscu przywróciło pewną zdolność samocięcia u zwykle nieaktywnego kuzyna, ADGRB3, zwłaszcza gdy połączono to z histydyną na pozycji katalitycznej. Odwrotnie, mutacja stabilizującej fenyloalaniny w aktywnym receptorze lub przeszczepienie klap przypominających ADGRB2 osłabiło cięcie. Te eksperymenty pokazują, że zarówno precyzyjna lokalna chemia, jak i długie, ruchome pętle współdziałają, aby wypchnąć białko w stan naprężony i reaktywny.
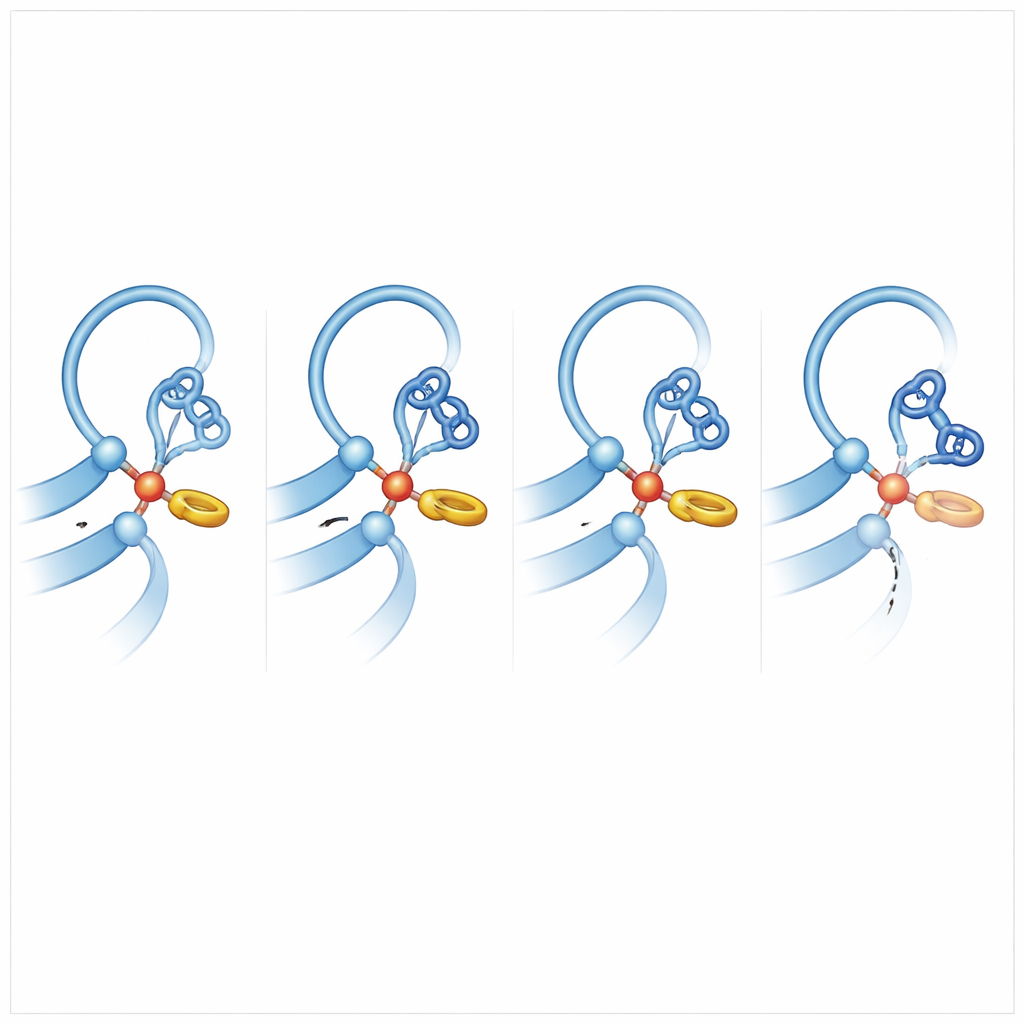
Dlaczego niektóre receptory pozostają nienaruszone
Analizując prawie 150 ssaczych wersji ADGRB2, zespół stwierdził, że większość nie ma idealnej histydyny na miejscu cięcia, a ich klapy i pobliskie reszty są wysoce zmienne. W połączeniu z zmierzoną połówkową trwałością wynoszącą około 100 dni dla cięcia w oczyszczonym ADGRB2 sugeruje to, że wiele receptorów podobnych do BAI2 jest zaprojektowanych tak, by unikać szybkiego samocięcia. Zamiast tego mogą one przekazywać sygnał bez nigdy nie zachodzącego rozcięcia lub przez bardzo wolne bądź kontekstowo zależne cięcie w określonych tkankach. Szerzej rzecz biorąc, praca pokazuje, że samoprzetwarzanie w tych receptorach nie jest prostym przełącznikiem włącz/wyłącz sterowanym trzyliterowym motywem. Raczej wynika z subtelnej równowagi upakowania łańcuchów bocznych, naprężenia szkieletu i ruchomych pętli, które łącznie regulują, czy domena GAIN działa jak wbudowany nóż, czy pozostaje bezpiecznie zablokowana. Zrozumienie tej równowagi może w przyszłości pozwolić badaczom zaprojektować leki przesuwające receptory między stanami stabilnymi a samocięcia, zmieniając sposób, w jaki komórki wyczuwają siły mechaniczne i sygnały chemiczne.
Cytowanie: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
Słowa kluczowe: adhesion GPCR, domena GAIN, autoproteoliza, struktura białka, dynamika molekularna