Clear Sky Science · he
הבסיס המבני של אוטופרוטאוליזה בתחום GAIN ועמידות בפני חיתוך בקולטני ההיצמדות GPCR
איך קולטנים על פני התא פועלים כמו מכונות זעירות שחוצבות את עצמן
תאי הגוף שלנו מכוסים בחלבוני קצה מורכבים החושבים את העולם החיצוני. חלק מהם, שנקראים קולטני G חלבון מסוג היצמדות (adhesion GPCR), מתנהגים כמו מכונות זעירות החוצבות את עצמן: חלק מהחלבון יכול לחתוך את עצמו, ובכך לשנות את האותות שהקולטן משדר. המחקר הזה שואל שאלה שמתרגשת בפשטותה אבל בעלת השלכות רחבות על תפקוד המוח ועיצוב תרופות: מדוע חלק מהקולטנים האלה נוטים לחתוך את עצמם בקלות, בעוד קרובי משפחה קרובים לעיתים קרובות מתנגדות בעקשנות?
מפתח נסתר על קולטני ההיצמדות הדביקים
קולטני G חלבון מסוג היצמדות (aGPCRs) מסייעים לתאים להיצמד לסביבתם ולתקשר עם תאים שכנים. סימן היכר של קולטנים אלה הוא אזור חיצוני מסיבי שכולל את מה שמכונה תחום GAIN. טמון בתוך תחום זה מקטע קצר של "אגוניסט קשור" (tethered agonist) שיכול להפעיל את הקולטן כשהוא נחשף. בהרבה aGPCRs, מקטע זעיר של שרשרת החלבון בתחום ה‑GAIN יכול לחתוך את עצמו בנקודה מסוימת, ולחלק את החלק החיצוני של הקולטן לקטע N‑טרמינלי וקטע C‑טרמינלי. החיתוך קורה לצד רצף בניין מסוים הכולל היסטידין וסרין או תראונין, ונחשב לפעול ככמו סכין כימית פנימית.
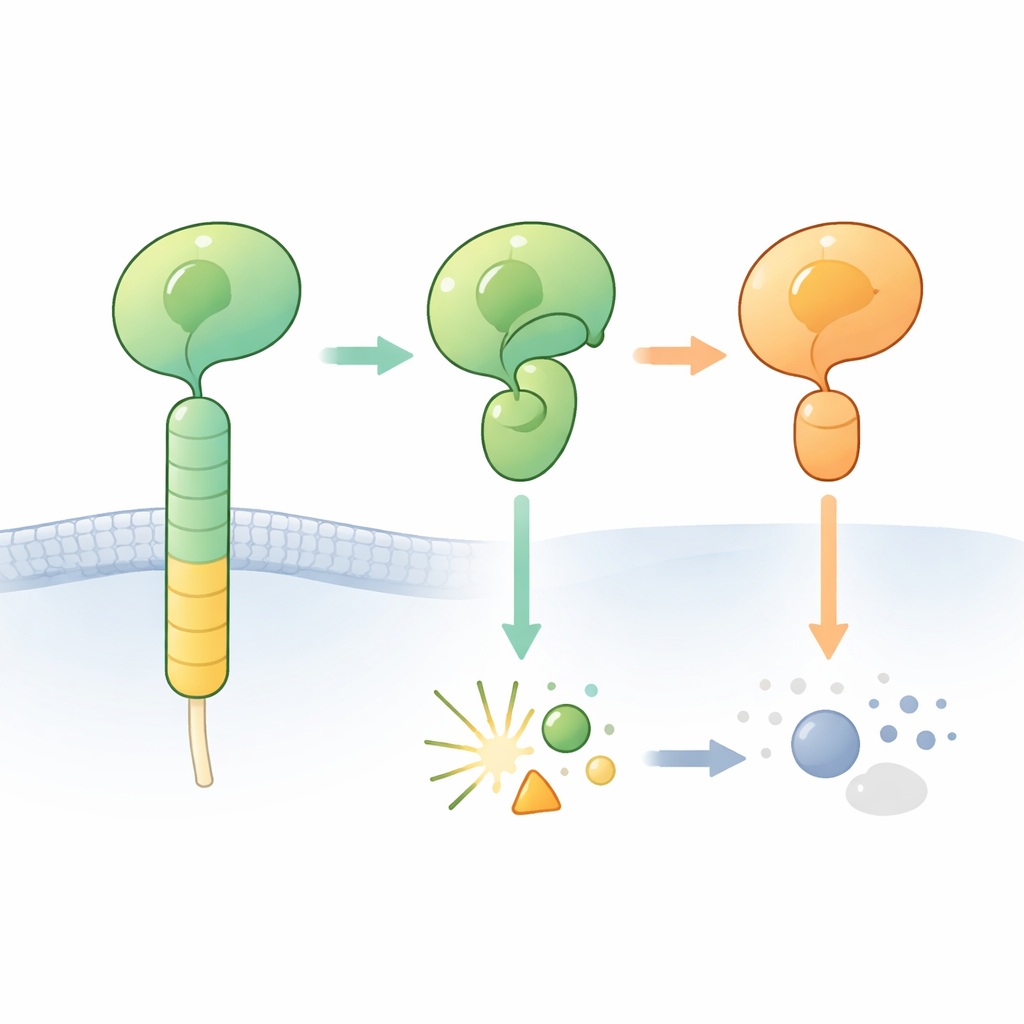
כשלא מתרחש החיתוך הצפוי
החוקרים התמקדותו בקולטן מוח אחד, ADGRB2 (המוכר גם כ‑BAI2), שתחום ה‑GAIN שלו נושא את רצף ההיסטידין–ליאוצין–סרין "הנכון" אך מפתיע בקשיותו להיחתך. הם קבעו מבנה גבישי ברזולוציה גבוהה של אזור הדומה לקולטן הורמונלי ושל תחום ה‑GAIN של ADGRB2 האנושי. באופן מפתיע, אתר החיתוך יושב בתעלה פתוחה שאליה מולקולות מים יכולות להגיע, אך שיירי הצד של ההיסטידין והסרין אינם מכוונים במצב מוכן לכימיה: הם היו צריכים להסתובב לתנוחות שונות כדי להתחיל את התגובה. חימום החלבון המטוהר או הוספת כימיקלים שבדרך כלל דוחפים תגובות אוטו‑חיתוך תקועות להשלמה לא גירו חיתוך, מה שאישר ש‑ADGRB2 עמיד מטבעו לחיתוך בתנאים אלה.
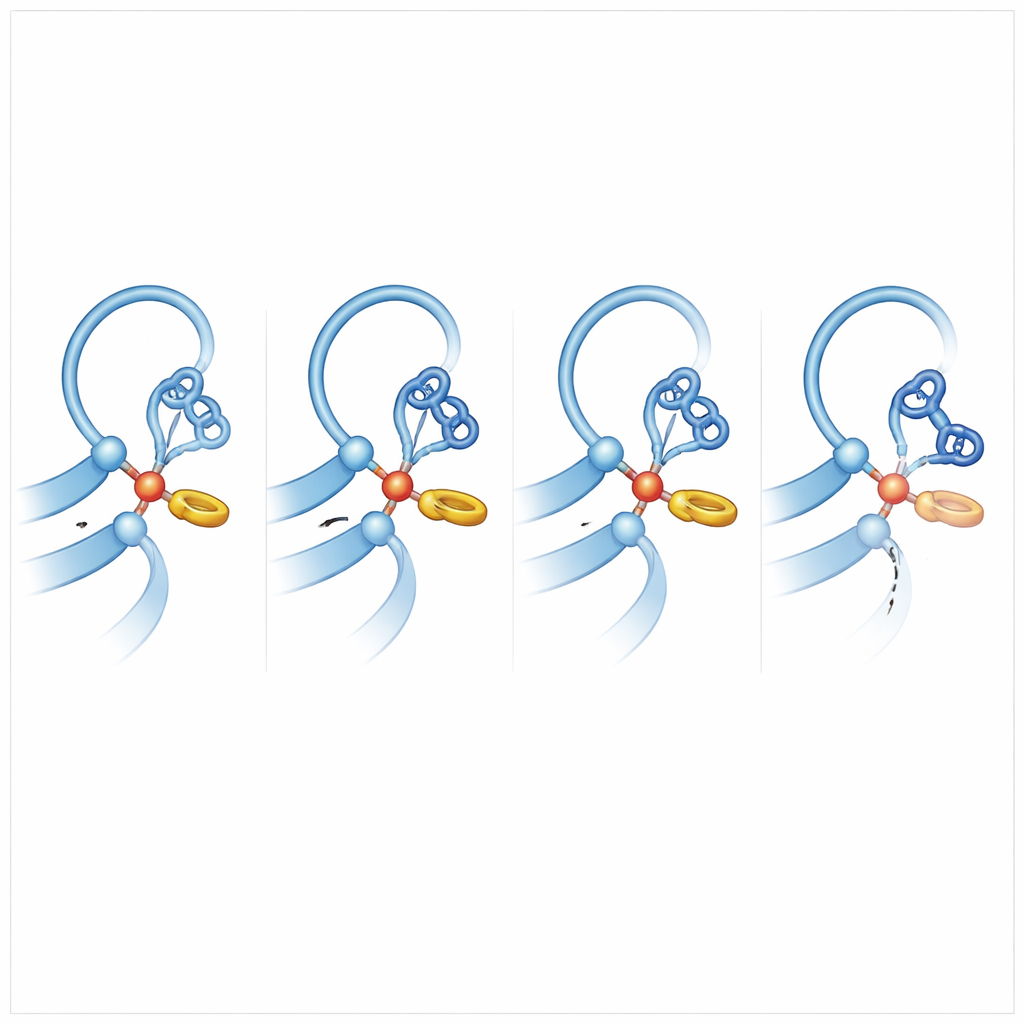
אינטראקציות טבעתיות עדינות מכוונות את המכה הכימית
כדי להבין מה עושה קולטנים אחרים ליותר "מוכנים לחתוך", הקבוצה השוותה את ADGRB2 לחברים במשפחה שמחייבים חיתוך ביעילות והפעילה סימולציות דינמיקת מולקולות נרחבות, שאפשרו לאטומים לזוז ולהתהדר במחשב. תובנה מפתח צצה: בקולטנים המסוגלים לחתוך, ההיסטידין באתר החיתוך יושב כנגד שייר פנילאלאנין או טירוזין סמוך באינטראקציה טבעת‑אל‑טבעת בצורת T. דחיפה עדינה זו ננעלת את ההיסטידין בכיוון מועדף שמיישר אותו כדי לשלוף פרוטון מהסרין או התראונין, מה שהופך את הקבוצה לתוקף חזק של קשר הפפטיד. ב‑ADGRB2, פנילאלאנין זה מוחלף בסרין, ואזור השרשרת הראשית הסמוך מעוות על ידי שייר צד גדול יותר, כך שההיסטידין מבלה הרבה פחות זמן בתנוחת ה"מוכנות־להתקפה". הסימולציות הראו גם שבקולקטני חיתוך יעילים, הקשר הפפטידי שעתיד להישבר לעיתים קרובות מעט מקופל, מאחסן עווית שמקלה על שברו.
לולאות גמישות כמנופי כיוון מתכווננים
מעבר לאינטראקציה הטבעתית הזו, תחום ה‑GAIN מכיל אזורי לולאה רופפים, או "סגרים", שממסגרות את תעלת החיתוך. הלולאות הללו משתנות במידה רבה בין הקולטנים ואינן שמורות בחוזקה באבולוציה, ובכל זאת מתברר שהן חיוניות לפעילות מלאה. על ידי החלפת מקטעי סגרים בין קולטן בדרך כלל מסוגל לחתוך (ADGRL1) לבין ADGRB2, המחברים יכלו לכוונן את קצב החיתוך כלפי מעלה או מטה. הכנסת שיירים דמויי פנילאלאנין במקום המתאים השיבה קצת יכולת חיתוך לקרוב רגיל שהיה בדרך כלל לא פעיל, ADGRB3, במיוחד כשהיא צומדה להיסטידין במיקום הקטליטי. לעומת זאת, מוטציה של פנילאלאנין המייצב בקולטן הפעיל או שתילת סגרים בדומה ל‑ADGRB2 החלישה את החיתוך. הניסויים הללו מראים ששתי רמות — הכימיה המקומית המדויקת ולולאות ארוכות ניידות — משתפות פעולה כדי לדחוף את החלבון למצב מתוח ותגובה.
למה חלק מהקולטנים נשארים שלמים
בהסתכלות על כמעט 150 גרסאות יונקיות של ADGRB2, הקבוצה מצאה שרובם חסרים את ההיסטידין האידיאלי באתר החיתוך, והסגרים והשיירים הסמוכים שלהם משתנים במידה רבה. ביחד עם חצי‑חיים נמדד של כ‑100 ימים לחיתוך ב‑ADGRB2 המטוהר, ממצא זה מציע שרבים מהקולטנים בדמות BAI2 מעוצבים להימנע מחיתוך עצמי מהיר. במקום זאת, הם עשויים לאותת או בלי לחתוך כלל או באמצעות חיתוך איטי מאוד או תלוי‑הקשר ברקמות ספציפיות. באופן רחב יותר, העבודה מראה שעיבוד עצמי בקולטנים אלה אינו מתג דלוק/כבוי פשוט המבוקר על‑ידי רצף תלת‑אותי. במקום זאת, הוא צץ מתוך איזון עדין של אריזת שיירי צד, מתח בשרשרת הראשית ולולאות ניידות, שמכווננים יחד האם תחום ה‑GAIN מתפקד כסכין מובנה או נשאר נעול בבטחה. הבנת האיזון הזה עשויה בסופו של דבר לאפשר לחוקרים לעצב תרופות שמעבירות קולטנים בין מצבים יציבים למצבים חותכים את עצמם, ולשנות את האופן שבו תאים חשים כוחות מכניים ורמזים כימיים.
ציטוט: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
מילות מפתח: adhesion GPCR, תחום GAIN, אוטופרוטאוליזה, מבנה חלבון, דינמיקת מולקולות