Clear Sky Science · ar
الأساس البنيوي للتحلل الذاتي في مجال GAIN ومقاومة الشقوق في مستقبلات الالتصاق المرافقة للبروتين G
كيف تتصرف مستقبلات سطح الخلية مثل آلات صغيرة تقص نفسها
تغطي خلاينا بروتينات مستقبلية معقدة تستشعر العالم الخارجي. بعضها، المسمى مستقبلات الالتصاق المرافقة للبروتين G، يتصرف مثل آلات صغيرة تقص نفسها: قطعة من البروتين يمكن أن تقطع نفسها، مغيرةً طريقة إشارة المستقبل. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكنه ذو تبعات كبيرة لوظيفة الدماغ وتصميم الأدوية: لماذا تقطع بعض هذه المستقبلات نفسها بسهولة بينما تقاوم قريباتها الشديدة الصلة هذه العملية بعناد؟
مفتاح خفي على مستقبلات الخلية اللزجة
تساعد مستقبلات الالتصاق المرافقة للبروتين G (aGPCRs) الخلايا على الالتصاق ببيئتها والتواصل مع الخلايا المجاورة. من سمات هذه المستقبلات وجود منطقة خارجية ضخمة تتضمن ما يسمى مجال GAIN. مخبأ داخل هذا المجال يوجد مقطع قصير «محفز مربوط» يمكنه تشغيل المستقبل عند تعرّضه. في العديد من aGPCRs، يمكن لقسم صغير من سلسلة البروتين في مجال GAIN أن يقطع نفسه عند موقع محدد، مقسماً الجزء الخارجي من المستقبل إلى شظية طرفية N وشظية طرفية C. يحدث القطع بجانب تسلسل بناء محدد يتضمن هيستيدين وسيرين أو ثريونين ويُعتقد أنه يعمل كسكين كيميائي مدمج.
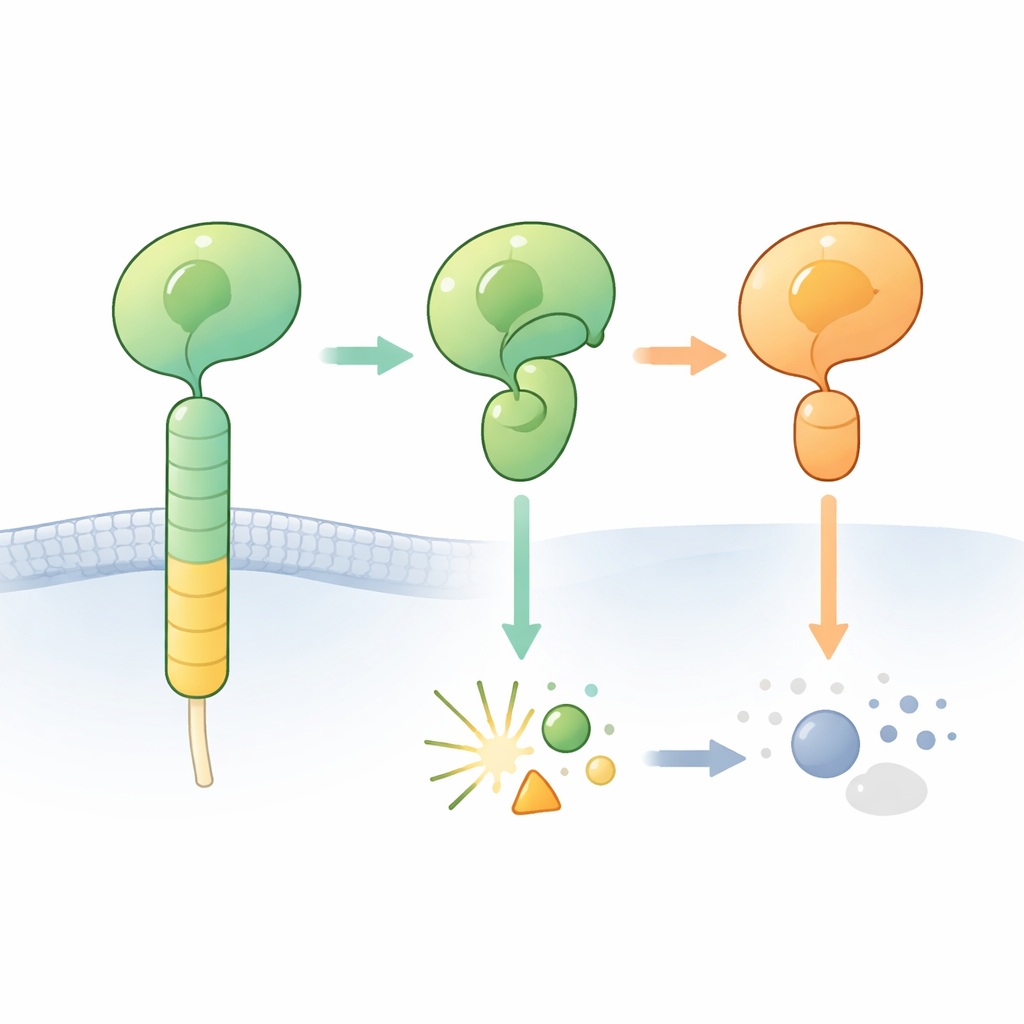
عندما لا يحدث القطع المتوقع
ركز الباحثون على مستقبل دماغي واحد، ADGRB2 (المعروف أيضاً باسم BAI2)، الذي يحمل في مجال GAIN التسلسل «الصحيح» هيستيدين–ليوسين–سيرين لكنه مدهشاً يصعب قطعه. حددوا بنية بلورية عالية الدقة لمناطق مستقبل الهرمون المشابه ومجال GAIN من ADGRB2 البشري. بشكل مفاجئ، يقع موقع القطع في أخدود مفتوح يمكن لجزيئات الماء الوصول إليه، لكن سلاسل جانبيتي الهيستيدين والسيرين مؤذية التوجه بطريقة لا تصلح للتفاعل الكيميائي: كانت بحاجة إلى الانقسام إلى أوضاع مختلفة لبدء التفاعل. تسخين البروتين المنقى أو إضافة مواد كيميائية عادةً ما تدفع تفاعلات التحلل الذاتي المتوقفة إلى الاكتمال لم يحفز القطع، مما يؤكد أن ADGRB2 مقاوم طبيعيًا للقطع تحت هذه الشروط.
تفاعلات حلقية طفيفة توجه الضربة الكيميائية
لفهم ما يجعل مستقبلات أخرى أكثر «ميلًا للقطع»، قارن الفريق ADGRB2 مع أعضاء العائلة التي تقطع بكفاءة وأجرى محاكاة ديناميكا جزيئية واسعة النطاق، متيحين للذرات الارتعاش والتحول على الحاسوب. برزت بصيرة رئيسية: في المستقبلات المؤهلة للقطع، يستقر الهيستيدين عند موقع القطع مقابل سلسلة جانبية لفينيل ألانين أو تيروزين مجاورة في تفاعل حلقي بشكل حرف T. هذه الدفعَة اللطيفة تثبت الهيستيدين في اتجاه مفضّل يوافقه ليقتلع بروتونًا من السيرين أو الثريونين، محولاً تلك المجموعة إلى مهاجم قوي للرابطة الببتيدية. في ADGRB2، استبدل هذا الفينيل ألانين بسيرين، والمنطقة العظمية القريبة مشوهة بسلسلة جانبية أكثر ضخامًة، لذا يقضي الهيستيدين وقتًا أقل بكثير في الوضع «الجاهز للهجوم». أظهرت المحاكاة أيضًا أن الرابطة الببتيدية المراد كسرها في القاطعين الفعّالين غالبًا ما تكون ملتوية قليلاً، مخزّنة توتراً يجعل كسرها أسهل.
حلقات مرنة كرافعات قابلة للضبط
بعيدًا عن هذا التفاعل الحلقي، يحتوي مجال GAIN على مناطق حلقية مرنة، أو «أغطية»، تؤطر أخدود القطع. تختلف هذه الحلقات على نطاق واسع بين المستقبلات وليست محفوظة بقوة عبر التطور، ومع ذلك تبين أنها حاسمة للنشاط الكامل. من خلال تبديل مقاطع الأغطية بين مستقبل عادةً ما يكون مؤهلاً للقطع (ADGRL1) وADGRB2، تمكن المؤلفون من رفع أو خفض معدلات القطع. إدخال بقايا شبيهة بالفينيل ألانين في المكان الصحيح أعاد بعض القدرة على القطع لقرين عادة غير نشط، ADGRB3، خاصةً عند الجمع مع هيستيدين في الموقع التحفيزي. بالمقابل، أدى تحوير الفينيل ألانين المثبت في المستقبل النشط أو زرع أغطية شبيهة بـ ADGRB2 إلى إضعاف القطع. تبيّن هذه التجارب أن الكيمياء المحلية الدقيقة والحلقات الطويلة المتحركة تتعاون لدفع البروتين إلى حالة متوترة وتفاعلية.
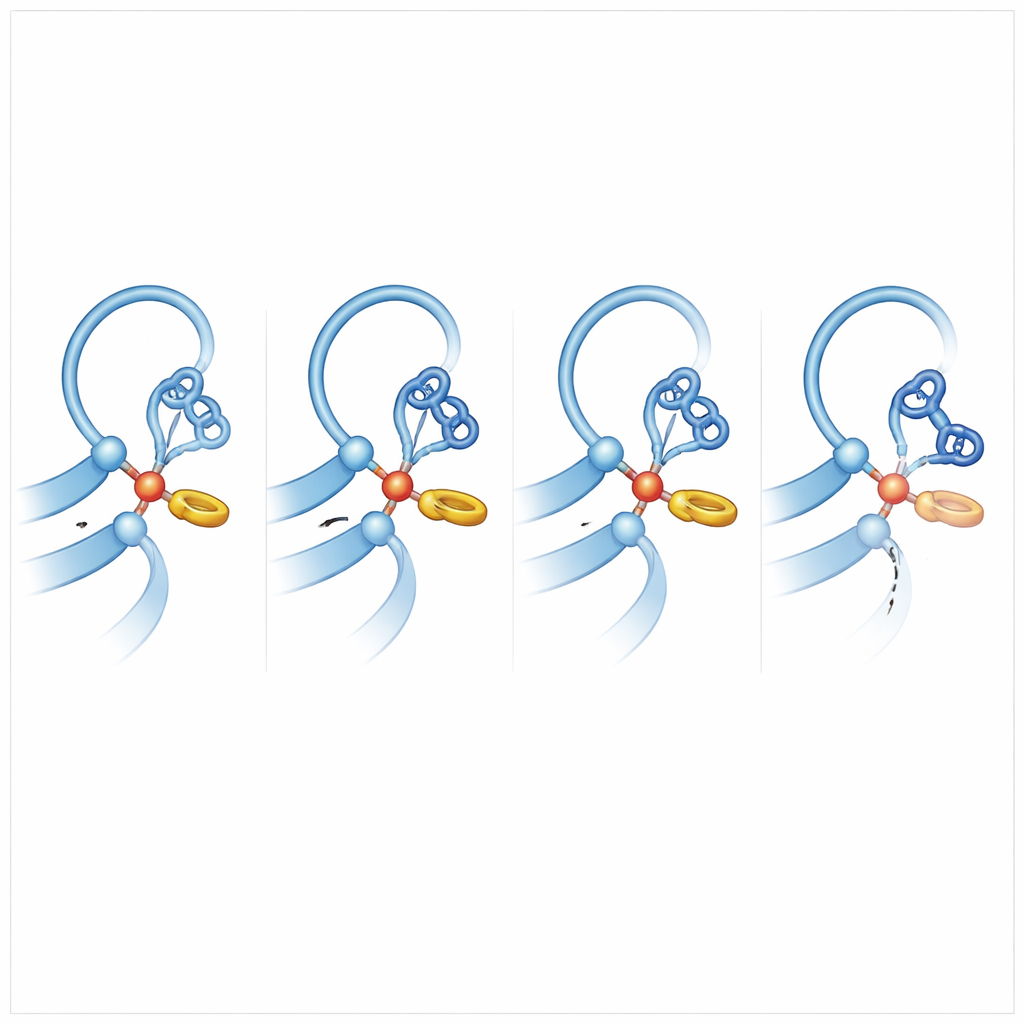
لماذا تبقى بعض المستقبلات سليمة
عند النظر عبر ما يقرب من 150 نسخة ثديية من ADGRB2، وجد الفريق أن معظمها يفتقر إلى الهيستيدين المثالي في موقع القطع، وأن أغطيتها والبقايا القريبة متقلبة للغاية. إلى جانب نصف العمر المقاس بحوالي 100 يوم للقطع في ADGRB2 المنقى، يشير هذا إلى أن العديد من مستقبلات شبيهة BAI2 مصممة لتجنب التحلل الذاتي السريع. بدلاً من ذلك، قد تشير إشاراتها إما دون أي قطع على الإطلاق أو عبر قطعٍ بطيء جدًا أو معتمد على السياق في أنسجة محددة. وعلى نحو أوسع، تُظهر هذه الدراسة أن المعالجة الذاتية في هذه المستقبلات ليست مفتاح تشغيل/إيقاف بسيطًا تسيطر عليه ثلاثية حرفية. بل إنها تنبثق من توازن دقيق بين حزم سلاسل جانبية، إجهاد العمود الفقري وحلقات متحركة تضبط جماعياً ما إذا كان مجال GAIN يعمل كسكين مدمج أو يظل مقفلًا بأمان. قد يتيح فهم هذا التوازن للباحثين في نهاية المطاف تصميم أدوية تغير مستقبلات بين حالات مستقرة وحالات تقص ذاتيًا، مغيرةً طريقة استشعار الخلايا للقوى الميكانيكية والإشارات الكيميائية.
الاستشهاد: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
الكلمات المفتاحية: مستقبلات GPCR الالتصاقية, مجال GAIN, التحلل الذاتي, بنية البروتين, ديناميكا جزيئية