Clear Sky Science · de
Strukturelle Grundlage der Autoproteolyse des GAIN-Domänen und der Spaltungsresistenz bei Adhesions-G-Protein-gekoppelten Rezeptoren
Wie Zelloberflächenrezeptoren wie winzige Selbstschneidemaschinen funktionieren
Unsere Zellen sind mit komplexen Rezeptorproteinen überzogen, die die Außenwelt wahrnehmen. Einige davon, als Adhesions-G-Protein-gekoppelte Rezeptoren bezeichnet, verhalten sich wie winzige Selbstschneidemaschinen: ein Teil des Proteins kann sich selbst zerschneiden und dadurch die Signalgebung des Rezeptors verändern. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage für Hirnfunktion und Wirkstoffdesign: Warum schneiden sich einige dieser Rezeptoren bereitwillig, während eng verwandte Rezeptoren hartnäckig widerstehen?
Ein verborgener Schalter an klebenden Zellrezeptoren
Adhesions-G-Protein-gekoppelte Rezeptoren (aGPCRs) helfen Zellen, an ihrer Umgebung zu haften und mit Nachbarzellen zu kommunizieren. Ein Kennzeichen dieser Rezeptoren ist eine voluminöse Außendomäne, die die sogenannte GAIN-Domäne enthält. Versteckt in dieser Domäne liegt ein kurzes „tethered agonist“-Segment, das den Rezeptor aktivieren kann, wenn es freigelegt wird. In vielen aGPCRs kann ein winziger Abschnitt der Proteinkette in der GAIN-Domäne an einer spezifischen Stelle selbst schneiden und so den äußeren Teil des Rezeptors in ein N-terminales und ein C-terminales Fragment teilen. Der Schnitt findet neben einer bestimmten Aminosäuresequenz statt, die ein Histidin und eine Serin- oder Threonin-Rest enthält und als eingebautes chemisches Messer wirken soll.
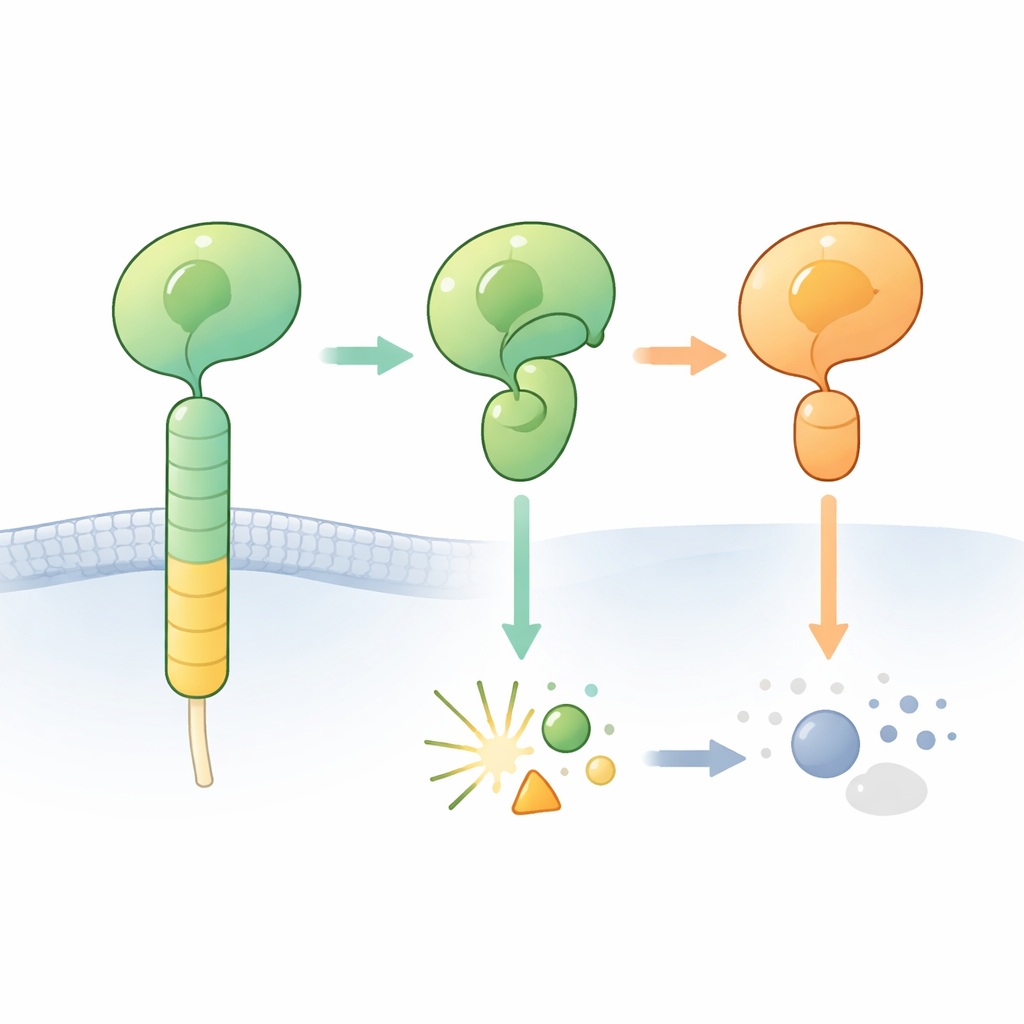
Wenn der erwartete Schnitt nie passiert
Die Forscher fokussierten sich auf einen Hirnrezeptor, ADGRB2 (auch bekannt als BAI2), dessen GAIN-Domäne die „richtige“ Histidin‑Leucin‑Serin-Sequenz trägt, der aber bemerkenswerterweise schwer zu spalten ist. Sie bestimmten eine hochaufgelöste Kristallstruktur der hormonrezeptorähnlichen und GAIN-Regionen von menschlichem ADGRB2. Überraschenderweise liegt die Spaltstelle in einer offenen Rinne, die von Wassermolekülen zugänglich ist, doch die Seitenketten des entscheidenden Histidins und Serins sind in einer Orientierung angeordnet, die chemisch nicht einsatzbereit ist: Für die Reaktion müssten sie in andere Positionen drehen. Erhitzen des gereinigten Proteins oder Zugabe von Chemikalien, die normalerweise festgefahrene Selbstspaltungsreaktionen vollenden, lösten keine Spaltung aus, was bestätigt, dass ADGRB2 unter diesen Bedingungen natürlicherweise spaltungsresistent ist.
Fein abgestimmte Ring‑Interaktionen lenken den chemischen Schlag
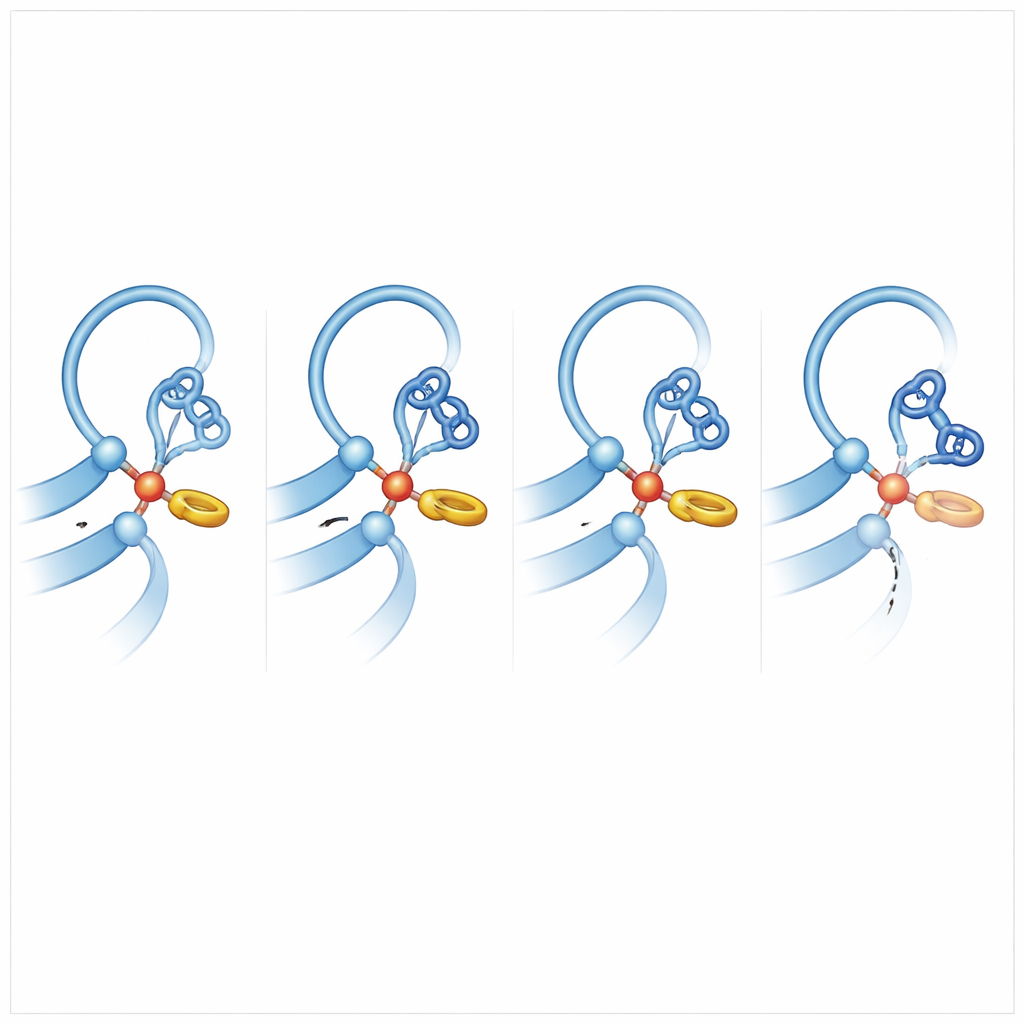
Um zu verstehen, was andere Rezeptoren „schnittfreudiger“ macht, verglich das Team ADGRB2 mit Familienmitgliedern, die effizient spalten, und führte umfangreiche Simulationen molekularer Dynamik durch, bei denen die Atome am Computer herumwackeln und sich verschieben. Ein zentrales Ergebnis war: In spaltfähigen Rezeptoren liegt das Histidin an der Spaltstelle eingekeilt an einer benachbarten Phenylalanin- oder Tyrosin-Seitenkette in einer T‑förmigen Ring‑zu‑Ring-Interaktion. Dieser sanfte Anschub verriegelt das Histidin in einer bevorzugten Orientierung, die es ausrichtet, um ein Proton vom Serin oder Threonin abzuziehen und diese Gruppe so in einen starken Angreifer auf die Peptidbindung zu verwandeln. In ADGRB2 ist dieses Phenylalanin durch ein Serin ersetzt, und der nahegelegene Rückgratbereich ist durch eine voluminösere Seitenkette verzerrt, sodass das Histidin viel weniger Zeit in der „angriffsbereiten“ Pose verbringt. Simulationen zeigten außerdem, dass in effizienten Schneidern die zu brechende Peptidbindung oft leicht verdreht ist und so Spannung speichert, die das Aufbrechen erleichtert.
Flexible Schleifen als einstellbare Hebel
Über diese Ring‑Interaktion hinaus enthält die GAIN-Domäne flexible Schleifenregionen, oder „Lappen“, die die Spaltrinne umrahmen. Diese Schleifen variieren stark zwischen Rezeptoren und sind evolutionär nicht stark konserviert, erweisen sich jedoch als entscheidend für volle Aktivität. Durch Austausch von Lappenabschnitten zwischen einem normalerweise spaltfähigen Rezeptor (ADGRL1) und ADGRB2 konnten die Autoren die Spaltungsraten hoch- oder herunterregeln. Das Einführen von Phenylalanin‑ähnlichen Resten an der richtigen Stelle stellte einer normalerweise inaktiven Verwandten, ADGRB3, teilweise die Selbstspaltungsfähigkeit wieder her, besonders in Kombination mit einem Histidin an der katalytischen Position. Umgekehrt schwächten Mutationen des stabilisierenden Phenylalanins im aktiven Rezeptor oder das Einpflanzen von ADGRB2‑ähnlichen Lappen die Spaltung. Diese Experimente zeigen, dass sowohl die präzise lokale Chemie als auch lange, bewegliche Schleifen zusammenwirken, um das Protein in einen gespannt reaktiven Zustand zu bringen.
Warum einige Rezeptoren intakt bleiben
Beim Vergleich von nahezu 150 säugetierspezifischen Varianten von ADGRB2 stellte das Team fest, dass die meisten nicht das ideale Histidin an der Spaltstelle tragen und ihre Lappen sowie benachbarten Reste stark variabel sind. Zusammen mit der gemessenen Halbwertszeit von etwa 100 Tagen für die Spaltung im gereinigten ADGRB2 legt dies nahe, dass viele BAI2‑ähnliche Rezeptoren darauf ausgelegt sind, schnelle Selbstspaltung zu vermeiden. Stattdessen könnten sie entweder ohne jemals zu spalten signalisieren oder sehr langsame bzw. kontextabhängige Spaltung in bestimmten Geweben nutzen. Allgemeiner zeigt die Arbeit, dass die Selbstverarbeitung in diesen Rezeptoren kein einfacher Ein‑/Aus‑Schalter ist, der von einem drei‑Buchstaben‑Motiv kontrolliert wird. Vielmehr ergibt sie sich aus einem empfindlichen Gleichgewicht von Seitenkettenpackung, Rückgratspannung und mobilen Schleifen, die gemeinsam einstellen, ob die GAIN‑Domäne als eingebautes Messer wirkt oder sicher verriegelt bleibt. Das Verständnis dieses Gleichgewichts könnte letztlich Forschern erlauben, Wirkstoffe zu entwerfen, die Rezeptoren zwischen stabilen und selbstspaltenden Zuständen verschieben und damit verändern, wie Zellen mechanische Kräfte und chemische Signale wahrnehmen.
Zitation: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
Schlüsselwörter: adhäsions-GPCR, GAIN-Domäne, Autoproteolyse, Proteinstruktur, molekulare Dynamik