Clear Sky Science · ja
接着Gタンパク質共役受容体におけるGAINドメイン自己切断の構造基盤と切断抵抗性
細胞表面受容体が小さな自己切断装置のように働く仕組み
私たちの細胞表面には外界を感知する複雑な受容体タンパク質が並んでいます。そのうちの一群、接着型Gタンパク質共役受容体(aGPCR)は、小さな自己切断機のように振る舞います:タンパク質の一部が自身を切断し、受容体のシグナル伝達様式を変えます。本研究は一見単純だが脳機能や創薬に大きな示唆を与える問いを扱います:なぜ類縁の受容体でも、あるものは容易に自己切断する一方で、近縁でも頑強に切断に抵抗するのか?
粘着性のある細胞受容体に潜むスイッチ
接着型Gタンパク質共役受容体(aGPCR)は、細胞が周囲に付着したり近隣の細胞と情報をやり取りしたりするのを助けます。これら受容体の特徴は、いわゆるGAINドメインを含む大型の外部領域です。このドメインの内部には短い「テザードアゴニスト」断片が埋め込まれており、露出すると受容体をオンにするスイッチとして働きます。多くのaGPCRでは、GAINドメイン内のタンパク質鎖の小さな部分が特定の部位で自己切断し、受容体の外側領域をN末端とC末端の断片に分割します。切断はヒスチジンとセリンまたはスレオニンを含む特定の残基配列の隣で起こり、この配列が内蔵の化学的なナイフとして機能すると考えられています。
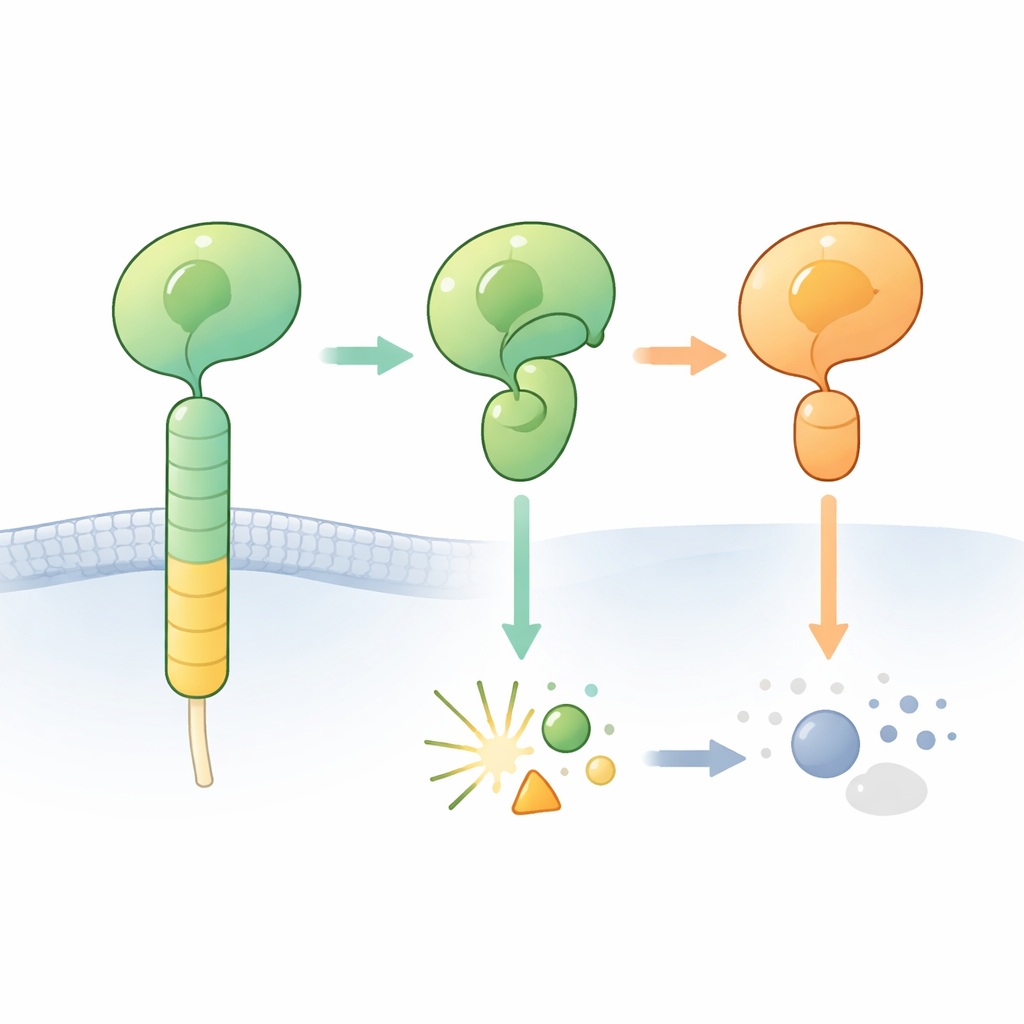
期待される切断が起きないとき
研究者らは脳に発現する一つの受容体、ADGRB2(別名BAI2)に注目しました。この受容体のGAINドメインは“適切な”ヒスチジン–ロイシン–セリン配列を持つにもかかわらず、興味深いことに切断されにくい性質を示します。彼らはヒトADGRB2のホルモン受容体様領域とGAIN領域の高解像度結晶構造を決定しました。驚くべきことに、切断部位は水分子が到達できる開いた溝に位置していましたが、鍵となるヒスチジンとセリンの側鎖は化学反応に適した配向にはなっておらず、反応を始めるには別の位置に回転する必要がありました。精製タンパク質を加熱したり、停滞した自己切断反応を通常完了に導く化学薬品を加えたりしても切断は誘導されず、これによりADGRB2がこれらの条件下で自然に切断抵抗性であることが確認されました。
微妙な芳香環相互作用が化学的攻撃を導く
他の受容体がなぜより“切りやすい”のかを理解するため、チームはADGRB2を効率的に切断するファミリーのメンバーと比較し、大規模な分子動力学シミュレーションを行って原子の揺らぎを観察しました。重要な洞察が得られました:切断が可能な受容体では、切断部位のヒスチジンが近傍のフェニルアラニンまたはチロシンの側鎖に対してT字型の芳香環-芳香環相互作用で寄り添っています。この穏やかな押し込みがヒスチジンを好ましい配向に固定し、ヒスチジンがセリンやスレオニンからプロトンを引き抜いて、それらをペプチド結合を攻撃する強力な求核剤に変えるように並べます。ADGRB2ではこのフェニルアラニンがセリンに置換され、近接する主鎖領域もよりかさばる側鎖によって歪んでいるため、ヒスチジンは“攻撃準備”の姿勢をとる時間がはるかに短くなります。さらにシミュレーションは、効率的に切断する受容体では切断されるべきペプチド結合がややねじれていて、そのひずみが切断を容易にすることを示しました。
可撓性のあるループは調整可能なレバー
この芳香環相互作用に加え、GAINドメインには切断溝を取り囲む可動性の高いループ領域、いわゆる「フラップ」が存在します。これらのループは受容体間で大きく異なり進化的にも強く保存されていませんが、完全な活性のために重要であることが判明しました。通常は切断能を持つ受容体(ADGRL1)とADGRB2との間でフラップ断片を交換すると、切断速度を上下に調節できました。適切な位置にフェニルアラニン様残基を導入すると、本来不活性な近縁体ADGRB3にいくらか自己切断能を回復させられ、特に触媒位置にヒスチジンを併せて導入した場合に顕著でした。逆に、活性受容体の安定化フェニルアラニンを変異させたりADGRB2様のフラップを移植したりすると切断は弱まりました。これらの実験は、精密な局所化学と長く可動なループが協調してタンパク質をひずみのかかった反応性の高い状態に押し込むことを示しています。
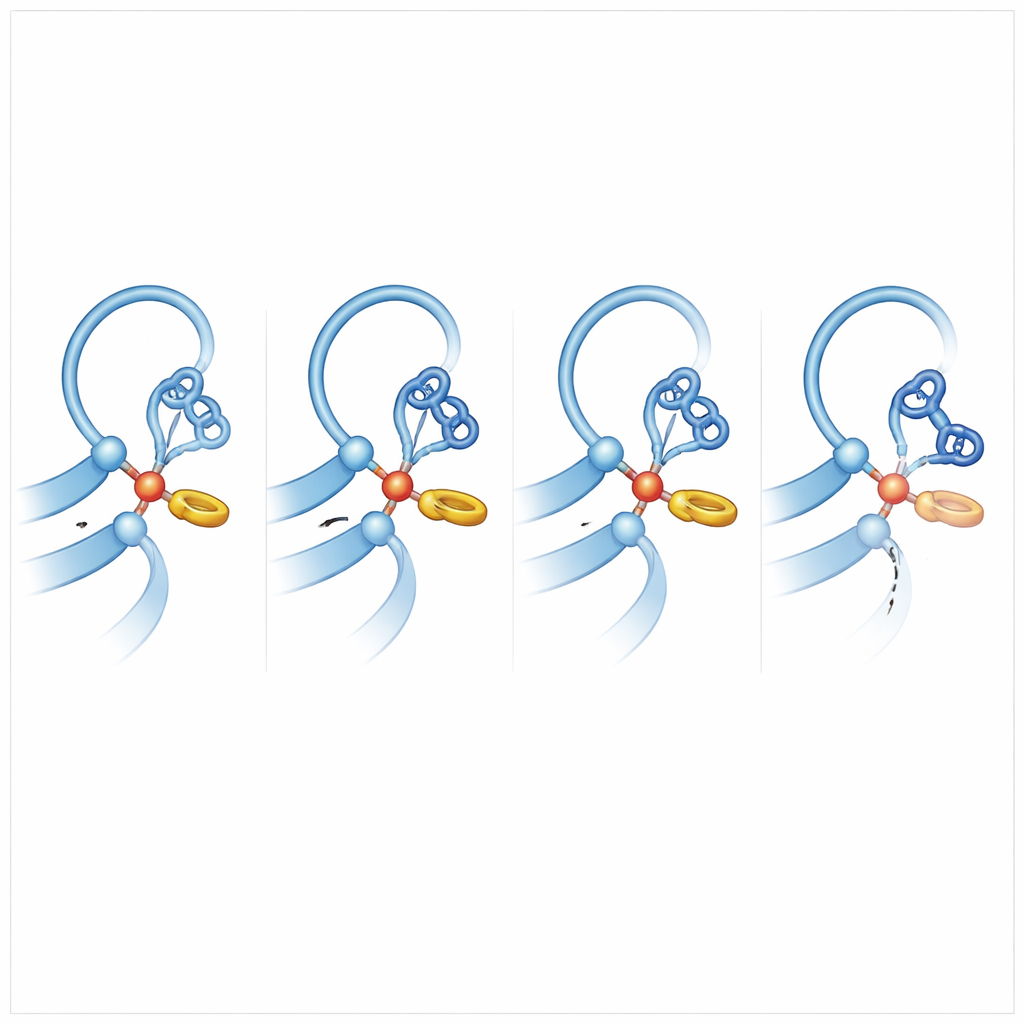
なぜ一部の受容体は無傷のままでいるのか
約150種の哺乳類版ADGRB2を調べると、多くが切断部位に理想的なヒスチジンを欠き、フラップや近傍の残基も非常に多様であることが分かりました。精製されたADGRB2の切断の半減期が約100日であるという測定と合わせると、多くのBAI2様受容体は急速な自己切断を避けるように設計されていることが示唆されます。代わりに、これらは一度も切断せずにシグナルを送るか、特定の組織で非常に遅いあるいは文脈依存的な切断を用いる可能性があります。より広く見れば、これら受容体の自己処理は三文字のモチーフで単純にオン・オフが切り替わるものではなく、副鎖の詰まり方、主鎖のひずみ、可動ループという微妙な均衡から生じ、GAINドメインが内蔵のナイフとして働くか安全にロックされたままでいるかを調節しています。この均衡の理解は、最終的に受容体を安定な状態と自己切断状態の間で切り替える薬剤を設計し、細胞が機械的力や化学的手がかりを感知する仕方を変えることにつながるかもしれません。
引用: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
キーワード: 接着型GPCR, GAINドメイン, 自己切断, タンパク質構造, 分子動力学