Clear Sky Science · sv
Strukturella grunder för GAIN-domänens autoproteolys och klyvningsmotstånd i adhesions G‑proteinkopplade receptorer
Hur cellmembranreceptorer fungerar som små självklingande maskiner
Våra celler är täckta av förgrenade receptorproteiner som känner av omvärlden. Några av dessa, så kallade adhesions G‑proteinkopplade receptorer, beter sig som små självskärande maskiner: en del av proteinet kan skära av sig självt och därigenom förändra hur receptorn signalerar. Denna studie ställer en bedrägligt enkel fråga med stora följder för hjärnfunktion och läkemedelsdesign: varför skär sig vissa av dessa receptorer lätt, medan nära besläktade receptorer envist motstår?
En dold brytare på klibbiga cellreceptorer
Adhesions G‑proteinkopplade receptorer (aGPCRs) hjälper celler att fästa mot omgivningen och kommunicera med grannceller. Ett kännetecken för dessa receptorer är en skrymmande yttre region som inkluderar den så kallade GAIN‑domänen. Inuti denna domän ligger ett kort ”tethered agonist”-segment som kan aktivera receptorn när det exponeras. I många aGPCRs kan en liten sektion av proteinkedjan i GAIN‑domänen skära sig vid en specifik plats och dela receptorens yttre del i en N‑terminal och en C‑terminal fragment. Klyvningen sker intill en viss aminosyraföljd som inkluderar en histidin och en serin eller treonin och tros fungera som en inbyggd kemisk kniv.
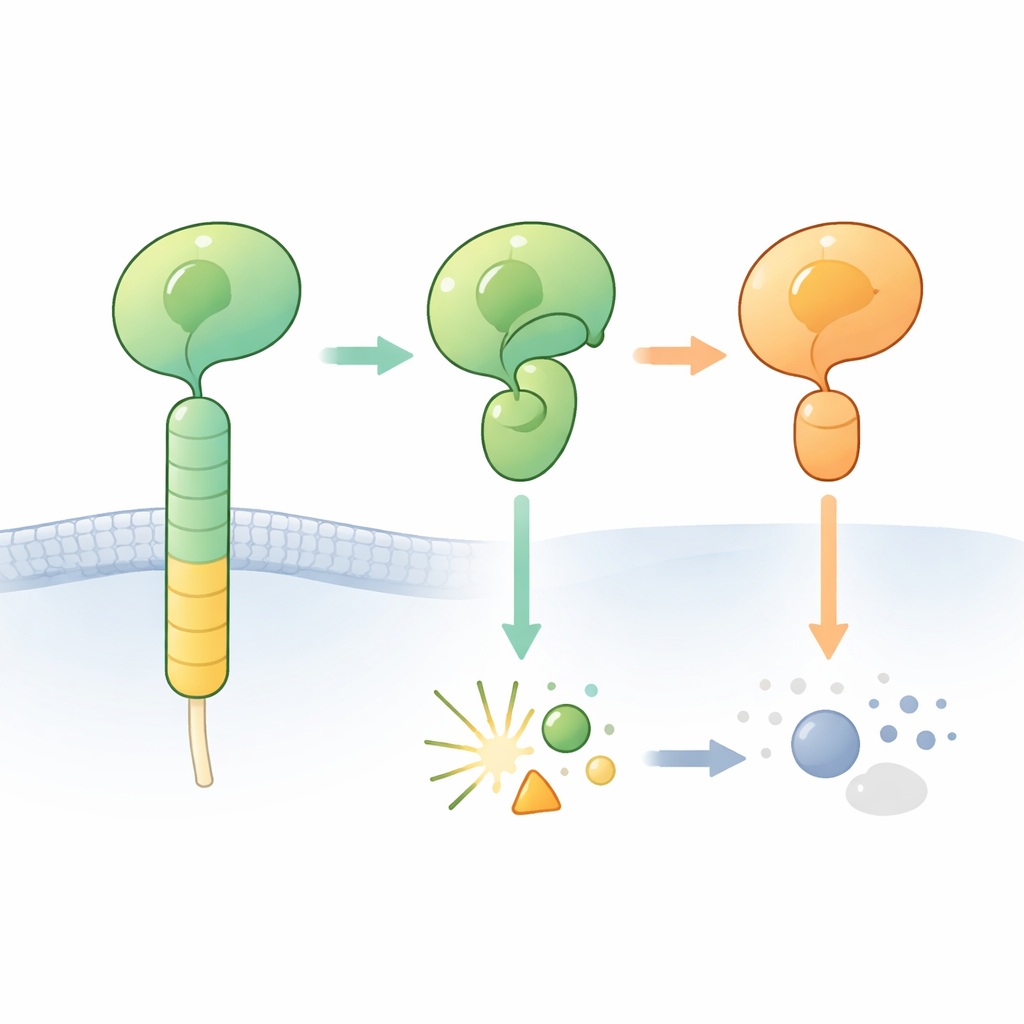
När den väntade klyvningen aldrig inträffar
Forskarna zoomade in på en hjärnreceptor, ADGRB2 (också kallad BAI2), vars GAIN‑domän bär den ”rätta” histidin‑leucin‑serin‑sekvensen men som påfallande nog är svårklyvd. De bestämde en högupplöst kristallstruktur av den hormonreceptorliknande och GAIN‑regionen från mänskligt ADGRB2. Överraskande nog ligger klyvningsstället i en öppen fåra som vattenmolekyler kan nå, men de centrala histidin‑ och serinsidokedjorna är orienterade på ett sätt som inte är redo för kemi: de skulle behöva vrida sig till andra positioner för att initiera reaktionen. Upphettning av det renade proteinet eller tillsats av kemikalier som normalt driver på ofullbordade självskärningsreaktioner ledde inte till klyvning, vilket bekräftar att ADGRB2 är naturligt motståndskraftigt mot klyvning under dessa förhållanden.
Subtila ringinteraktioner styr det kemiska anfallet
För att förstå vad som gör andra receptorer mer ”skär‑benägna” jämförde teamet ADGRB2 med familjemedlemmar som klyver effektivt och körde omfattande molekylärdynamiksimuleringar där atomerna fick skaka och ompositionera sig i datorn. En nyckelinsikt framträdde: i klyvningskompetenta receptorer vilar histidinen vid klyvningsstället mot en närliggande fenylalanin‑ eller tyrosinsidokedja i en T‑formad ring‑mot‑ring‑interaktion. Denna mjuka knuff låser histidinen i en föredragen orientering som ställer den för att avdra en proton från serinen eller treoninen, och förvandla den gruppen till en kraftfull angripare av peptidbindningen. I ADGRB2 har denna fenylalanin ersatts av en serin, och ryggradsregionen i närheten är förvriden av en mer skrymmande sidokedja, så histidinen spenderar mycket mindre tid i den ”attack‑redo” positionen. Simuleringarna visade också att i effektiva klyvare är peptidbindningen som ska brytas ofta något vriden och lagrar spänning som gör den lättare att knäcka.
Flexibla slingor som justerbara hävstänger
Bortom denna ringinteraktion innehåller GAIN‑domänen lösa slingregioner, eller ”flikar”, som ramar in klyvningsfåran. Dessa slingor varierar mycket mellan receptorer och är inte starkt konservativa evolutionärt, men de visar sig vara avgörande för full aktivitet. Genom att byta flap‑segment mellan en normalt klyvningskompetent receptor (ADGRL1) och ADGRB2 kunde författarna justera klyvningshastigheterna upp eller ner. Införande av fenylalaninliknande rester på rätt ställe återställde viss självskärande förmåga hos en normalt inaktiv kusin, ADGRB3, särskilt när det kombinerades med en histidin på den katalytiska positionen. Omvänt försvagade mutation av den stabiliserande fenylalaninen i den aktiva receptorn eller inplantering av ADGRB2‑lika flikar klyvningen. Dessa experiment visar att såväl precis lokal kemi som långa, rörliga slingor samarbetar för att pressa proteinet in i ett spänt, reaktivt tillstånd.
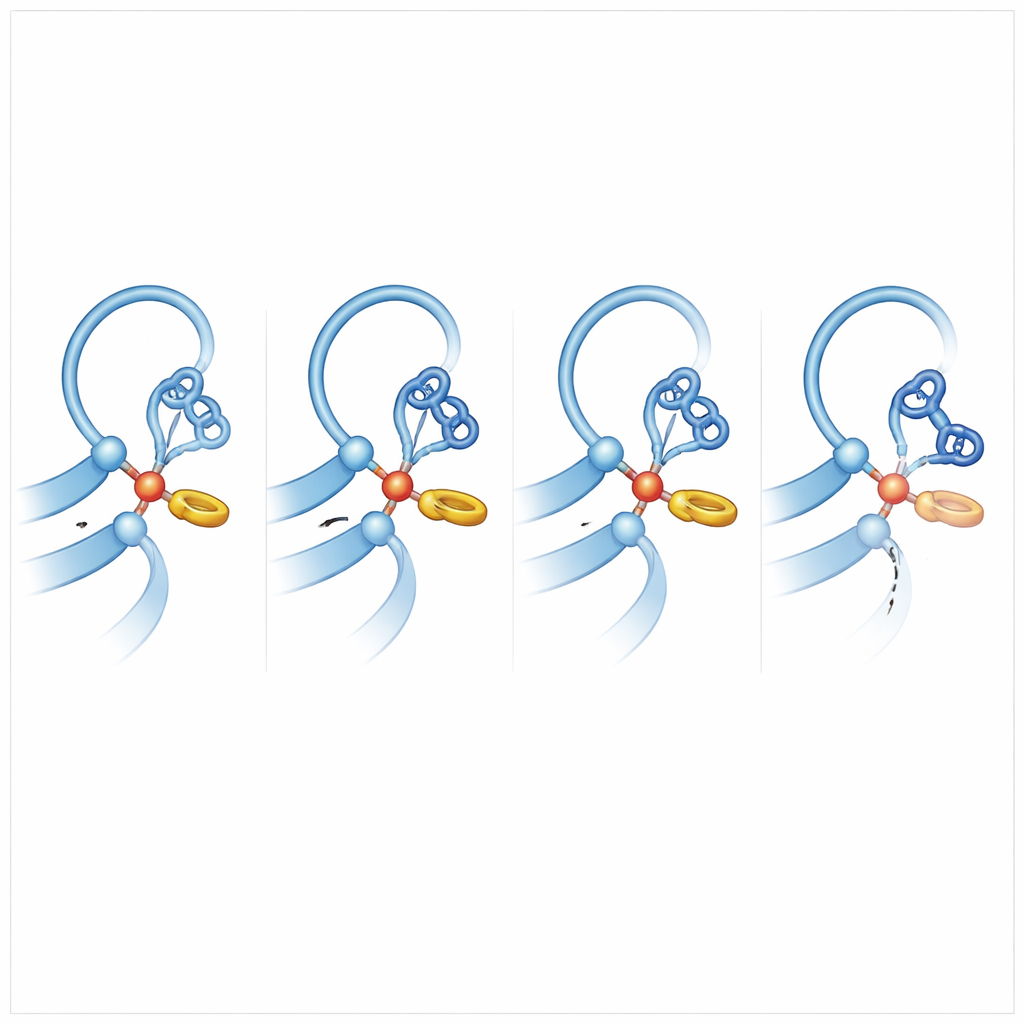
Varför vissa receptorer förblir intakta
Genom att titta över nästan 150 däggdjursversioner av ADGRB2 fann teamet att de flesta saknar den ideala histidinen vid klyvningsstället, och deras flikar och närliggande rester är mycket varierande. Tillsammans med den uppmätta halveringstiden på cirka 100 dagar för klyvning i renat ADGRB2 antyder detta att många BAI2‑lika receptorer är byggda för att undvika snabb självklyvning. Istället kan de signalera antingen utan att någonsin klyvas eller genom att använda mycket långsam eller kontextberoende klyvning i specifika vävnader. Mer allmänt visar arbetet att självbearbetning i dessa receptorer inte är en enkel av/på‑brytare som styrs av en tre‑bokstavs‑motif. Snarare uppstår den ur en fin balans mellan sidokedjepackning, ryggradsspänning och rörliga slingor som gemensamt ställer in om GAIN‑domänen fungerar som en inbyggd kniv eller förblir säkert låst. Att förstå denna balans kan så småningom göra det möjligt för forskare att designa läkemedel som skiftar receptorer mellan stabila och självskärande tillstånd, och därigenom förändrar hur celler känner mekaniska krafter och kemiska signaler.
Citering: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
Nyckelord: adhesions‑GPCR, GAIN‑domän, autoproteolys, proteinstruktur, molekylär dynamik