Clear Sky Science · tr
Yapışma G‑protein bağlantılı reseptörlerde GAIN domaininin oto‑proteolizi ve kesilmeye dirençlilik yapısal temeli
Hücre Yüzeyi Reseptörleri Nasıl Küçük Kendi Kendini Kesme Makineleri Gibi Davranır
Hücresel yüzeyimiz, dış dünyayı algılayan karmaşık reseptör proteinleriyle kaplıdır. Bunlardan bazıları, yapışma G protein‑bağlantılı reseptörler (aGPCR'ler) olarak adlandırılır ve küçük kendi kendini kesen makineler gibi davranır: proteinin bir parçası kendini keserek reseptörün sinyal verme biçimini değiştirir. Bu çalışma, beyin işlevi ve ilaç tasarımı açısından büyük çıkarımlara sahip gibi görünen aldatıcı derecede basit bir soruyu gündeme getiriyor: neden bazı reseptörler kolayca kendini keserken, yakından ilişkili olan diğerleri inatla direnç gösterir?
Yapışkan Hücre Reseptörlerinde Gizli Bir Anahtar
Yapışma G protein‑bağlantılı reseptörler (aGPCR'ler) hücrelerin çevrelerine tutunmasına ve komşu hücrelerle iletişim kurmasına yardımcı olur. Bu reseptörlerin ayırt edici bir özelliği, GAIN domaini denilen kısım da dahil olmak üzere hacimli bir dış bölgedir. Bu domainin içinde gömülü kısa bir “bağlı agonist” segmanı vardır; açığa çıktığında reseptörü aktif hale getirebilir. Birçok aGPCR'de, GAIN domainindeki proteinin küçük bir bölümü belirli bir noktada kendini keserek reseptörün dış bölümünü N‑terminall ve C‑terminall fragmentlere ayırır. Kesilme, bir histidin ile serin veya treonini içeren özgül bir amino asit dizisinin yanında gerçekleşir ve bunun yerleşik kimyasal bir bıçak gibi davrandığı düşünülür.
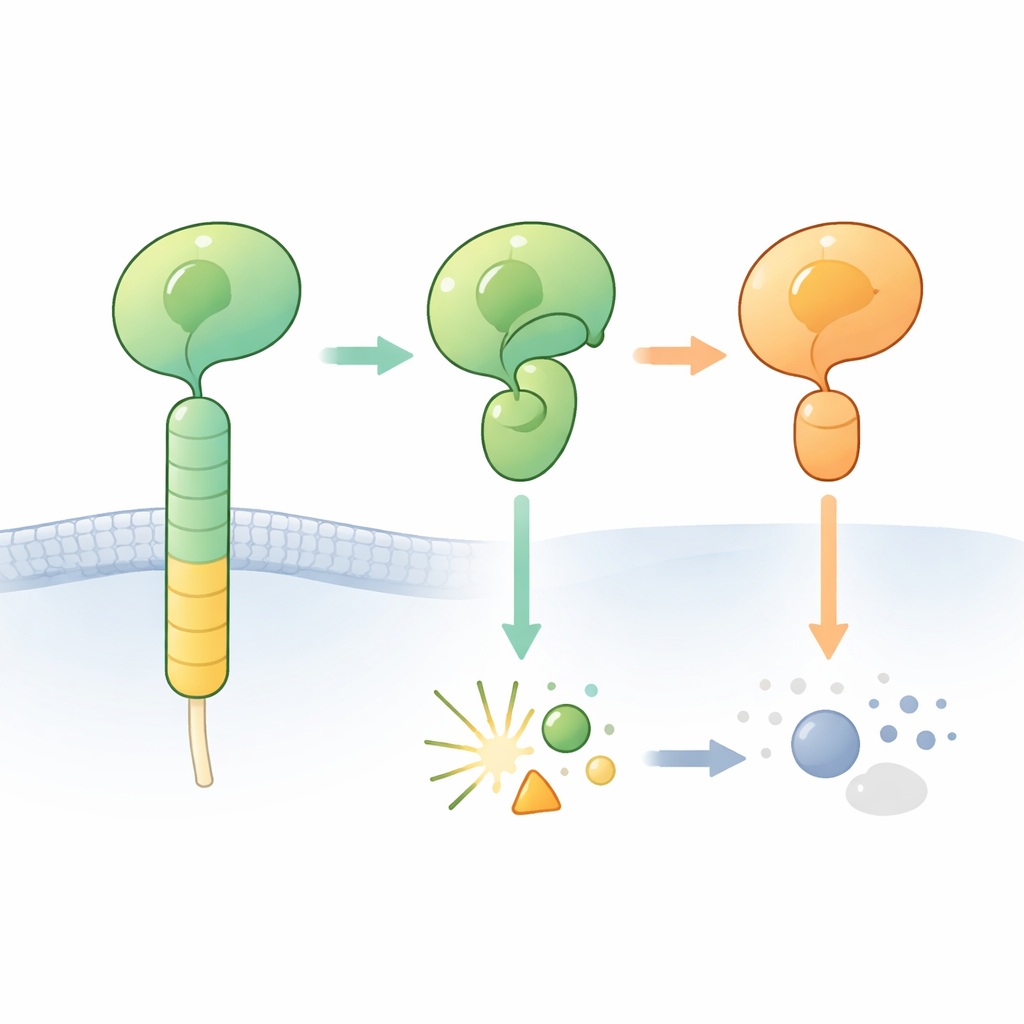
Beklenen Kesme Gerçekleşmediğinde
Araştırmacılar, GAIN domaini “doğru” histidin–lösin–serin dizisini taşımasına rağmen şaşırtıcı şekilde kesilmeye dirençli olan beyin reseptörü ADGRB2 (BAI2 olarak da bilinir) üzerine yakından odaklandı. İnsan ADGRB2'nin hormon reseptör‑benzeri ve GAIN bölgelerinin yüksek çözünürlüklü kristal yapısını belirlediler. İlginç bir şekilde, kesim bölgesi su moleküllerinin ulaşabileceği açık bir oluğa oturuyordu; ancak kritik histidin ve serin yan zincirleri kimya için hazır olmayan bir yönde konumlanmıştı: reaksiyonu başlatmak için farklı pozisyonlara dönmeleri gerekirdi. Saflaştırılmış proteini ısıtmak veya normalde tıkanmış oto‑kesim reaksiyonlarını tamamlamaya zorlayan kimyasallar eklemek kesilmeyi tetiklemedi; bu da ADGRB2'nin bu koşullar altında doğasında kesilmeye dirençli olduğunu doğruladı.
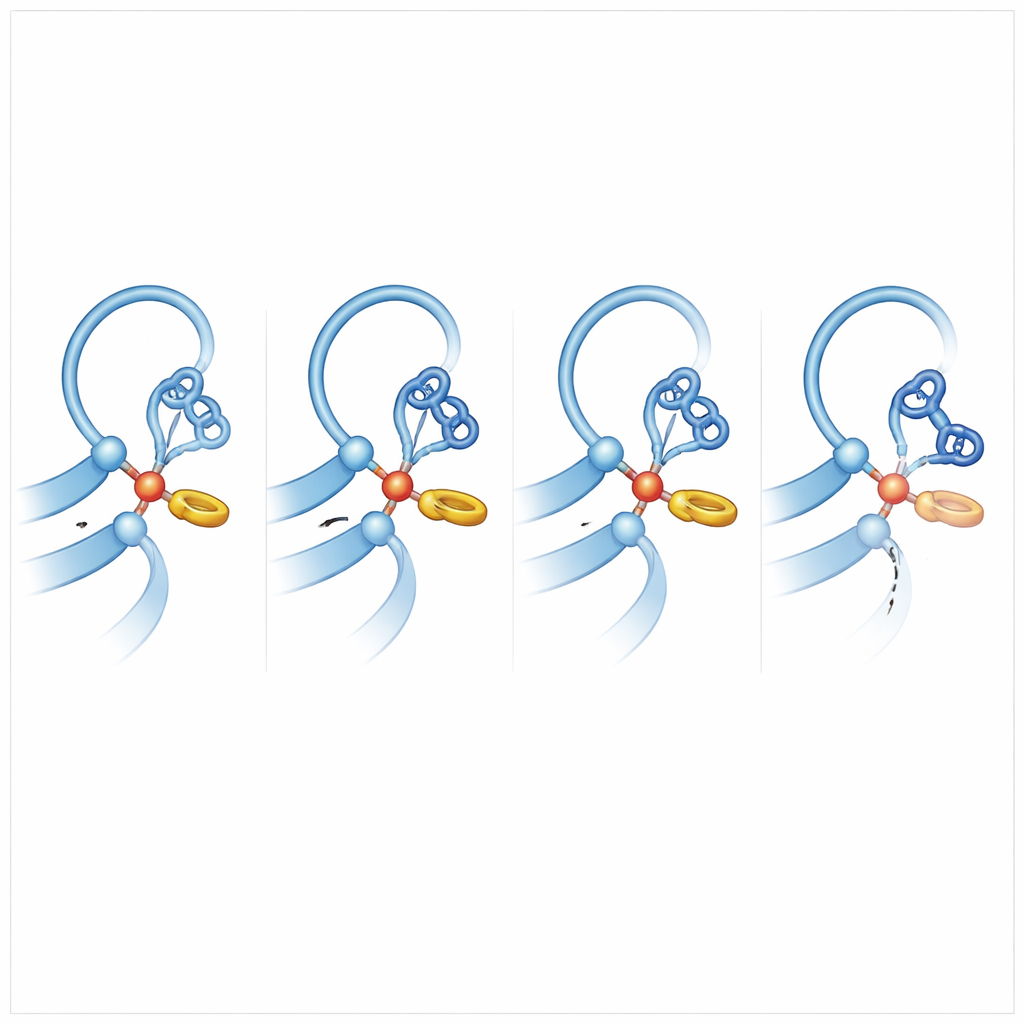
Halkalar Arası İnce Etkileşimler Kimyasal Saldırıyı Yönlendirir
Diğer reseptörleri neden daha “kesme meraklısı” olduklarını anlamak için ekip, ADGRB2'yi verimli şekilde kesen aile üyeleriyle karşılaştırdı ve atomların bilgisayarda sallanıp kaydığı geniş kapsamlı moleküler dinamik simülasyonları yürüttü. Önemli bir içgörü ortaya çıktı: kesme yetkin reseptörlerde, kesim bölgesindeki histidin, yakınındaki fenilalanin veya tirozin yan zinciriyle T‑şeklinde halka‑halkaya etkileşim içinde yuvalanır. Bu hafif itme, histidini tercih edilen bir yönelimde kilitler ve serin veya treoninden bir proton çekmeye hazır hale getirir; böylece o grup peptid bağını hedefleyen güçlü bir saldırgan olur. ADGRB2'de bu fenilalanin bir serin ile değiştirilmiş ve yakınlardaki omurga bölgesi daha hacimli bir yan zincir tarafından bozulmuştur, dolayısıyla histidin “saldırıya hazır” pozda çok daha az zaman geçirir. Simülasyonlar ayrıca verimli kesicilerde kırılacak peptid bağının genellikle hafifçe bükülerek gerilim depoladığını ve bu sayede kırılmasının kolaylaştığını gösterdi.
Ayarlanabilir Kollar Olarak Esnek Döngüler
Bu halka etkileşiminin ötesinde, GAIN domaini kesme oluğunu çerçeveleyen gevşek döngü bölgeleri veya “kapakçıklar” içerir. Bu döngüler reseptörler arasında büyük ölçüde değişir ve evrimde güçlü şekilde korunmuş değildir; yine de tam aktivite için çok önemli oldukları ortaya çıktı. Normalde kesme‑yetenekli bir reseptör (ADGRL1) ile ADGRB2 arasında kapakçık segmentlerini değiş tokuş ederek, yazarlar kesilme hızlarını artırıp azaltabildiler. Doğru konuma fenilalanin‑benzeri kalıntılar eklemek, katalitik pozisyonda bir histidin ile birleştirildiğinde normalde inaktif bir akraba olan ADGRB3'e bazı kendi‑kesme yeteneği kazandırdı. Tersine, aktif reseptörde stabilize edici fenilalanini mutasyona uğratmak veya ADGRB2‑benzeri kapakçıkları yerleştirmek kesilmeyi zayıflattı. Bu deneyler, hem hassas yerel kimyanın hem de uzun, hareketli döngülerin proteini gerilimli, reaksiyona yatkın bir duruma itmek için işbirliği yaptığını gösteriyor.
Neden Bazı Reseptörler Bütün Kalır
Bilinen neredeyse 150 memeli ADGRB2 versiyonuna bakıldığında, ekibin kesme bölgesinde ideal histidine çoğunlukla sahip olmadıklarını ve kapakçıkları ile yakın kalan kalıntıların oldukça değişken olduğunu buldu. Saflaştırılmış ADGRB2 için ölçülen yaklaşık 100 günlük yarı ömür ile birlikte bu, birçok BAI2‑benzeri reseptörün hızlı kendi‑kesmeyi önleyecek şekilde tasarlandığını düşündürüyor. Bunun yerine, bu reseptörler ya hiç kesilmeden sinyal verebilir ya da belirli dokularda çok yavaş veya bağlama‑bağlı kesilmeyi kullanabilir. Daha geniş bir bakışla, çalışma bu reseptörlerdeki kendi‑işlemmenin üç harfli bir motif tarafından kontrol edilen basit bir açma‑kapama düğmesi olmadığını gösteriyor. Bunun yerine, GAIN domaininin yerleşik bir bıçak gibi davranıp davranmayacağını veya güvenle kilitli kalıp kalmayacağını topluca ayarlayan yan zincir paketlemesi, omurga gerilimi ve hareketli döngülerin hassas dengesi ortaya çıkar. Bu dengenin anlaşılması, araştırmacıların reseptörleri kararlı ve kendi‑kesen durumlar arasında kaydıran ilaçlar tasarlamalarına ve hücrelerin mekanik kuvvetleri ve kimyasal ipuçlarını algılama şeklini değiştirmelerine olanak sağlayabilir.
Atıf: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
Anahtar kelimeler: yapışma GPCR, GAIN domaini, oto‑proteoliz, protein yapısı, moleküler dinamikler