Clear Sky Science · pt
Base estrutural da autoproteólise do domínio GAIN e resistência à clivagem nos receptores de adesão acoplados à proteína G
Como receptores na superfície celular agem como pequenas máquinas que se auto‑cortam
Nossas células estão cobertas por receptores proteicos complexos que percebem o mundo exterior. Alguns desses, chamados receptores de adesão acoplados à proteína G, comportam‑se como pequenas máquinas autocortantes: um pedaço da proteína pode cortar a si próprio, alterando a forma como o receptor sinaliza. Este estudo aborda uma pergunta aparentemente simples, com grandes implicações para a função cerebral e o desenho de fármacos: por que alguns desses receptores cortam‑se com facilidade, enquanto outros muito próximos resistem teimosamente?
Um interruptor oculto em receptores celulares aderentes
Os receptores de adesão acoplados à proteína G (aGPCRs) ajudam as células a aderir ao seu entorno e a comunicar‑se com células vizinhas. Uma característica marcante desses receptores é uma região externa volumosa que inclui o chamado domínio GAIN. Enterrado dentro desse domínio encontra‑se um curto segmento “agonista preso” que pode ativar o receptor quando exposto. Em muitos aGPCRs, uma pequena seção da cadeia proteica no domínio GAIN pode cortar‑se em um sítio específico, dividindo a porção externa do receptor em um fragmento N‑terminal e outro C‑terminal. A clivagem ocorre ao lado de uma sequência de blocos construtores particular que inclui uma histidina e uma serina ou treonina, e acredita‑se que funcione como uma lâmina química incorporada.
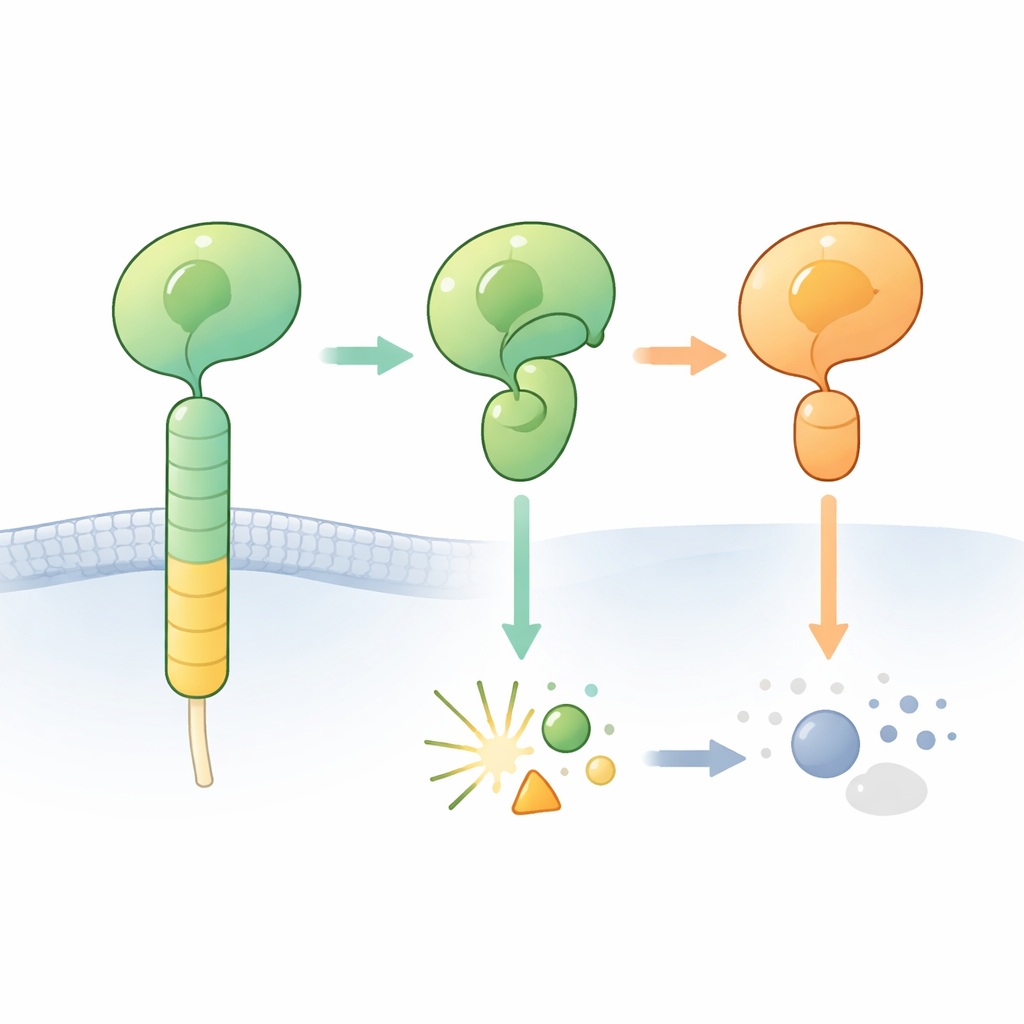
Quando o corte esperado nunca acontece
Os pesquisadores focaram em um receptor cerebral, ADGRB2 (também conhecido como BAI2), cujo domínio GAIN carrega a sequência “certa” histidina–leucina–serina, mas que é intrigantemente difícil de clivar. Eles determinaram uma estrutura cristalográfica de alta resolução das regiões semelhantes a receptor hormonal e do domínio GAIN do ADGRB2 humano. Surpreendentemente, o sítio de clivagem fica em um sulco aberto que moléculas de água podem alcançar, mas as cadeias laterais chave da histidina e da serina estão orientadas de modo que não estão prontas para a química: elas teriam de girar para posições diferentes para iniciar a reação. Aquecer a proteína purificada ou adicionar químicos que normalmente forçam reações de autocorte paralisadas a se completar não desencadeou a clivagem, confirmando que o ADGRB2 é naturalmente resistente à clivagem nessas condições.
Interações sutis entre anéis direcionam o ataque químico
Para entender o que torna outros receptores mais “cortadores”, a equipe comparou o ADGRB2 com membros da família que clivam eficientemente e executou extensas simulações de dinâmica molecular, permitindo que os átomos se agitassem e se reposicionassem no computador. Surgiu um insight chave: em receptores competentes para clivagem, a histidina no sítio de corte se aninha contra uma cadeia lateral de fenilalanina ou tirosina próxima em uma interação anel‑a‑anel em forma de T. Esse empurrão suave trava a histidina em uma orientação preferida que a alinha para retirar um próton da serina ou treonina, transformando esse grupo em um atacante potente da ligação peptídica. No ADGRB2, essa fenilalanina é substituída por uma serina, e a região da espinha dorsal próxima é distorcida por uma cadeia lateral mais volumosa, de modo que a histidina passa muito menos tempo na posição “pronta para atacar”. As simulações também mostraram que, em cortadores eficientes, a ligação peptídica a ser quebrada frequentemente está ligeiramente torcida, armazenando tensão que facilita o rompimento.
Alças flexíveis como alavancas ajustáveis
Além dessa interação entre anéis, o domínio GAIN contém regiões de alças frouxas, ou “abas”, que enquadram o sulco de corte. Essas alças variam amplamente entre receptores e não são fortemente conservadas na evolução, contudo mostram‑se cruciais para a atividade plena. Ao trocar segmentos de aba entre um receptor normalmente competente para clivagem (ADGRL1) e o ADGRB2, os autores conseguiram ajustar as taxas de clivagem para cima ou para baixo. Introduzir resíduos semelhantes à fenilalanina no ponto certo restaurou alguma capacidade de autocorte a um parente normalmente inativo, o ADGRB3, especialmente quando combinado com uma histidina na posição catalítica. Por outro lado, mutar a fenilalanina estabilizadora no receptor ativo ou enxertar abas do tipo ADGRB2 enfraqueceu a clivagem. Esses experimentos mostram que tanto a química local precisa quanto as longas alças móveis cooperam para empurrar a proteína a um estado tensionado e reativo.
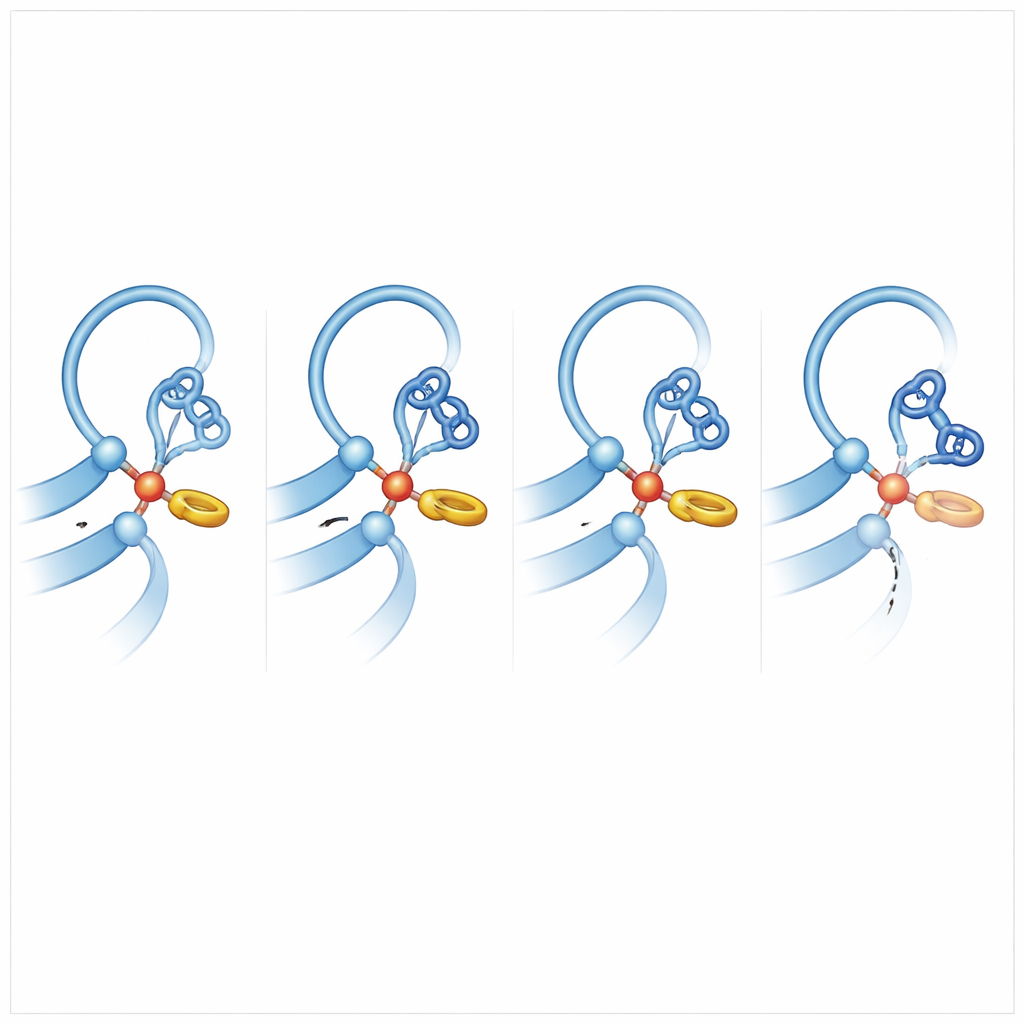
Por que alguns receptores permanecem intactos
Ao analisar quase 150 versões mamíferas do ADGRB2, a equipe encontrou que a maioria carece da histidina ideal no sítio de clivagem, e suas abas e resíduos próximos são altamente variáveis. Junto com a meia‑vida medida de cerca de 100 dias para clivagem no ADGRB2 purificado, isso sugere que muitos receptores do tipo BAI2 foram projetados para evitar o autocorte rápido. Em vez disso, podem sinalizar sem nunca se clivar ou usando uma clivagem muito lenta ou dependente do contexto em tecidos específicos. Mais amplamente, o trabalho mostra que o autoprocessamento nesses receptores não é um simples interruptor ligado–desligado controlado por um motivo de três letras. Em vez disso, ele emerge de um delicado equilíbrio de empacotamento de cadeias laterais, tensão na espinha dorsal e alças móveis que, coletivamente, ajustam se o domínio GAIN age como uma lâmina embutida ou permanece seguramente travado. Compreender esse equilíbrio pode eventualmente permitir que pesquisadores projetem fármacos que desloquem receptores entre estados estáveis e autocortantes, alterando como as células percebem forças mecânicas e sinais químicos.
Citação: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
Palavras-chave: receptor GPCR de adesão, domínio GAIN, autoproteólise, estrutura de proteínas, dinâmica molecular