Clear Sky Science · ru
Структурная основа автопротеолиза домена GAIN и устойчивости к расщеплению в адгезионных G‑белковых рецепторах, связанных с рецепторами
Как рецепторы на поверхности клетки действуют как маленькие саморассекающие машины
Поверхность наших клеток покрыта сложными рецепторными белками, которые ощущают окружающий мир. Некоторые из них, называемые адгезионными G‑белковыми рецепторами, ведут себя как крошечные саморассекающие механизмы: участок белка может разрезать сам себя, меняя способ сигнализации рецептора. В этом исследовании поставлен на вид — казалось бы — простой вопрос с большими последствиями для функций мозга и разработки лекарств: почему некоторые из этих рецепторов охотно расщепляются, тогда как близкородственные — упорно сопротивляются?
Скрытый переключатель на «липких» клеточных рецепторах
Адгезионные G‑белковые рецепторы (aGPCR) помогают клеткам прикрепляться к окружению и общаться с соседями. Характерной чертой этих рецепторов является массивная внешняя часть, включающая так называемый домен GAIN. Скрытый внутри этого домена находится короткий сегмент «прицелённого агониста», который может включать рецептор при обнажении. Во многих aGPCR небольшой участок полипептидной цепи в домене GAIN может самопроизвольно разрезаться в определённом месте, разделяя внешнюю часть рецептора на N‑ и C‑концевые фрагменты. Разрез происходит рядом с конкретной последовательностью строительных блоков, включающей гистидин и серин или треонин, и считается встроенным химическим «ножом».
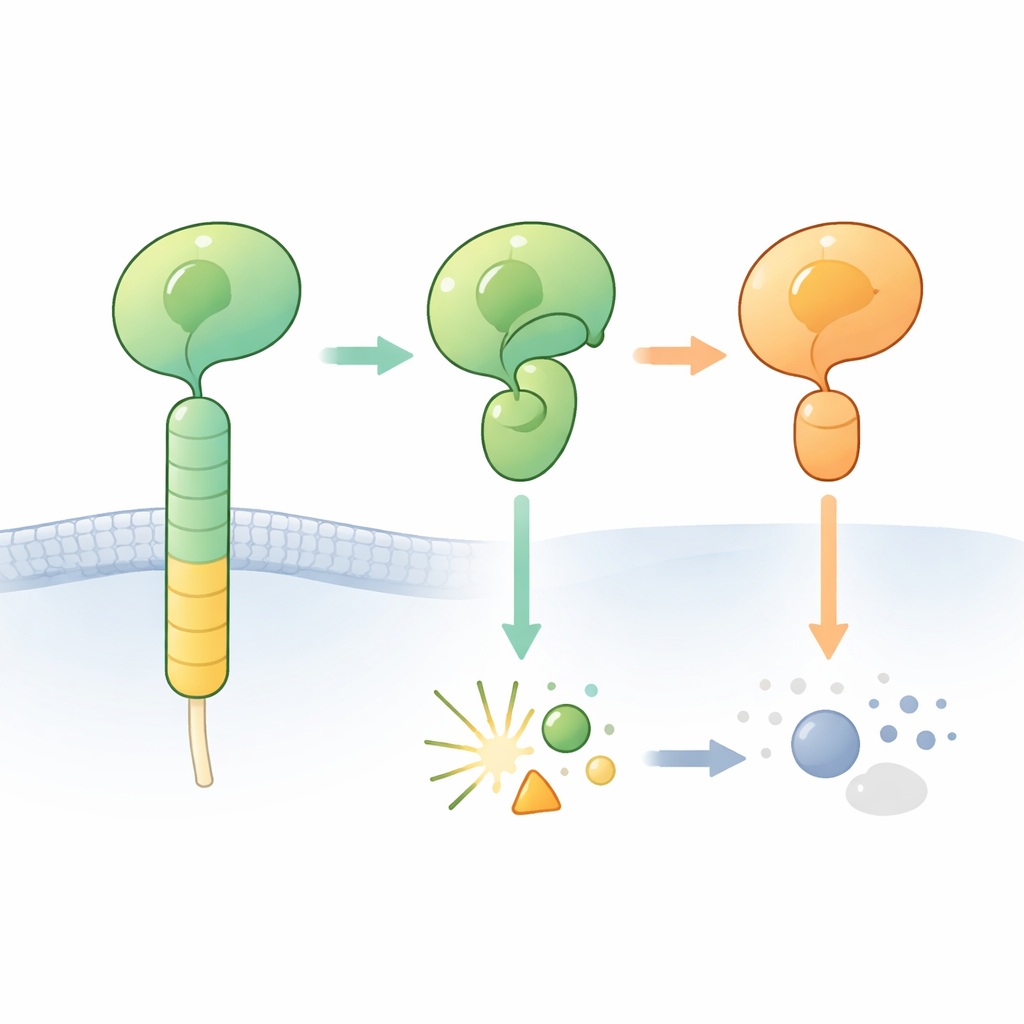
Когда ожидаемого разреза не происходит
Исследователи сосредоточились на одном мозговом рецепторе, ADGRB2 (также известном как BAI2), чей домен GAIN содержит «правильную» последовательность гистидин–лейцин–серин, но, что любопытно, его трудно разрезать. Они определили структуру кристалла высокого разрешения для гормоноподобного и GAIN‑регионов человеческого ADGRB2. Удивительно, но сайт расщепления расположен в открытой борозде, доступной для воды, однако ключевые боковые цепи гистидина и серина ориентированы так, что не готовы к химической реакции: им нужно было бы повернуться в другие положения, чтобы инициировать реакцию. Нагрев очищенного белка или добавление химических веществ, которые обычно доводят застрявшие саморасщепляющиеся реакции до конца, не вызвали кливажа, что подтверждает: ADGRB2 по своей природе устойчив к расщеплению в этих условиях.
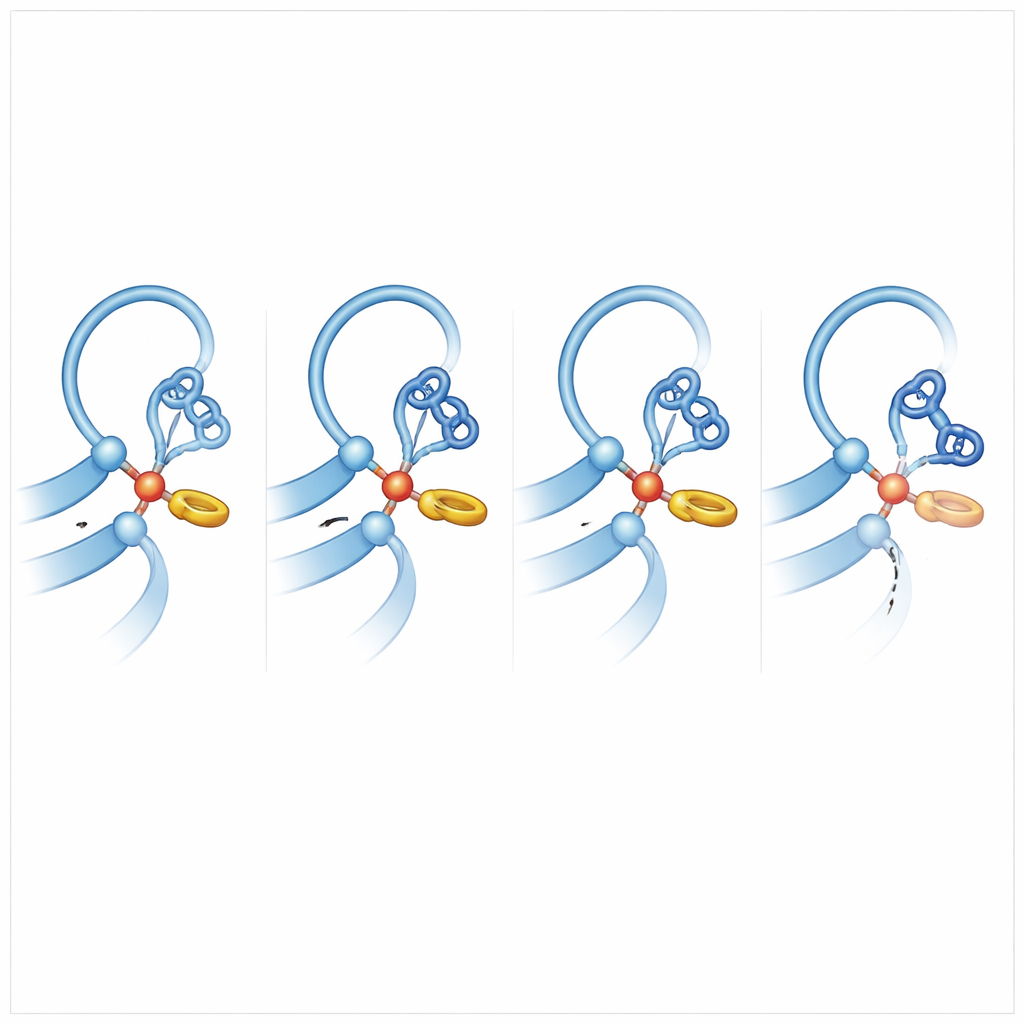
Тонкие кольцевые взаимодействия направляют химический удар
Чтобы понять, что делает другие рецепторы более «склонными к разрезанию», команда сравнила ADGRB2 с родственниками, которые эффективно расщепляются, и провела обширные симуляции молекулярной динамики, позволяя атомам дрожать и смещаться в компьютере. Важное наблюдение возникло: в расщепляющих рецепторах гистидин в месте кливача прижимается к соседней боковой цепи фенилаланина или тирозина в T‑образном кольцевом взаимодействии. Такое лёгкое подталкивание фиксирует гистидин в предпочтительной ориентации, выравнивая его для отъёма протона у серина или треонина, превращая эту группу в мощный нуклеофил, атакующий пептидную связь. В ADGRB2 этот фенилаланин заменён серином, а ближайшая к нему часть основной цепи искажена более объёмной боковой группой, поэтому гистидин гораздо реже пребывает в «готовой к атаке» позе. Симуляции также показали, что у эффективных «резаков» пептидная связь, подлежащая разрыву, часто слегка перекручена, накапливая напряжение, которое облегчает её разрыв.
Гибкие петли как регулируемые рычаги
Помимо этого кольцевого взаимодействия, домен GAIN содержит податливые петлистые области, или «клапаны», окружающие борозду разреза. Эти петли сильно варьируют между рецепторами и не строго консервативны в ходе эволюции, но оказываются существенными для полной активности. Путём замены сегментов «клапанов» между обычно расщепляющимся рецептором (ADGRL1) и ADGRB2 авторы смогли увеличить или уменьшить скорость расщепления. Введение остатков, похожих на фенилаланин, в нужное место восстановило некоторую способность к саморасщеплению у обычно неактивного родственника ADGRB3, особенно в сочетании с гистидином в каталитической позиции. Наоборот, мутация стабилизирующего фенилаланина в активном рецепторе или прививка «клапанов», похожих на ADGRB2, ослабляли расщепление. Эти эксперименты показывают, что и точная локальная химия, и длинные подвижные петли совместно способствуют переводу белка в напряжённое, реактивное состояние.
Почему некоторые рецепторы остаются целыми
Просмотрев почти 150 млекопитающих версий ADGRB2, команда обнаружила, что у большинства отсутствует идеальный гистидин в месте расщепления, а их «клапаны» и ближайшие остатки сильно варьируют. В сочетании с измеренным периодом полураспада около 100 дней для расщепления очищенного ADGRB2 это указывает на то, что многие рецепторы, похожие на BAI2, по замыслу избегают быстрого саморасщепления. Вместо этого они могут сигнализировать либо без какого‑либо очищения, либо посредством очень медленного или контекст‑зависимого расщепления в определённых тканях. В более широком смысле работа показывает, что самопроцессинг в этих рецепторах не является простым выключателем, управляемым трёхбуквенным мотивом. Скорее он возникает из тонкого баланса упаковки боковых цепей, напряжения основной цепи и подвижных петель, которые совместно настраивают, будет ли домен GAIN действовать как встроенный нож или оставаться надёжно заблокированным. Понимание этого баланса в перспективе может позволить разработчикам лекарств переводить рецепторы между стабильными и саморасщепляющимися состояниями, меняя то, как клетки воспринимают механические силы и химические сигналы.
Цитирование: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
Ключевые слова: адгезионный GPCR, домен GAIN, автопротеолиз, структура белка, молекулярная динамика