Clear Sky Science · it
Basi strutturali dell’autoproteolisi del dominio GAIN e resistenza al taglio nei recettori adesivi accoppiati a proteine G
Come i recettori di superficie cellulare funzionano come piccole macchine che si autoscolpiscono
Le nostre cellule sono rivestite da complessi recettori proteici che rilevano l’ambiente esterno. Alcuni di questi, chiamati recettori adesivi accoppiati a proteine G, si comportano come piccole macchine autoscolpitrici: una porzione della proteina può tagliarsi da sola, modificando il modo in cui il recettore segnala. Questo studio pone una domanda apparentemente semplice ma con grandi implicazioni per la funzione cerebrale e la progettazione di farmaci: perché alcuni di questi recettori si tagliano facilmente, mentre altri strettamente correlati resistono tenacemente?
Un interruttore nascosto sui recettori adesivi
I recettori adesivi accoppiati a proteine G (aGPCR) aiutano le cellule ad aderire all’ambiente circostante e a comunicare con le cellule vicine. Una caratteristica di questi recettori è una regione esterna ingombrante che include il cosiddetto dominio GAIN. Nascosto all’interno di questo dominio si trova un breve segmento “agonista tethered” che può attivare il recettore quando viene esposto. In molti aGPCR, una piccola porzione della catena proteica nel dominio GAIN può tagliarsi in un sito specifico, dividendo la parte esterna del recettore in un frammento N-terminale e uno C-terminale. Il taglio avviene accanto a una sequenza di aminoacidi particolare che include un istidina e una serina o treonina ed è ritenuto funzionare come un coltello chimico incorporato.
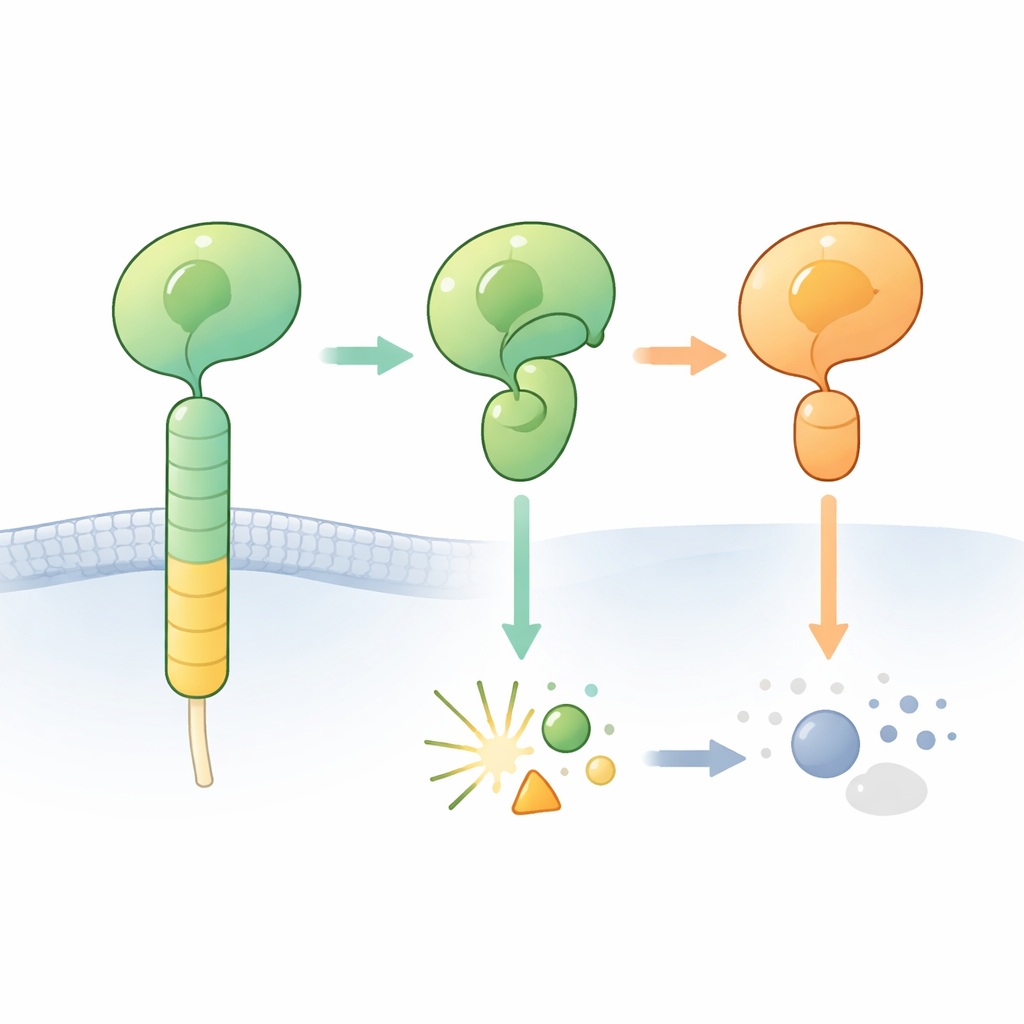
Quando il taglio previsto non avviene
I ricercatori si sono concentrati su un recettore cerebrale, ADGRB2 (noto anche come BAI2), il cui dominio GAIN presenta la sequenza “corretta” istidina‑leucina‑serina ma risulta sorprendentemente difficile da tagliare. Hanno determinato una struttura cristallina ad alta risoluzione delle regioni simili a recettore ormonale e del dominio GAIN di ADGRB2 umano. A sorpresa, il sito di clivaggio si trova in una scanalatura aperta raggiungibile dall’acqua, ma le catene laterali chiave dell’istidina e della serina sono orientate in modo non pronto per la reazione: dovrebbero ruotare in posizioni differenti per avviare il processo chimico. Riscaldare la proteina purificata o aggiungere sostanze chimiche che normalmente completano reazioni di autoscissione bloccate non ha scatenato il taglio, confermando che ADGRB2 è naturalmente resistente al clivaggio in queste condizioni.
Interazioni sottili tra anelli guidano l’attacco chimico
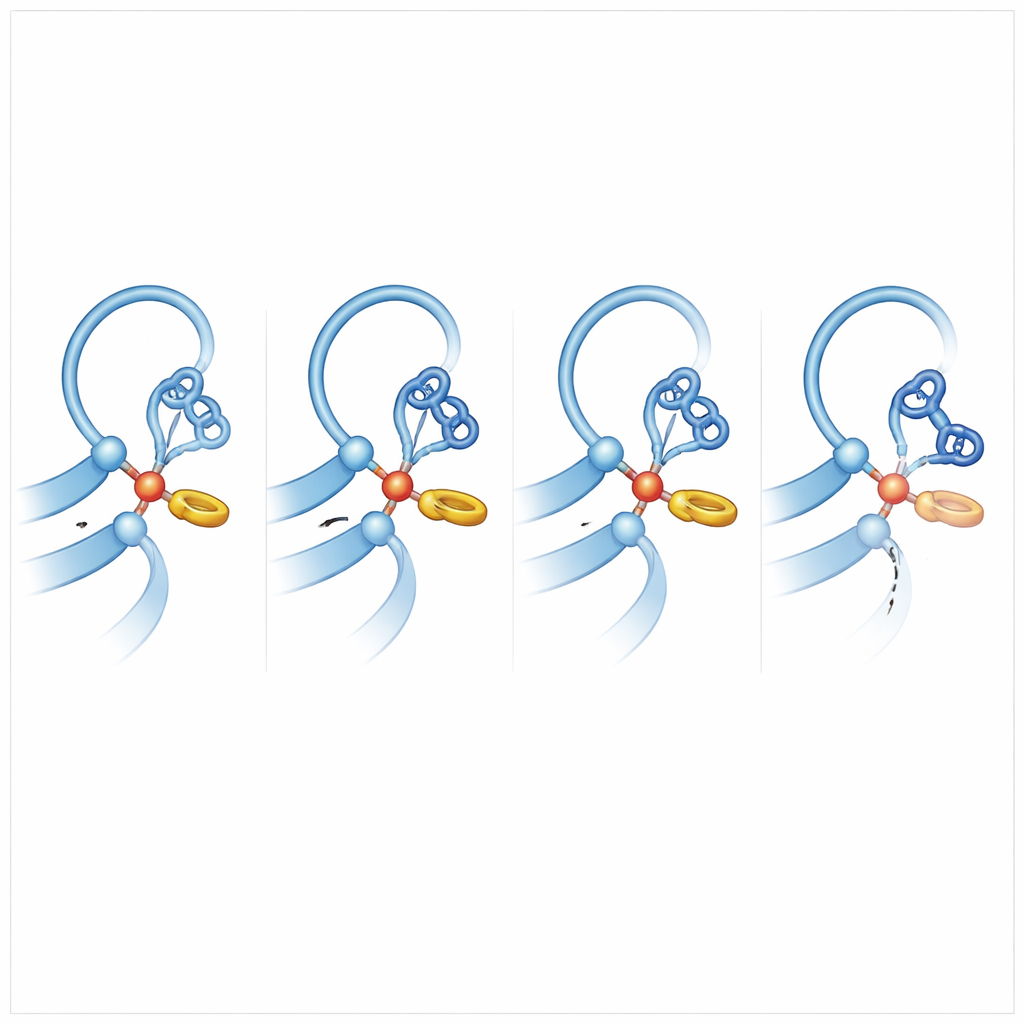
Per capire cosa rende altri recettori più inclini al taglio, il gruppo ha confrontato ADGRB2 con membri della famiglia che si clivano efficacemente e ha eseguito estese simulazioni di dinamica molecolare, lasciando gli atomi vibrare e spostarsi in silico. È emerso un insight chiave: nei recettori competenti per il clivaggio, l’istidina nel sito di taglio si appoggia contro una catena laterale vicina di fenilalanina o tirosina in un’interazione anello‑contro‑anello a T. Questo leggero spintone blocca l’istidina in un’orientazione preferita che la mette in linea per togliere un protone dalla serina o treonina, trasformando quel gruppo in un potente attaccante del legame peptidico. In ADGRB2, questa fenilalanina è sostituita da una serina e la regione di backbone vicina è distorta da una catena laterale più ingombrante, così l’istidina passa molto meno tempo nella posa «pronta all’attacco». Le simulazioni hanno mostrato anche che nei recettori efficienti, il legame peptidico da rompere è spesso leggermente torsionato, accumulando tensione che facilita la rottura.
Loop flessibili come leve regolabili
Oltre a questa interazione tra anelli, il dominio GAIN contiene regioni ad anse flosce, o «alette», che incorniciano la scanalatura di taglio. Queste anse variano molto tra i recettori e non sono fortemente conservate dall’evoluzione, eppure risultano cruciali per l’attività completa. Scambiando segmenti di anse tra un recettore normalmente competente per il clivaggio (ADGRL1) e ADGRB2, gli autori sono riusciti a modulare i tassi di clivaggio verso l’alto o verso il basso. L’introduzione di residui simili alla fenilalanina nel punto giusto ha ripristinato parte della capacità di autoscissione in un parente normalmente inattivo, ADGRB3, soprattutto se combinata con un’istidina nella posizione catalitica. Al contrario, mutare la fenilalanina stabilizzante nel recettore attivo o innestare anse in stile ADGRB2 ne ha indebolito il clivaggio. Questi esperimenti mostrano che sia la chimica locale precisa sia le lunghe anse mobili cooperano per spingere la proteina in uno stato teso e reattivo.
Perché alcuni recettori restano intatti
Analizzando quasi 150 versioni amniote di ADGRB2, il team ha scoperto che la maggior parte manca dell’istidina ideale nel sito di taglio, e le loro anse e i residui vicini sono altamente variabili. Unito alla vita media misurata di circa 100 giorni per il clivaggio nella ADGRB2 purificata, ciò suggerisce che molti recettori simili a BAI2 sono progettati per evitare un’autoscucciatura rapida. Invece, possono segnalare senza mai clivarsi o usando un clivaggio molto lento o dipendente dal contesto in tessuti specifici. Più in generale, il lavoro mostra che l’autoprocessamento in questi recettori non è un semplice interruttore acceso‑spento controllato da un motivo di tre lettere. Piuttosto, emerge da un delicato equilibrio di impacchettamento delle catene laterali, tensione del backbone e anse mobili che insieme modulano se il dominio GAIN agisca come un coltello incorporato o resti saldamente bloccato. Comprendere questo equilibrio potrebbe alla lunga permettere ai ricercatori di progettare farmaci che spostino i recettori tra stati stabili e auto‑taglianti, modificando il modo in cui le cellule percepiscono forze meccaniche e segnali chimici.
Citazione: Pohl, F., Seufert, F., Chung, Y.K. et al. Structural basis of GAIN domain autoproteolysis and cleavage-resistance in the adhesion G-protein coupled receptors. Nat Commun 17, 3259 (2026). https://doi.org/10.1038/s41467-026-71225-1
Parole chiave: recettore GPCR adesivo, dominio GAIN, autoproteolisi, struttura proteica, dinamica molecolare