Clear Sky Science · zh
AcuB感知细胞能量电荷以协调细菌中乙酰辅酶A的合成
细菌如何决定何时合成细胞燃料
细菌生活在不断变化的环境中,食物和能量供应可能在丰饶与饥荒之间波动。为求生存,它们必须精细调控一种称为乙酰-CoA的核心燃料分子,这一分子供给许多关键过程。本研究揭示了一种名为AcuB的细菌蛋白如何充当内部“能量表”,帮助细胞决定何时开启或关闭乙酰-CoA的生成,从而避免既浪费资源又陷入饥饿。
控制乙酸利用的分子交换台
这项工作以土壤细菌枯草芽孢杆菌及其近缘种为研究对象,它们能将简单分子乙酸既作为废物也作为营养物质利用。一种酶AcsA把乙酸转化为乙酰-CoA,在首选糖类如葡萄糖匮乏时为生长提供原料。另一条途径则由两种酶Pta和Ack驱动,将反应推向相反方向,把乙酰-CoA转回乙酸并将其释放出细胞。如果两条反向通路同时运转将极为浪费,因此细胞必须协调这些途径。此前的研究表明,AcsA可通过附加一个小的化学标签(乙酰基)被关闭,而在该标签被移除时再被重新激活,但这两个相对步骤如何协调一直不清楚。
AcuB的隐秘角色被揭示
就在acsA基因旁边有一簇包含三个基因的acu操纵子,编码AcuA、AcuB和AcuC三种蛋白。AcuA把乙酰标签加到AcsA上,使其失活,而AcuC则去除该标签并重新激活该酶。AcuB的作用此前一直不明。在本研究中,作者在实验室制备了来自若干细菌物种的AcuB蛋白并分析其性质。他们发现AcuB天然结合小型能量载体分子——AMP、ADP和ATP,以及一种应激信号分子Ap4A。通过生化实验证明,当AcuB结合AMP时,它会强烈结合AcuC并抑制其去乙酰化酶活性,从而阻止AcsA被重新激活。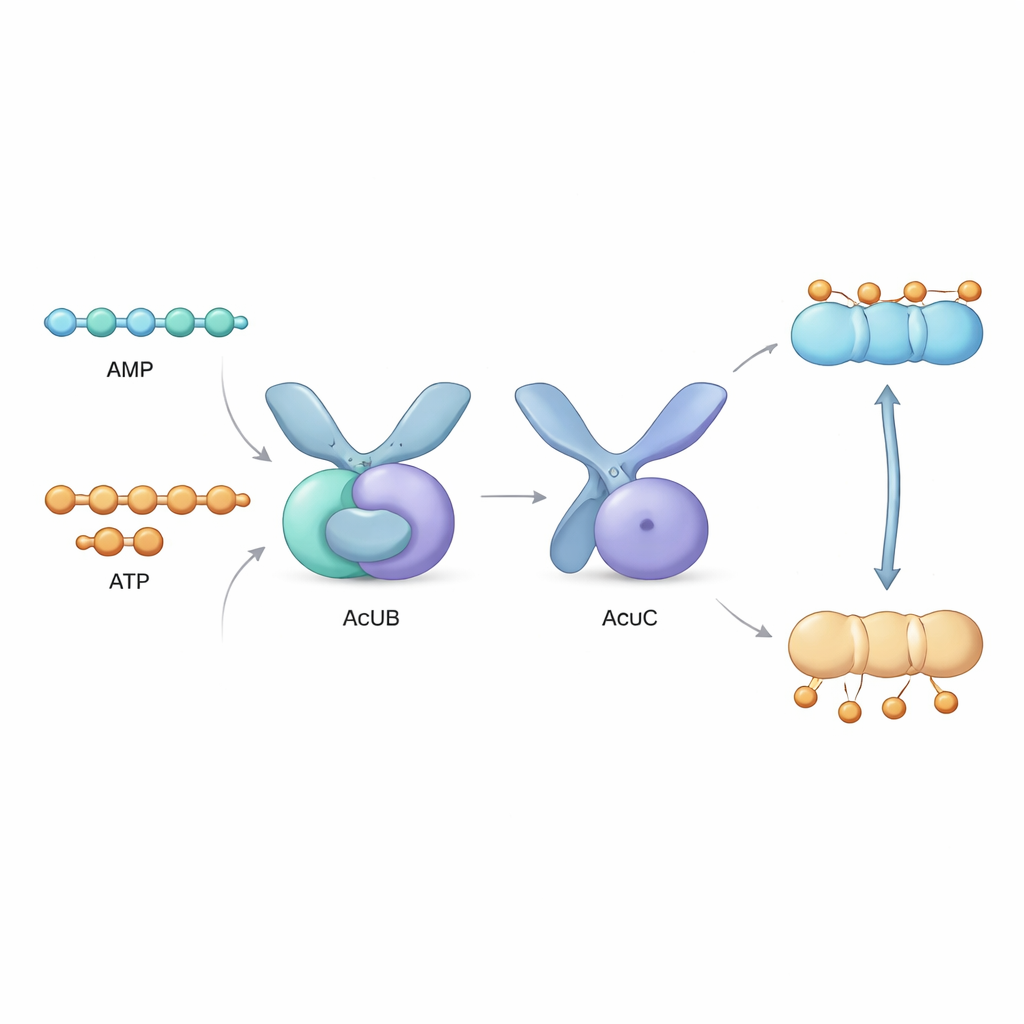
通过变形的蛋白读取能量状态
为了在原子水平上理解其工作方式,研究组使用X射线晶体学解析了两种细菌来源AcuB的三维结构。AcuB形成一对剪刀状的蛋白单元,每个单元具有一对口袋状的“传感器”区,用以结合含腺嘌呤的核苷酸,以及一个与AcuC接触的“柄”区。每个AcuB二聚体可容纳四个核苷酸分子。研究者观察到这些口袋由带正电的氨基酸残基衬里,它们与AMP、ADP、ATP或Ap4A的相互作用不同。计算模拟显示,当结合AMP时,AcuB倾向于采纳紧凑构象,便于夹住并阻断AcuC。相反,当结合ATP或ADP时,蛋白转向更伸展或更具柔性的形态,从而削弱其对AcuC的束缚,允许去乙酰化酶发挥作用。
为燃料合成提供的内建安全机制
将这些发现结合起来,作者提出AcuB是一种能量传感器,读取细胞内AMP与ATP之间的平衡。当能量匮乏时,AMP水平升高,AcuB结合AMP,夹住AcuC并阻止其重新激活AcsA。结果,AcsA保持乙酰化且失活,细胞避免将宝贵能量用于合成超出承受能力的乙酰-CoA。当能量充足且ATP占优时,AcuB释放AcuC,后者去除AcsA上的乙酰标签,使乙酸可以被转化为乙酰-CoA并为生物合成提供燃料。
为何这超越单一细菌具有重要性
这项工作将AcuB确定为长期寻觅的连接器,将两条相对的乙酸通路与细胞的能量状态协调起来。通过将化学“能量电荷”与酶活性耦合,借助可逆的蛋白–蛋白相互作用和构象变化,细菌确保资源的高效利用并避免冲突的代谢流。该发现还暗示类似的能量感应开关可能广泛存在,并且诸如Ap4A之类的应激信号可以微调这种控制,帮助微生物应对恶劣环境。
引用: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
关键词: 细菌代谢, 能量感应, 乙酰-CoA, 蛋白质乙酰化, 变构调控