Clear Sky Science · he
AcuB חשה את מטען האנרגיה התאית כדי לתאם סינתזת אצטיל‑CoA בחיידקים
כיצד חיידקים מחליטים מתי לייצר דלק תאי
חיידקים חיים בסביבות שמשתנות ברצף, שבהן מאגרי מזון ואנרגיה יכולים לנוע בין שפע לרעב. כדי לשרוד הם חייבים לנהל בזהירות מולקולה מרכזית של דלק הנקראת אצטיל‑CoA, שמזינה תהליכים חיוניים רבים. המחקר הזה מגלה כיצד חלבון חיידקי בשם AcuB מתפקד כ"מד אנרגיה" פנימי, ומסייע לתאים להחליט מתי להפעיל או לכבות את יצירת האצטיל‑CoA כדי שלא יבזבזו משאבים ולא ייתקלו במחסור.
לוח חשמל מולקולרי לשימוש באצטט
העבודה מתמקדת בחיידק הקרקע Bacillus subtilis ובקרובים שלו, שיכולים להשתמש במולקולה הפשוטה אצטט הן כפסולת והן כמקור מזון. אנזים אחד, AcsA, ממיר אצטט לאצטיל‑CoA ומזין גדילה כאשר סוכרים מועדפים כמו גלוקוז נדירים. מסלול אחר, שכולל שני אנזימים בשם Pta ו‑Ack, דוחף את התגובה בכיוון ההפוך, והופך אצטיל‑CoA חזרה לאצטט ומשחרר אותו מהתא. הפעלת שני הכיוונים בו‑זמנית תהיה בזבזנית, ולכן התא חייב לתאם בין המסלולים. מחקרים מוקדמים הראו שניתן לכבות את AcsA על‑ידי הוספת תג כימי קטן (קבוצת אצטיל) ולהחזירו לפעולה כאשר התג מוסר, אך לא היה ברור כיצד שני הצעדים הנגדיים הללו מתואמים.
התפקיד הנסתר של AcuB נחשף
ישירות ליד הגֵן acsA נמצא אשכול של שלושה גנים, הקרוי האופרון acu, שמקודד לחלבונים AcuA, AcuB ו‑AcuC. AcuA מוסיף את תג האצטיל על AcsA וכיבית אותו, בעוד AcuC מסיר את התג ומחזיר את האנזים לפעולה. תפקידו של AcuB נותר מסתורי. במחקר זה החוקרם הפיקו חלבוני AcuB ממספר מינים של חיידקים במעבדה וניתחו את התנהגותם. הם גילו ש‑AcuB נקשר באופן טבעי למולקולות נשא‑אנרגיה קטנות — AMP, ADP ו‑ATP — וכן למולקולת אות לחץ הנקראת Ap4A. בעזרת מבחני ביו‑כימיה הראו שכאשר AcuB מטען ב‑AMP, הוא נקשר בחוזקה ל‑AcuC וגורם לעיכוב פעילות הדה‑אצטילאז שלו, ובכך מונע את החזרת הפעילות של AcsA.
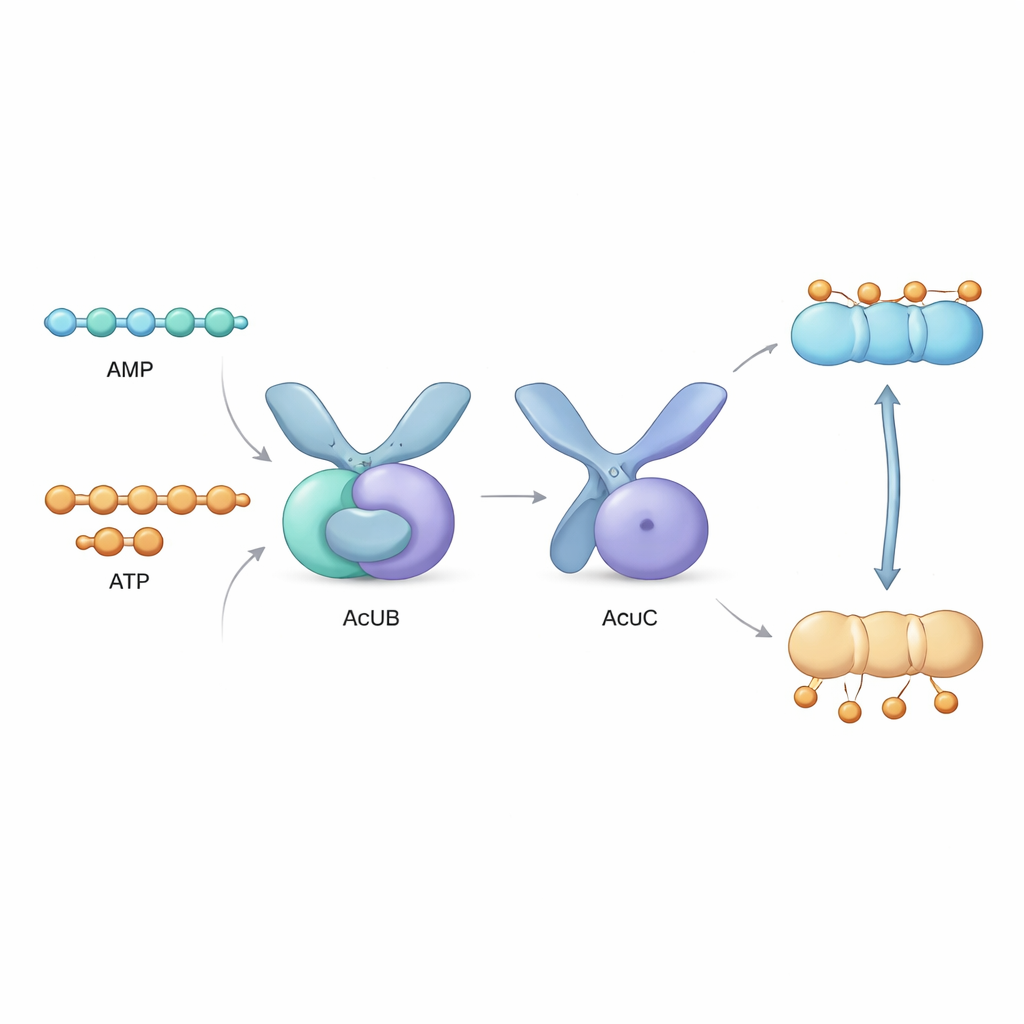
קריאת אנרגיה על‑ידי חלבונים שמשנים צורה
כדי להבין כיצד זה פועל ברמת האטומים, הצוות השתמש בקריסטלוגרפיית קרני‑X כדי לפתור את המבנים התלת‑ממדיים של AcuB משני חיידקים. AcuB יוצר זוג יחידות חלבוניות בדומה למספריים, כאשר לכל יחידה יש "חיישן" עם שתי כיסים הקושרים נוקלאוטידים מבוססי אדנין, ו"ידית" שמייצרת מגע עם AcuC. ארבע מולקולות נוקלאוטיד יכולות להיכנס לכל דימר של AcuB. החוקרים תיארו כיצד הכיסים מרופדים בחומצות אמינו טעונות חיובית שמתקשרות בצורה שונה עם AMP, ADP, ATP או Ap4A. סימולציות מחשב הראו שכאשר AMP קשור, AcuB נוטה לאמץ קונפורמציה קומפקטית שמתאימה לעטיפה וחסימה של AcuC. לעומת זאת, כאשר ATP או ADP קשורים, החלבון משנה את צורתו ליותר מוארכת או גמישה שמחלישה את אחיזתו ב‑AcuC ומאפשרת את פעולת הדה‑אצטילאז.
מנגנון בטיחות מובנה לייצור דלק
לאיחוד הממצאים, המחברים מציעים ש‑AcuB הוא חיישן אנרגיה שקורא את האיזון בין AMP ל‑ATP בתוך התא. כאשר האנרגיה נמוכה, רמות AMP עולות. AcuB נקשר ל‑AMP, מה שמביא לעיגון שלו על AcuC ומונע ממנו להחזיר את AcsA לפעולה. כתוצאה מכך, AcsA נשאר אצטילט ובלתי פעיל, והתא נמנע מהשקעת אנרגיה יקרה בייצור יותר מדי אצטיל‑CoA. כאשר האנרגיה בשפע ו‑ATP שולט, AcuB משחרר את AcuC, שמסיר אז את תגי האצטיל מ‑AcsA, מה שמאפשר המרת אצטט לאצטיל‑CoA והזנת הביוסינתזה.
מדוע זה חשוב מעבר לחיידק אחד
עבודה זו מזהה את AcuB כקשר שחיפשו זמן רב, שתואם בין שני מסלולי אצטט מנוגדים לבין מצב האנרגיה של התא. על‑ידי חיבור "מטען האנרגיה" הכימי לפעילות אנזימטית באמצעות אינטראקציות חלבון‑חלבון הפיכות ושינויים קונפורמציוניים, חיידקים מבטיחים שימוש יעיל במשאבים ומונעים זרימות מטבוליות מנוגדות. הגילוי גם מרמז שמפסקים חישת‑אנרגיה דומים עשויים להיות נפוצים, ושאותות לחץ כמו Ap4A יכולים לכוונן את הבקרה הזאת, ולעזור למיקרובים להתמודד עם תנאים קשים.
ציטוט: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
מילות מפתח: מטבוליזם חיידקי, חישת אנרגיה, אצטיל‑CoA, אצטילציה של חלבונים, ויסות אלוסטרי