Clear Sky Science · pt
AcuB detecta a carga de energia celular para coordenar a síntese de acetil-CoA em bactérias
Como as bactérias decidem quando produzir combustível celular
Bactérias vivem em ambientes em constante mudança, onde suprimentos de alimento e energia podem oscilar entre fartura e escassez. Para sobreviver, elas precisam gerenciar com cuidado uma molécula de combustível central chamada acetil-CoA, que alimenta muitos processos vitais. Este estudo revela como uma proteína bacteriana chamada AcuB atua como um “medidor de energia” interno, ajudando as células a decidir quando ligar ou desligar a produção de acetil-CoA para que não desperdicem recursos nem passem fome. 
Um painel molecular para o uso do acetato
O trabalho foca na bactéria do solo Bacillus subtilis e seus parentes, que podem usar a molécula simples acetato tanto como produto de desperdício quanto como nutriente. Uma enzima, AcsA, converte acetato em acetil-CoA, alimentando o crescimento quando açúcares preferenciais como a glicose são escassos. Outra via, envolvendo duas enzimas chamadas Pta e Ack, empurra a reação na direção oposta, transformando acetil-CoA de volta em acetato e liberando-o da célula. Executar as duas direções ao mesmo tempo seria dispendioso, então a célula precisa coordenar essas rotas. Estudos anteriores mostraram que AcsA pode ser desligada pela adição de uma pequena etiqueta química (um grupo acetil) e religada quando essa etiqueta é removida, mas como esses dois passos opostos eram coordenados não estava claro.
O papel oculto de AcuB revelado
Logo ao lado do gene acsA fica um conjunto de três genes, chamado operon acu, que codificam as proteínas AcuA, AcuB e AcuC. AcuA coloca a marca acetil em AcsA, inativando-a, enquanto AcuC remove a marca e reativa a enzima. O papel de AcuB permanecia misterioso. Neste estudo, os autores produziram proteínas AcuB de várias espécies bacterianas em laboratório e analisaram seu comportamento. Descobriram que AcuB se liga naturalmente a pequenas moléculas transportadoras de energia—AMP, ADP e ATP—bem como a uma molécula sinal de estresse chamada Ap4A. Usando testes bioquímicos, mostraram que quando AcuB está carregada com AMP, ela se liga fortemente à AcuC e bloqueia sua atividade desacetilase, impedindo a reativação de AcsA. 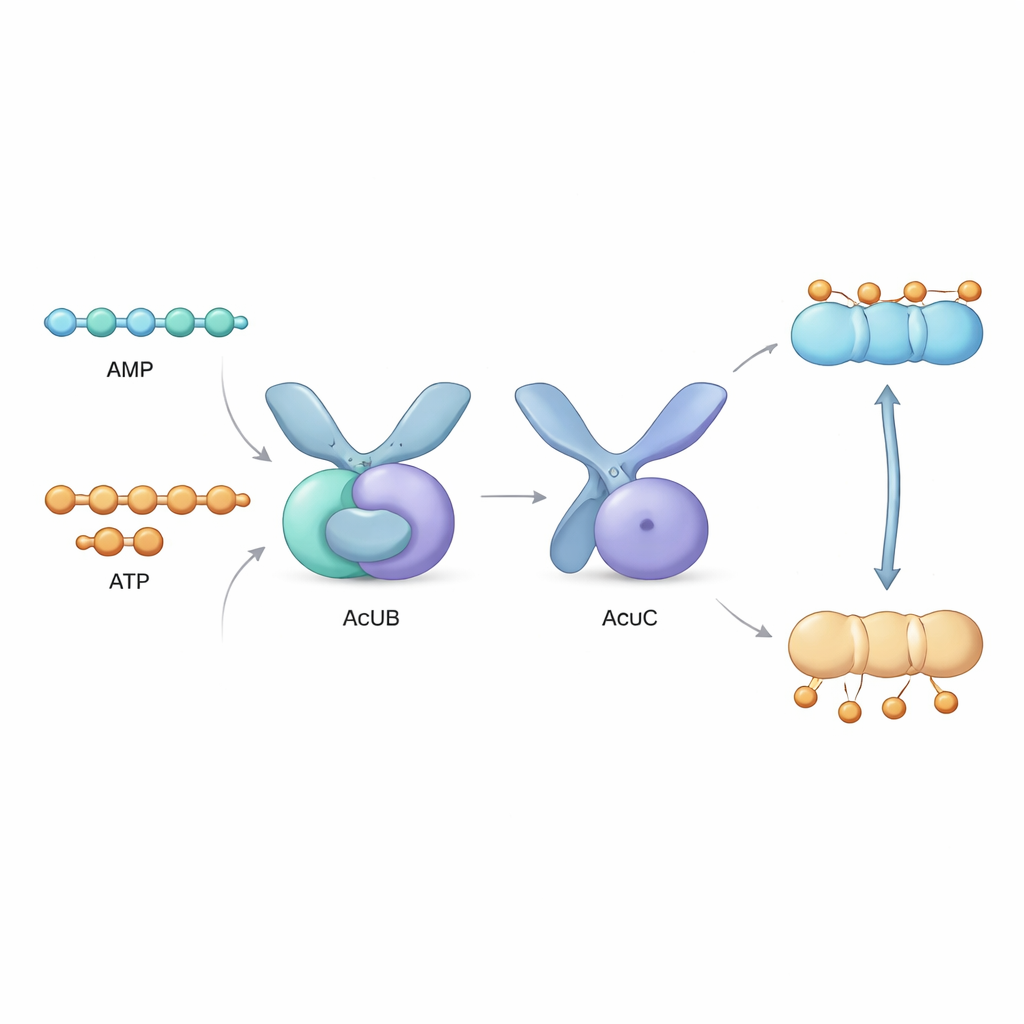
Leitura de energia por proteínas que mudam de forma
Para ver como isso funciona em nível atômico, a equipe usou cristalografia de raios X para resolver as estruturas tridimensionais de AcuB de duas bactérias. AcuB forma um par de unidades proteicas em forma de tesoura, cada uma com uma seção “sensor” de bolso duplo que liga nucleotídeos à base de adenina e uma seção “alça” que contata AcuC. Quatro moléculas de nucleotídeo podem encaixar-se em cada dímero de AcuB. Os pesquisadores observaram como esses bolsos são revestidos por aminoácidos carregados positivamente que interagem de maneira distinta com AMP, ADP, ATP ou Ap4A. Simulações por computador mostraram que quando AMP está ligado, AcuB tende a adotar uma conformação compacta bem adequada para abraçar e bloquear AcuC. Em contraste, quando ATP ou ADP se ligam, a proteína desloca-se para formas mais estendidas ou flexíveis que enfraquecem sua interação com AcuC e permitem que a desacetilase funcione.
Um mecanismo de segurança embutido para a produção de combustível
Reunindo essas descobertas, os autores propõem que AcuB é um sensor de energia que lê o equilíbrio entre AMP e ATP dentro da célula. Quando a energia está baixa, os níveis de AMP aumentam. AcuB liga AMP, prende AcuC e impede que ele reative AcsA. Como resultado, AcsA permanece acetilada e inativa, e a célula evita comprometer energia preciosa para produzir mais acetil-CoA do que pode sustentar. Quando a energia é abundante e o ATP domina, AcuB libera AcuC, que então remove as marcas acetil de AcsA, permitindo que o acetato seja convertido em acetil-CoA e alimente a biossíntese.
Por que isso importa além de uma única bactéria
Este trabalho identifica AcuB como o elo tão procurado que coordena duas vias opostas do acetato com o status energético da célula. Ao acoplar a “carga de energia” química à atividade enzimática por meio de interações proteína–proteína reversíveis e mudanças conformacionais, as bactérias garantem uso eficiente dos recursos e evitam fluxos metabólicos conflitantes. A descoberta também sugere que interruptores sensoriais de energia semelhantes podem ser amplamente distribuídos, e que sinais de estresse como Ap4A podem ajustar finamente esse controle, ajudando microrganismos a enfrentar condições adversas.
Citação: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
Palavras-chave: metabolismo bacteriano, sensoriamento de energia, acetil-CoA, acetilação de proteínas, regulação alostérica