Clear Sky Science · sv
AcuB känner av cellens energiladdning för att samordna syntesen av acetyl‑CoA i bakterier
Hur bakterier avgör när de ska tillverka cellbränsle
Bakterier lever i ständigt skiftande miljöer där födo‑ och energitillgångar kan pendla mellan överflöd och brist. För att överleva måste de noggrant hantera en central bränslemolekyl kallad acetyl‑CoA, som försörjer många viktiga processer. Denna studie avslöjar hur ett bakteriellt protein som heter AcuB fungerar som en intern ”energimätare” och hjälper cellerna att avgöra när produktionen av acetyl‑CoA ska slås på eller av, så att de varken slösar resurser eller blir utarmade. 
En molekylär växelcentral för användning av acetat
Arbetet fokuserar på jordbakterien Bacillus subtilis och dess släktingar, som kan använda den enkla molekylen acetat både som avfallsprodukt och som näringsämne. Ett enzym, AcsA, omvandlar acetat till acetyl‑CoA och ger näring åt tillväxt när föredragna sockerarter som glukos är knappa. En annan väg, som involverar två enzymer kallade Pta och Ack, driver reaktionen i motsatt riktning och omvandlar acetyl‑CoA tillbaka till acetat som sedan släpps ut ur cellen. Att köra båda riktningarna samtidigt vore slöseri, så cellen måste samordna dessa vägar. Tidigare studier visade att AcsA kan stängas av genom att fästa en liten kemisk etikett (en acetylgrupp) och återaktiveras när denna etikett tas bort, men hur dessa två motsatta steg koordinerades var inte känt.
AcuB:s dolda roll avslöjas
Precis intill acsA‑genen ligger en kluster av tre gener, kallad acu‑operonet, som kodar för proteinerna AcuA, AcuB och AcuC. AcuA fäster acetylkollen på AcsA och inaktiverar det, medan AcuC tar bort kollen och återaktiverar enzymet. AcuB:s roll hade förblivit mystisk. I denna studie framställde författarna AcuB‑proteiner från flera bakteriearter i labbet och analyserade deras beteende. De upptäckte att AcuB naturligt binder små energibärande molekyler — AMP, ADP och ATP — samt en stressignalmolekyl kallad Ap4A. Med biokemiska tester visade de att när AcuB är laddat med AMP binder det starkt till AcuC och stänger av dess deacetylasaktivitet, vilket förhindrar att AcsA återaktiveras. 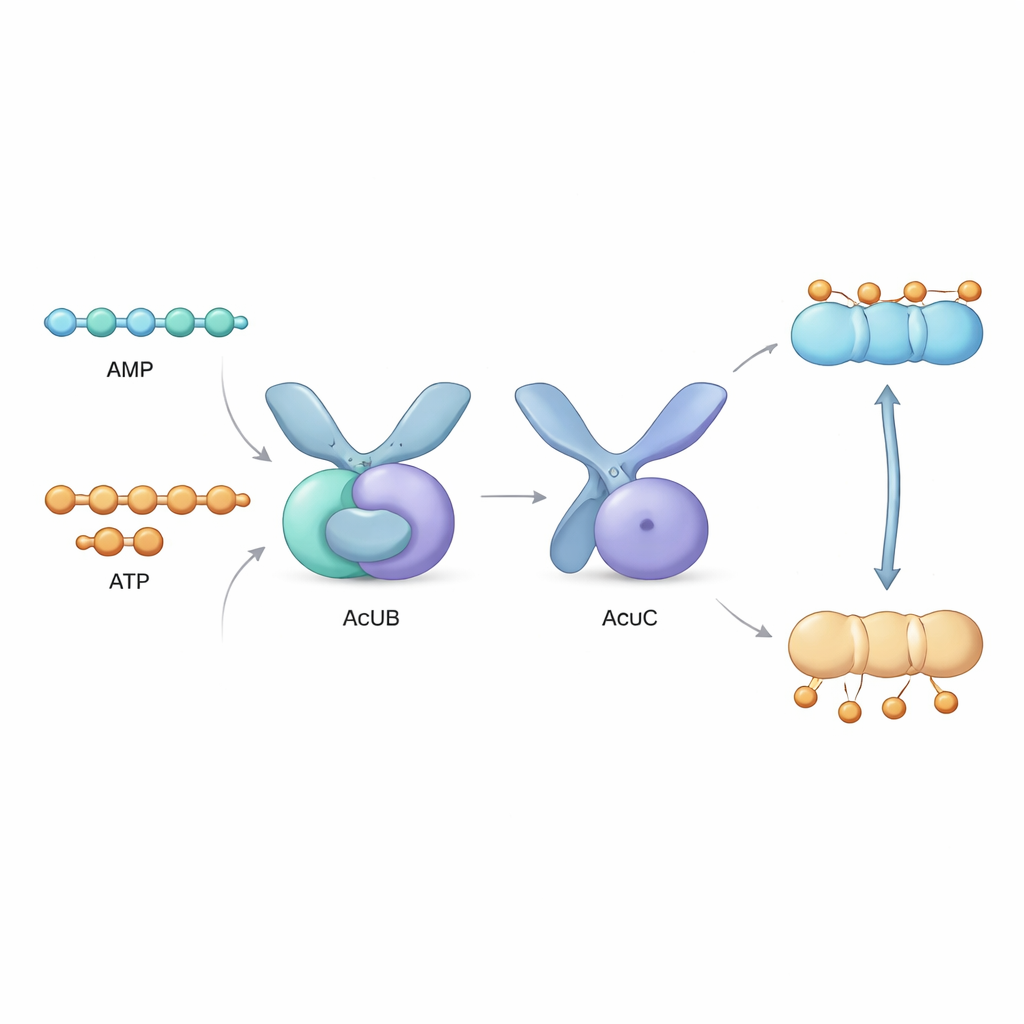
Energiavläsning genom formförändrande proteiner
För att se hur detta fungerar på atomnivå använde teamet röntgenkristallografi för att bestämma AcuB:s tredimensionella strukturer från två bakterier. AcuB bildar ett saxliknande par av proteinenheter, vardera med en dubbelbrunnig ”sensor” som binder adeninbaserade nukleotider och en ”handtags”‑sektion som kontaktar AcuC. Fyra nukleotidmolekyler kan passa in i varje AcuB‑dimer. Forskarna observerade hur dessa fickor är fodrade med positivt laddade aminosyror som interagerar olika med AMP, ADP, ATP eller Ap4A. Datorsimuleringar visade att när AMP är bundet tenderar AcuB att anta en kompakt konformation som är väl anpassad för att omfamna och blockera AcuC. Däremot, när ATP eller ADP binder, skiftar proteinet mot mer utsträckta eller flexibla former som försvagar greppet om AcuC och tillåter deacetylaset att fungera.
En inbyggd säkerhetsmekanism för bränsleproduktion
Genom att sammanföra dessa fynd föreslår författarna att AcuB är en energisensor som avläser balansen mellan AMP och ATP inne i cellen. När energin är låg stiger AMP‑nivåerna. AcuB binder AMP, klämmer fast AcuC och förhindrar att det återaktiverar AcsA. Som en följd förblir AcsA acetylerat och inaktivt, och cellen undviker att satsa dyrbar energi på att tillverka mer acetyl‑CoA än den har råd med. När energin är riklig och ATP dominerar släpper AcuB AcuC, vilket då tar bort acetyltaggar från AcsA och tillåter att acetat omvandlas till acetyl‑CoA och driver biosyntes.
Varför detta är viktigt bortom en enda bakterie
Detta arbete identifierar AcuB som den länge sökta länken som samordnar två motsatta acetatvägar med cellens energitillstånd. Genom att koppla det kemiska ”energitalet” till enzymaktivitet via reversibla protein–protein‑interaktioner och konformationsförändringar säkerställer bakterier effektiv resursanvändning och undviker motstridiga metaboliska flöden. Upptäckten antyder också att liknande energiavkännande brytare kan vara utbredda, och att stressignaler som Ap4A kan finjustera denna kontroll och hjälpa mikrober att klara hårda förhållanden.
Citering: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
Nyckelord: bakteriell metabolism, energiavkänning, acetyl‑CoA, proteinacetylering, allosterisk reglering