Clear Sky Science · de
AcuB erkennt die zelluläre Energieladung, um die Acetyl‑CoA‑Synthese bei Bakterien zu koordinieren
Wie Bakterien entscheiden, wann sie Zelltreibstoff herstellen
Bakterien leben in ständig wechselnden Umgebungen, in denen Nahrungs‑ und Energieangebote von Überfluss bis Mangel schwanken können. Um zu überleben, müssen sie ein zentrales Brennstoffmolekül namens Acetyl‑CoA sorgfältig verwalten, das viele lebenswichtige Prozesse speist. Diese Studie zeigt, wie ein bakterielles Protein namens AcuB als internes „Energieniveau‑Messgerät“ fungiert und den Zellen hilft zu entscheiden, wann die Acetyl‑CoA‑Produktion ein‑ oder ausgeschaltet wird, damit sie weder Ressourcen verschwenden noch verarmen. 
Eine molekulare Schalttafel für die Nutzung von Acetat
Die Arbeit konzentriert sich auf den Bodenkeim Bacillus subtilis und seine Verwandten, die das einfache Molekül Acetat sowohl als Abfallprodukt als auch als Nährstoff nutzen können. Ein Enzym, AcsA, wandelt Acetat in Acetyl‑CoA um und fördert so das Wachstum, wenn bevorzugte Zucker wie Glukose knapp sind. Ein anderer Weg, an dem zwei Enzyme namens Pta und Ack beteiligt sind, treibt die Reaktion in die entgegengesetzte Richtung und wandelt Acetyl‑CoA zurück zu Acetat, das aus der Zelle freigesetzt wird. Beide Richtungen gleichzeitig laufen zu lassen wäre verschwenderisch, daher muss die Zelle diese Wege koordinieren. Frühere Studien zeigten, dass AcsA durch das Anheften einer kleinen chemischen Gruppe (einer Acetylgruppe) ausgeschaltet und durch deren Entfernung wieder eingeschaltet werden kann, doch wie diese beiden entgegenwirkenden Schritte koordiniert werden, war unbekannt.
Die verborgene Rolle von AcuB enthüllt
Direkt neben dem acsA‑Gen liegt ein Gencluster aus drei Genen, das sogenannte acu‑Operon, das die Proteine AcuA, AcuB und AcuC kodiert. AcuA fügt AcsA die Acetylmarke hinzu und inaktiviert es, während AcuC die Marke entfernt und das Enzym reaktiviert. Die Rolle von AcuB war bislang rätselhaft. In dieser Studie stellten die Autoren AcuB‑Proteine aus mehreren Bakterienarten im Labor her und analysierten ihr Verhalten. Sie entdeckten, dass AcuB natürlicherweise kleine energieübertragende Moleküle — AMP, ADP und ATP — sowie ein Stresssignal‑Molekül namens Ap4A bindet. Biochemische Tests zeigten, dass AcuB, wenn es mit AMP beladen ist, stark an AcuC bindet und dessen Deacetylase‑Aktivität unterdrückt, wodurch AcsA nicht reaktiviert werden kann. 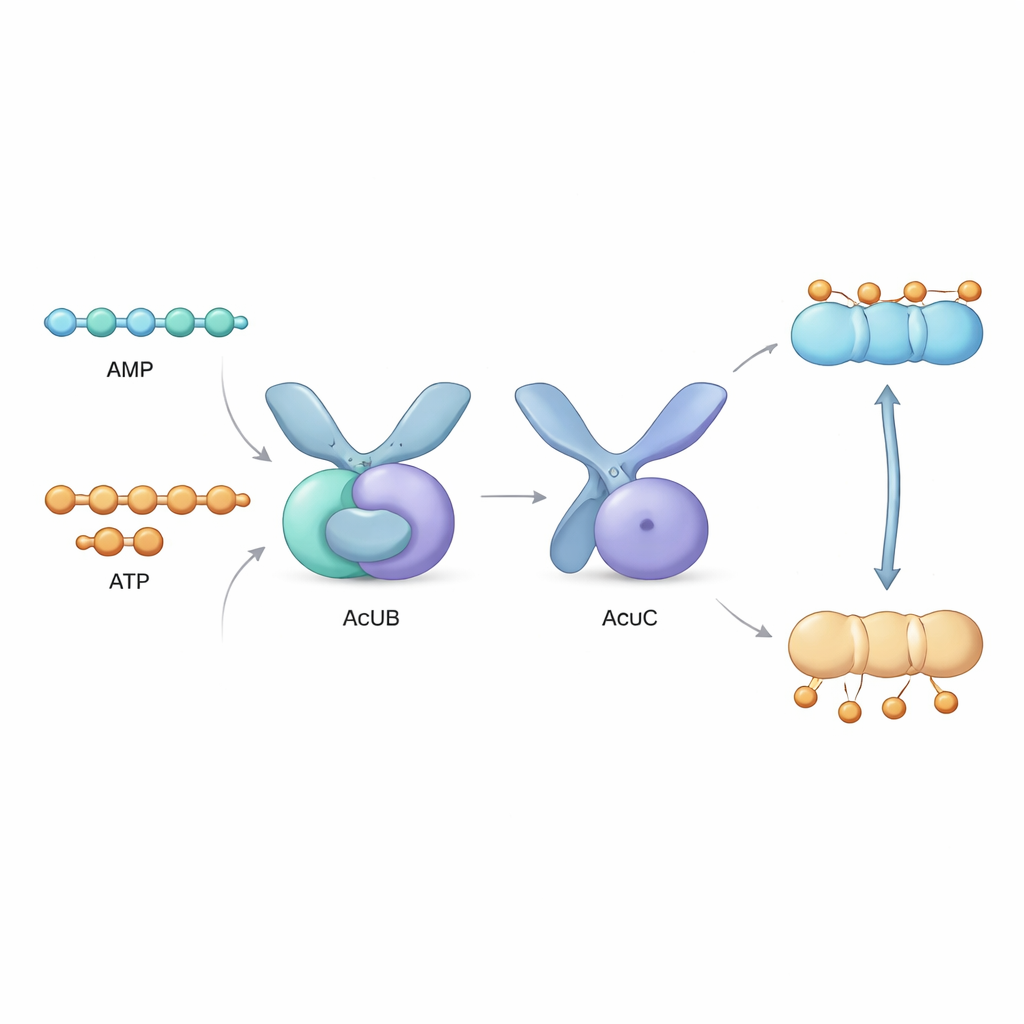
Energieablesung durch formveränderliche Proteine
Um zu verstehen, wie das auf atomarer Ebene funktioniert, löste das Team mittels Röntgenkristallographie die dreidimensionalen Strukturen von AcuB aus zwei Bakterien. AcuB bildet ein scherenartiges Paar von Proteinuntereinheiten, von denen jede einen doppelten Taschen‑„Sensor“ besitzt, der adeninhaltige Nukleotide bindet, sowie einen „Griff“, der Kontakt zu AcuC herstellt. Vier Nukleotidmoleküle können in jedem AcuB‑Dimer Platz finden. Die Forscher beobachteten, wie diese Taschen mit positiv geladenen Aminosäuren ausgekleidet sind, die unterschiedlich mit AMP, ADP, ATP oder Ap4A interagieren. Computersimulationen zeigten, dass AcuB bei AMP‑Bindung dazu neigt, eine kompakte Konformation einzunehmen, die gut geeignet ist, AcuC zu umschließen und zu blockieren. Im Gegensatz dazu verschiebt sich das Protein bei ATP‑ oder ADP‑Bindung zu weiter ausgedehnteren oder flexibleren Formen, die seinen Griff an AcuC abschwächen und der Deacetylase ihre Funktion erlauben.
Ein eingebauter Sicherheitsmechanismus für die Treibstoffproduktion
Ausgehend von diesen Ergebnissen schlagen die Autoren vor, dass AcuB ein Energiesensor ist, der das Verhältnis von AMP zu ATP in der Zelle abliest. Ist die Energie niedrig, steigen die AMP‑Spiegel. AcuB bindet AMP, klemmt sich an AcuC und verhindert so dessen Reaktivierung von AcsA. Infolgedessen bleibt AcsA acetylisiert und inaktiv, und die Zelle vermeidet es, kostbare Energie für die Herstellung von mehr Acetyl‑CoA als nötig aufzuwenden. Ist Energie reichlich vorhanden und dominiert ATP, löst AcuB AcuC, das dann Acetylgruppen von AcsA entfernt, sodass Acetat in Acetyl‑CoA umgewandelt wird und die Biosynthese befeuert.
Warum das über ein Bakterium hinaus wichtig ist
Diese Arbeit identifiziert AcuB als die längst gesuchte Verbindung, die zwei gegenläufige Acetatwege mit dem Energiezustand der Zelle verknüpft. Indem die chemische „Energieladung“ über reversible Protein‑Protein‑Interaktionen und Konformationsänderungen an die Enzymaktivität gekoppelt wird, stellen Bakterien eine effiziente Nutzung der Ressourcen sicher und vermeiden widersprüchliche Stoffflussrichtungen. Die Entdeckung deutet außerdem darauf hin, dass ähnliche Energieschalter weit verbreitet sein könnten und dass Stresssignale wie Ap4A diese Kontrolle feinabstimmen können, um Mikroben bei der Bewältigung harscher Bedingungen zu helfen.
Zitation: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
Schlüsselwörter: bakterieller Stoffwechsel, Energiesensorik, Acetyl‑CoA, Proteinacetylierung, allosterische Regulation