Clear Sky Science · pl
AcuB wyczuwa ładunek energetyczny komórki, koordynując syntezę acetyl-CoA u bakterii
Jak bakterie decydują, kiedy wytwarzać paliwo komórkowe
Bakterie żyją w warunkach ciągłych zmian, gdzie dostępność pożywienia i energii może wahać się od obfitości po głód. Aby przetrwać, muszą starannie zarządzać centralną cząsteczką paliwową — acetyl-CoA — która zasila wiele istotnych procesów. Badanie to ujawnia, jak białko bakteryjne o nazwie AcuB działa jak wewnętrzny „miernik energii”, pomagając komórkom zdecydować, kiedy włączać lub wyłączać produkcję acetyl-CoA, tak by nie marnować zasobów ani nie dopuścić do wygłodzenia. 
Molekularna centrala do wykorzystania acetatu
Praca koncentruje się na bakterii glebowej Bacillus subtilis i jej krewniakach, które potrafią wykorzystywać prostą cząsteczkę acetatu zarówno jako produkt odpadowy, jak i jako źródło pokarmu. Jedne enzym, AcsA, przekształca acetat w acetyl-CoA, wspierając wzrost, gdy preferowane cukry, takie jak glukoza, są rzadkie. Inna droga, obejmująca dwa enzymy Pta i Ack, prowadzi w przeciwnym kierunku, przekształcając acetyl-CoA z powrotem w acetat i uwalniając go z komórki. Jednoczesne działanie obu kierunków byłoby marnotrawne, więc komórka musi skoordynować te ścieżki. Wcześniejsze badania wykazały, że AcsA może być wyłączany przez przyłączenie małej grupy chemicznej (grupy acetylowej) i ponownie włączany po jej usunięciu, ale nie było wiadomo, jak koordynowane są te przeciwstawne kroki.
Odkryta ukryta rola AcuB
Tuż obok genu acsA znajduje się klaster trzech genów, zwany operonem acu, kodujący białka AcuA, AcuB i AcuC. AcuA przyłącza grupę acetylową do AcsA, inaktywując go, podczas gdy AcuC usuwa tę grupę i reaktywuje enzym. Rola AcuB pozostawała tajemnicą. W tym badaniu autorzy wytworzyli białka AcuB z kilku gatunków bakterii w laboratorium i przeanalizowali ich zachowanie. Odkryli, że AcuB naturalnie wiąże małe nośniki energii — AMP, ADP i ATP — oraz cząsteczkę sygnałową stresu o nazwie Ap4A. Za pomocą testów biochemicznych wykazali, że gdy AcuB jest obładowany AMP, silnie wiąże się z AcuC i wyłącza jego aktywność deacetylazy, zapobiegając reaktywacji AcsA. 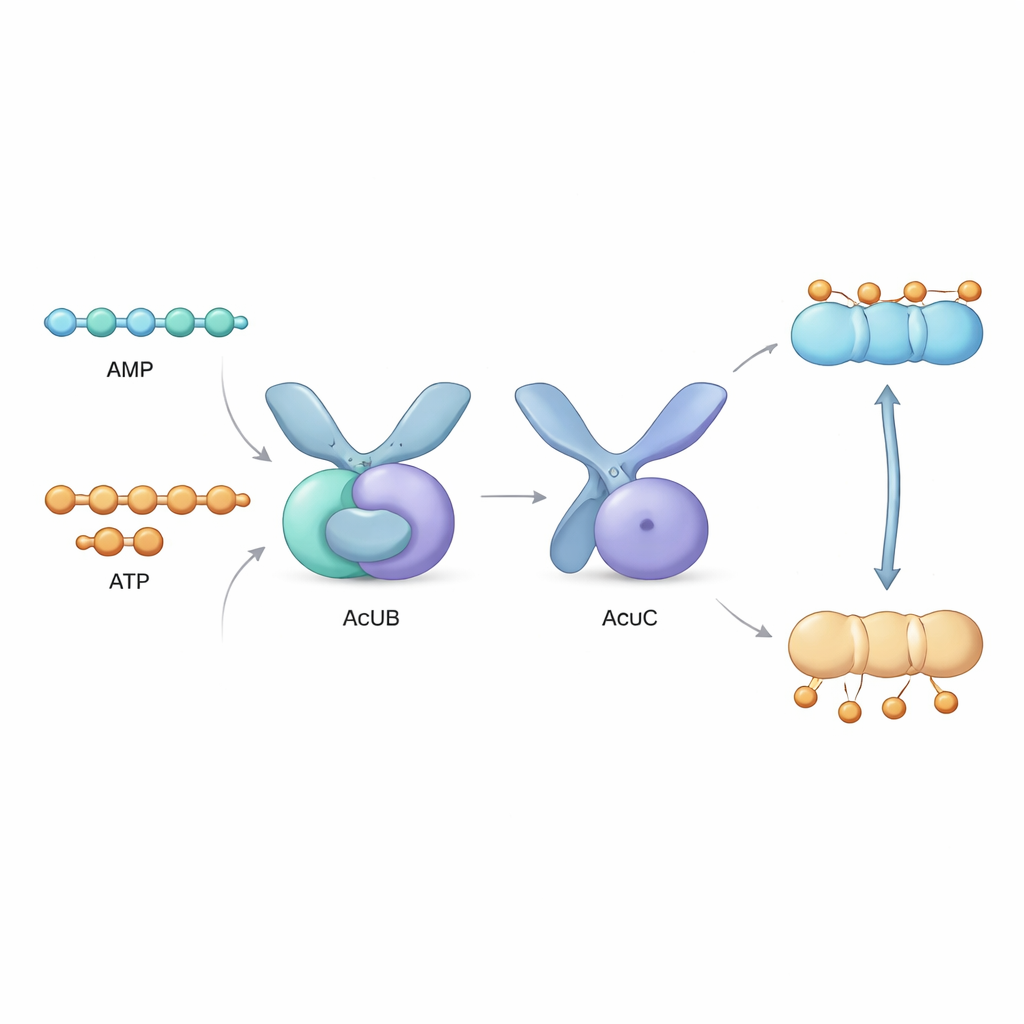
Czytanie energii przez białka zmieniające kształt
Aby zobaczyć, jak to działa na poziomie atomowym, zespół użył krystalografii rentgenowskiej, by rozwiązać trójwymiarowe struktury AcuB z dwóch bakterii. AcuB tworzy nożycową parę jednostek białkowych, z każdą zawierającą bliźniacze „kieszonki-sensor” wiążące nukleotydy adenozynowe oraz sekcję „uchwytu”, która kontaktuje się z AcuC. Do każdego dimera AcuB może włożyć się cztery cząsteczki nukleotydu. Badacze zaobserwowali, że te kieszonki są wyścielone dodatnio naładowanymi aminokwasami, które wchodzą w różny sposób w interakcje z AMP, ADP, ATP czy Ap4A. Symulacje komputerowe pokazały, że po związaniu AMP AcuB ma tendencję do przyjmowania zwartej konformacji, dobrze nadającej się do obejmowania i blokowania AcuC. Natomiast przy związaniu ATP lub ADP białko przesuwa się ku bardziej rozciągniętym lub elastycznym kształtom, które osłabiają jego uchwyt na AcuC i pozwalają deacetylazie funkcjonować.
Wbudowany mechanizm bezpieczeństwa dla produkcji paliwa
Składając te ustalenia razem, autorzy proponują, że AcuB jest sensorem energii, który odczytuje równowagę między AMP a ATP w komórce. Gdy energia jest niska, rośnie poziom AMP. AcuB wiąże AMP, zaciska się na AcuC i uniemożliwia mu reaktywację AcsA. W rezultacie AcsA pozostaje acetylowany i nieaktywny, a komórka unika angażowania cennej energii w produkcję więcej acetyl-CoA, niż może sobie pozwolić. Gdy energia jest obfita i dominuje ATP, AcuB uwalnia AcuC, który następnie usuwa grupy acetylowe z AcsA, umożliwiając przekształcenie acetatu w acetyl-CoA i zasilenie biosyntezy.
Dlaczego to ma znaczenie poza jedną bakterią
Praca ta identyfikuje AcuB jako długo poszukiwany łącznik, który koordynuje dwie przeciwstawne ścieżki wykorzystania acetatu z stanem energetycznym komórki. Poprzez sprzężenie chemicznego „ładunku energetycznego” z aktywnością enzymów za pośrednictwem odwracalnych interakcji białko–białko i zmian konformacyjnych, bakterie zapewniają efektywne wykorzystanie zasobów i unikają konfliktów metabolicznych. Odkrycie sugeruje także, że podobne przełączniki wyczuwające energię mogą być powszechne, a sygnały stresowe takie jak Ap4A mogą precyzować tę kontrolę, pomagając mikrobom radzić sobie w trudnych warunkach.
Cytowanie: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
Słowa kluczowe: metabolizm bakteryjny, wyczuwanie energii, acetyl-CoA, acetylacja białek, regulacja allosteryczna