Clear Sky Science · it
AcuB percepisce la carica energetica cellulare per coordinare la sintesi di acetil‑CoA nei batteri
Come i batteri decidono quando produrre combustibile cellulare
I batteri vivono in ambienti in continuo cambiamento, dove scorte di cibo ed energia possono oscillare tra abbondanza e scarsità. Per sopravvivere devono gestire con attenzione una molecola centrale di carburante chiamata acetil‑CoA, che alimenta molti processi vitali. Questo studio rivela come una proteina batterica chiamata AcuB funziona da “conta‑energia” interna, aiutando le cellule a decidere quando attivare o disattivare la produzione di acetil‑CoA, evitando così sprechi o fame. 
Un quadro di comando molecolare per l’uso dell’acetato
Il lavoro si concentra sul batterio del suolo Bacillus subtilis e suoi parenti, che possono utilizzare la semplice molecola acetato sia come prodotto di scarto sia come nutriente. Un enzima, AcsA, converte l’acetato in acetil‑CoA, alimentando la crescita quando zuccheri preferiti come il glucosio scarseggiano. Un’altra via, che coinvolge due enzimi chiamati Pta e Ack, spinge la reazione nel senso opposto, trasformando l’acetil‑CoA nuovamente in acetato ed espellendolo dalla cellula. Far funzionare entrambe le direzioni contemporaneamente sarebbe uno spreco, quindi la cellula deve coordinare questi percorsi. Studi precedenti avevano mostrato che AcsA può essere disattivata mediante l’aggiunta di un piccolo gruppo chimico (un gruppo acetile) e riattivata quando tale gruppo viene rimosso, ma non si sapeva come fossero coordinate queste due azioni opposte.
Il ruolo nascosto di AcuB rivelato
Accanto al gene acsA si trova un gruppo di tre geni, detto operone acu, che codifica per le proteine AcuA, AcuB e AcuC. AcuA applica il marchio acetile su AcsA, inattivandolo, mentre AcuC rimuove il marchio e riattiva l’enzima. Il ruolo di AcuB era rimasto misterioso. In questo studio gli autori hanno prodotto in laboratorio proteine AcuB provenienti da diverse specie batteriche e ne hanno analizzato il comportamento. Hanno scoperto che AcuB lega naturalmente piccole molecole trasportatrici di energia—AMP, ADP e ATP—oltre a un segnale di stress chiamato Ap4A. Attraverso test biochimici hanno dimostrato che quando AcuB è caricato con AMP, si lega saldamente ad AcuC e inibisce fortemente la sua attività deacetilasica, impedendo la riattivazione di AcsA. 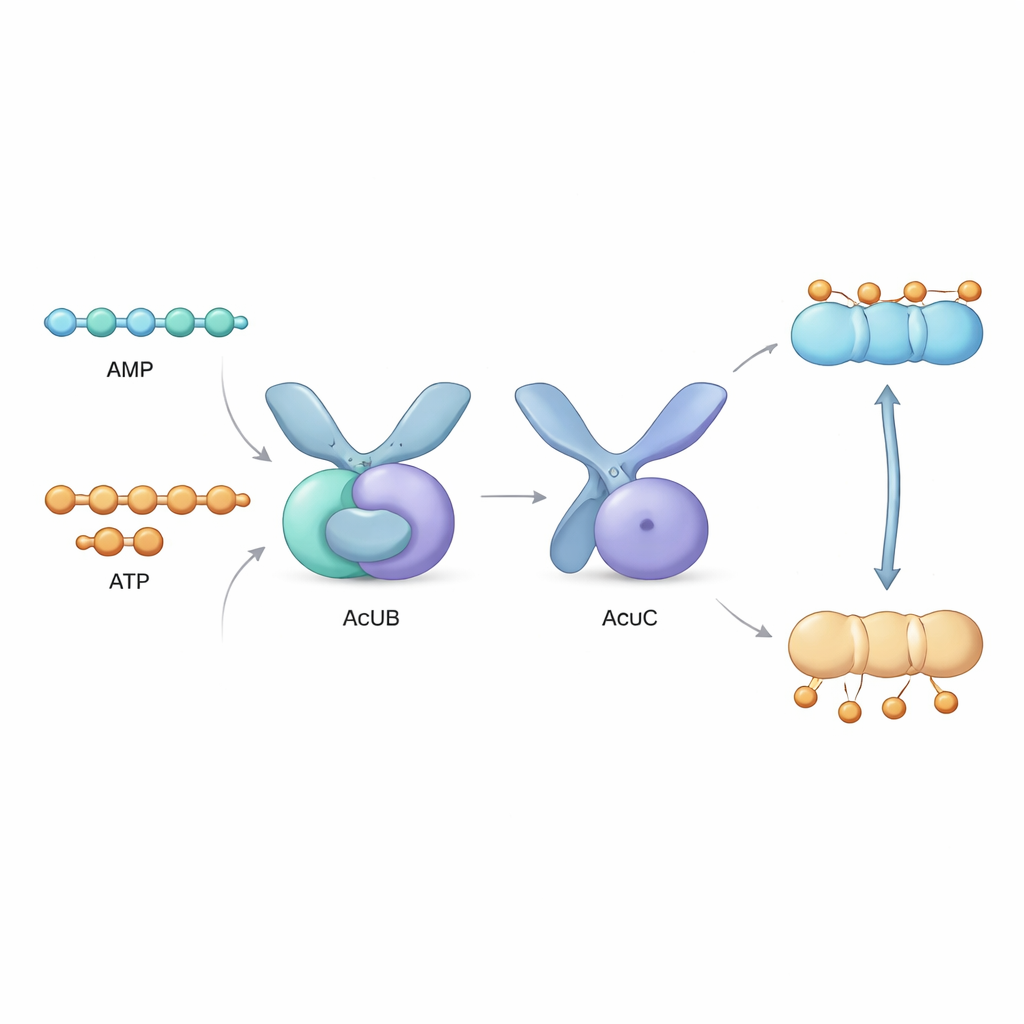
La lettura energetica mediante proteine che cambiano forma
Per capire come ciò avviene a livello atomico, il gruppo ha usato la cristallografia a raggi X per risolvere le strutture tridimensionali di AcuB da due batteri. AcuB forma una coppia a forbice di unità proteiche, ciascuna con una sezione “sensore” a doppia tasca che lega nucleotidi a base adenina e una sezione “manico” che entra in contatto con AcuC. Quattro molecole di nucleotide possono inserirsi in ogni dimero di AcuB. I ricercatori hanno osservato che queste tasche sono rivestite da aminoacidi carichi positivamente che interagiscono in modo diverso con AMP, ADP, ATP o Ap4A. Simulazioni al computer hanno mostrato che quando è legato AMP, AcuB tende ad assumere una conformazione compatta, adatta ad abbracciare e bloccare AcuC. Al contrario, quando si legano ATP o ADP, la proteina si sposta verso forme più estese o flessibili che indeboliscono la presa su AcuC e permettono al deacetilasico di funzionare.
Un meccanismo di sicurezza integrato per la produzione di carburante
Mettendo insieme questi risultati, gli autori propongono che AcuB sia un sensore energetico che legge l’equilibrio tra AMP e ATP all’interno della cellula. Quando l’energia è bassa, i livelli di AMP aumentano. AcuB lega AMP, si ancora ad AcuC e ne impedisce la riattivazione di AcsA. Di conseguenza AcsA rimane acetilato e inattivo, e la cellula evita di impegnare energia preziosa per produrre più acetil‑CoA di quanto possa permettersi. Quando l’energia è abbondante e domina l’ATP, AcuB rilascia AcuC, che quindi rimuove i gruppi acetile da AcsA, permettendo la conversione dell’acetato in acetil‑CoA e alimentando la biosintesi.
Perché questo conta oltre un singolo batterio
Questo studio identifica AcuB come il collegamento a lungo cercato che coordina due vie opposte dell’acetato con lo stato energetico della cellula. Accoppiando la “carica energetica” chimica all’attività enzimatica tramite interazioni proteina‑proteina reversibili e cambiamenti conformazionali, i batteri assicurano un uso efficiente delle risorse ed evitano flussi metabolici contraddittori. La scoperta suggerisce anche che interruttori sensibili all’energia simili potrebbero essere diffusi e che segnali di stress come Ap4A possono affinare questo controllo, aiutando i microrganismi a far fronte a condizioni avverse.
Citazione: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
Parole chiave: metabolismo batterico, rilevamento energetico, acetil‑CoA, acetilazione delle proteine, regolazione allosterica