Clear Sky Science · ar
تتعرف AcuB على شحنة الطاقة الخلوية لتنسيق تصنيع الأسيتيل-CoA في البكتيريا
كيف تقرر البكتيريا متى تصنع وقود الخلية
تعيش البكتيريا في بيئات متغيرة باستمرار، حيث يمكن أن تتقلب إمدادات الغذاء والطاقة بين وفرة ومجاعة. لكي تبقى على قيد الحياة، عليها إدارة جزيء وقود مركزي يسمى أسيتيل‑CoA بعناية، لأنه يغذي العديد من العمليات الحيوية. تكشف هذه الدراسة كيف يعمل بروتين بكتيري يدعى AcuB كـ«عداد طاقة» داخلي، يساعد الخلايا على تقرير متى تشغل أو توقف إنتاج الأسيتيل‑CoA حتى لا تهدر الموارد أو تجوع. 
لوحة مفاتيح جزيئية لاستخدام الأسيتات
تركز العمل على بكتيريا التربة Bacillus subtilis وأقاربها، التي يمكنها استخدام جزيء بسيط مثل الأسيتات سواء كناتج نفاية أو كمغذٍ. إنزيم واحد، AcsA، يحول الأسيتات إلى أسيتيل‑CoA، مغذيًا النمو عندما تكون السكريات المفضلة مثل الجلوكوز نادرة. مسار آخر، يتضمن إنزيمين يُدعيان Pta وAck، يدفع التفاعل في الاتجاه المعاكس، محولًا الأسيتيل‑CoA مرة أخرى إلى أسيتات ومطلقيه من الخلية. تشغيل كلا الاتجاهين في آن واحد سيكون تبذيرًا، لذا يجب على الخلية تنسيق هذه المسارات. أظهرت دراسات سابقة أن AcsA يمكن تعطيله بوضع وسم كيميائي صغير (مجموعة أسيتيل) ويُعاد تنشيطه عند إزالة هذا الوسم، لكن لم يكن معروفًا كيف يتم تنسيق هذين الخطوتين المتعارضتين.
الدور الخفي لـAcuB يكشف عن نفسه
على الجوار مباشرة من جين acsA يوجد عنقود من ثلاثة جينات، يُسمى أوبيرون acu، يُشفِّر البروتينات AcuA وAcuB وAcuC. يضع AcuA وسم الأسيتيل على AcsA، معطِّلاً إياه، بينما يزيل AcuC الوسم ويُعيد تنشيط الإنزيم. ظل دور AcuB غامضًا. في هذه الدراسة، أنتج المؤلفون بروتينات AcuB من عدة أنواع بكتيرية في المختبر وحللوا سلوكها. اكتشفوا أن AcuB يرتبط طبيعيًا بجزيئات صغيرة حاملة للطاقة — AMP وADP وATP — وكذلك بجزيء إشارة إجهاد يسمى Ap4A. أظهرت الاختبارات الكيميائية الحيوية أنه عندما يُحمَّل AcuB بالـAMP، يرتبط بقوة بـAcuC ويوقف نشاطه كمزيل للأسيتيل، مانعًا إعادة تنشيط AcsA. 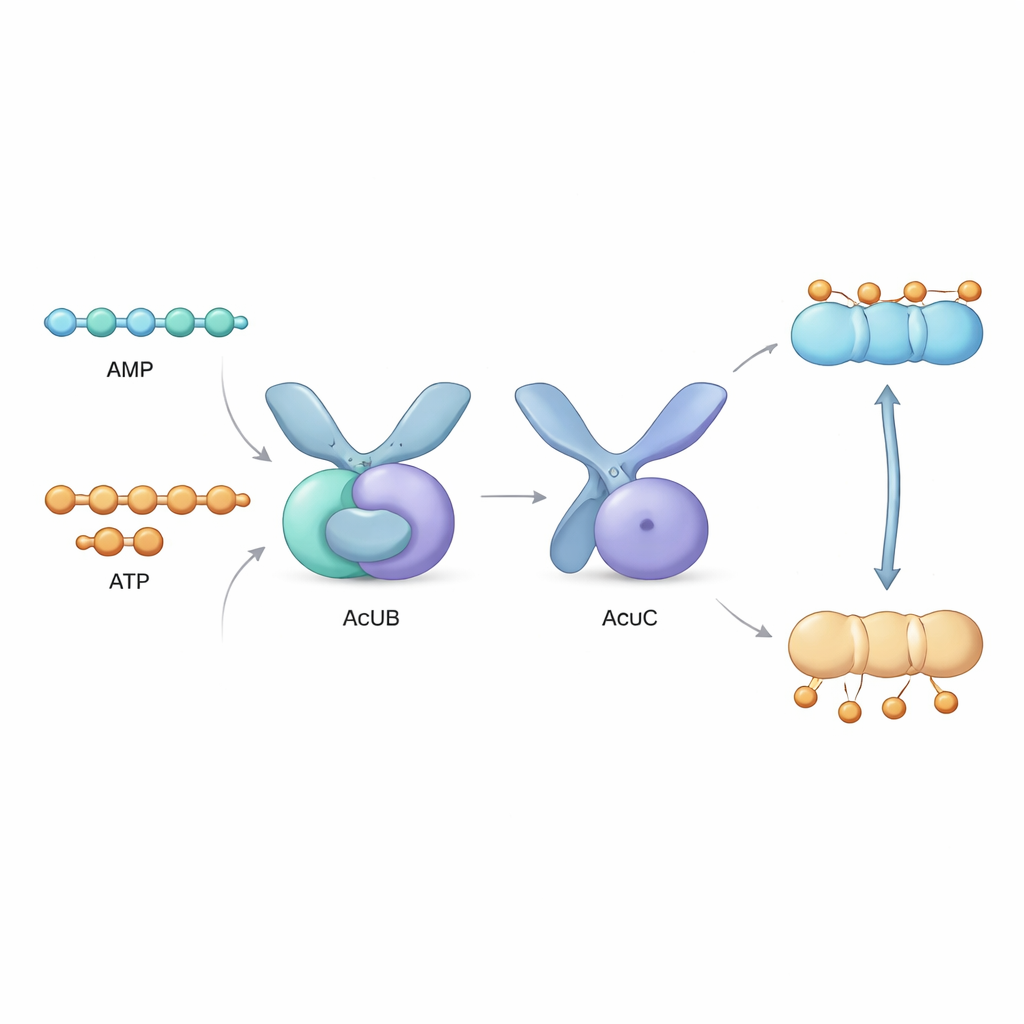
قراءة الطاقة عبر بروتينات متغيرة الشكل
لمعرفة كيفية عمل ذلك على المستوى الذري، استخدم الفريق البلورة بالأشعة السينية لحل البنى الثلاثية الأبعاد لـAcuB من بكتيريتين. يتشكل AcuB كثنائي يشبه المقص، كل وحدة منه تحتوي على قسم «مستشعر» ذو جيبتين توأمتين يربط النيوكليوتيدات المبنية على الأدينين وقسم «مقبض» يتصل بـAcuC. يمكن أن يستوعب كل ديمر من AcuB أربعة جزيئات نيوكليوتيد. لاحظ الباحثون كيف تبطن هذه الجيوب أحماض أمينية موجبة الشحنة تتفاعل بشكل مختلف مع AMP وADP وATP أو Ap4A. أظهرت المحاكاة الحاسوبية أنه عند ارتباط AMP، يميل AcuB إلى اعتماد شكل مدمج يناسب احتضان وإغلاق AcuC. بالمقابل، عندما يرتبط ATP أو ADP، يتحول البروتين نحو أشكال أكثر ممدودة أو مرنة تضعف قبضته على AcuC وتسمح لميزة إزالة الأسيتيل بالعمل.
آلية أمان مدمجة لإنتاج الوقود
بجمع هذه النتائج، يقترح المؤلفون أن AcuB هو جهاز استشعار للطاقة يقرأ التوازن بين AMP وATP داخل الخلية. عندما تكون الطاقة منخفضة، ترتفع مستويات AMP. يرتبط AcuB بالـAMP، ويقبض على AcuC، ويمنعه من إعادة تنشيط AcsA. نتيجة لذلك، يبقى AcsA ممتصلاً وغير نشط، وتتجنب الخلية إنفاق طاقة ثمينة على صنع أسيتيل‑CoA أكثر مما تتحمل. عندما تكون الطاقة وفيرة ويسود ATP، يحرر AcuB AcuC، الذي يزيل وسوم الأسيتيل من AcsA، ما يسمح بتحويل الأسيتات إلى أسيتيل‑CoA وتغذية التخليق الحيوي.
لماذا يهم هذا الأمر خارج بكتيريا واحدة
تحدد هذه الدراسة AcuB كالصلة الطويلة البحث التي تنسق بين مسارين متعاكسين للأسيتات وحالة الطاقة في الخلية. من خلال ربط «شحنة الطاقة» الكيميائية بنشاط الإنزيم عبر تفاعلات بروتين‑بروتين قابلة للانعكاس وتغيرات شكلية، تضمن البكتيريا استخدام الموارد بكفاءة وتتفادى تضارب التدفقات الأيضية. كما يوحي الاكتشاف بأن مفاتيح استشعار الطاقة المماثلة قد تكون منتشرة على نطاق واسع، وأن إشارات الإجهاد مثل Ap4A يمكن أن تضبط هذا التنظيم بدقة، مما يساعد الميكروبات على التكيف مع ظروف قاسية.
الاستشهاد: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
الكلمات المفتاحية: الأيض البكتيري, استشعار الطاقة, أسيتيل-CoA, أسيتلة البروتين, تنظيم كلوستيري