Clear Sky Science · tr
AcuB, hücresel enerji yükünü algılayarak bakterilerde asetil-CoA sentezini koordine eder
Bakteriler Hücresel Yakıtı Ne Zaman Üreteceklerine Nasıl Karar Verir?
Bakteriler, yiyecek ve enerji kaynaklarının bolluktan kıtlığa hızla değişebildiği sürekli değişen ortamlarda yaşar. Hayatta kalmak için, birçok hayati sürece yakıt sağlayan merkezî bir molekül olan asetil-CoA’yı dikkatle yönetmek zorundadırlar. Bu çalışma, AcuB adlı bakteriyel bir proteinin içsel bir “enerji ölçeği” gibi davranarak hücrelerin asetil‑CoA üretimini açıp kapatmaya ne zaman karar vereceğini sağlamasına yardımcı olduğunu ortaya koyuyor; böylece kaynakların israf edilmesi veya hücrelerin aç kalması engelleniyor. 
Asetat Kullanımı İçin Moleküler Bir Anahtar Kartı
Araştırma, atık ürün olarak da besin olarak da basit molekül asetatı kullanabilen toprak bakterisi Bacillus subtilis ve akrabaları üzerinde yoğunlaşıyor. AcsA adlı bir enzim asetatı asetil‑CoA’ya dönüştürür ve tercih edilen şekerler (örneğin glukoz) kıt olduğunda büyümeyi besler. Diğer yönde çalışan bir yol ise Pta ve Ack adlı iki enzim aracılığıyla reaksiyonu tersine çevirir; asetil‑CoA’yı tekrar asetata dönüştürüp hücre dışına salar. Her iki yönde aynı anda çalışmak israf olur, bu yüzden hücre bu yolları koordine etmelidir. Önceki çalışmalar AcsA’nın küçük bir kimyasal etiket (asetil grubu) bağlanarak kapatılabildiğini ve bu etiketin kaldırılmasıyla yeniden etkinleştirilebildiğini göstermişti, ancak bu iki karşıt adımın nasıl koordine edildiği bilinmiyordu.
AcuB’nin Gizli Rolü Ortaya Çıkıyor
AcsA geninin hemen yanında, AcuA, AcuB ve AcuC adlı proteinleri kodlayan üç genlikli bir küme bulunur; buna acu operonu denir. AcuA, AcsA’ya asetil etiketini koyarak onu inaktive ederken AcuC etiketi kaldırıp enzimi yeniden etkinleştirir. AcuB’nin rolü ise gizemini koruyordu. Bu çalışmada yazarlar laboratuvarda çeşitli bakteri türlerinden AcuB proteinleri ürettiler ve davranışlarını analiz ettiler. AcuB’nin doğal olarak AMP, ADP ve ATP gibi küçük enerji taşıyan moleküllere ve ayrıca Ap4A adlı bir stres sinyali molekülüne bağlandığını keşfettiler. Biyokimyasal testlerle gösterdiler ki AcuB AMP ile yüklendiğinde AcuC’ye güçlü biçimde bağlanıyor ve onun deasetilaz aktivitesini kapatıyor; böylece AcsA’nın yeniden etkinleşmesi engelleniyor. 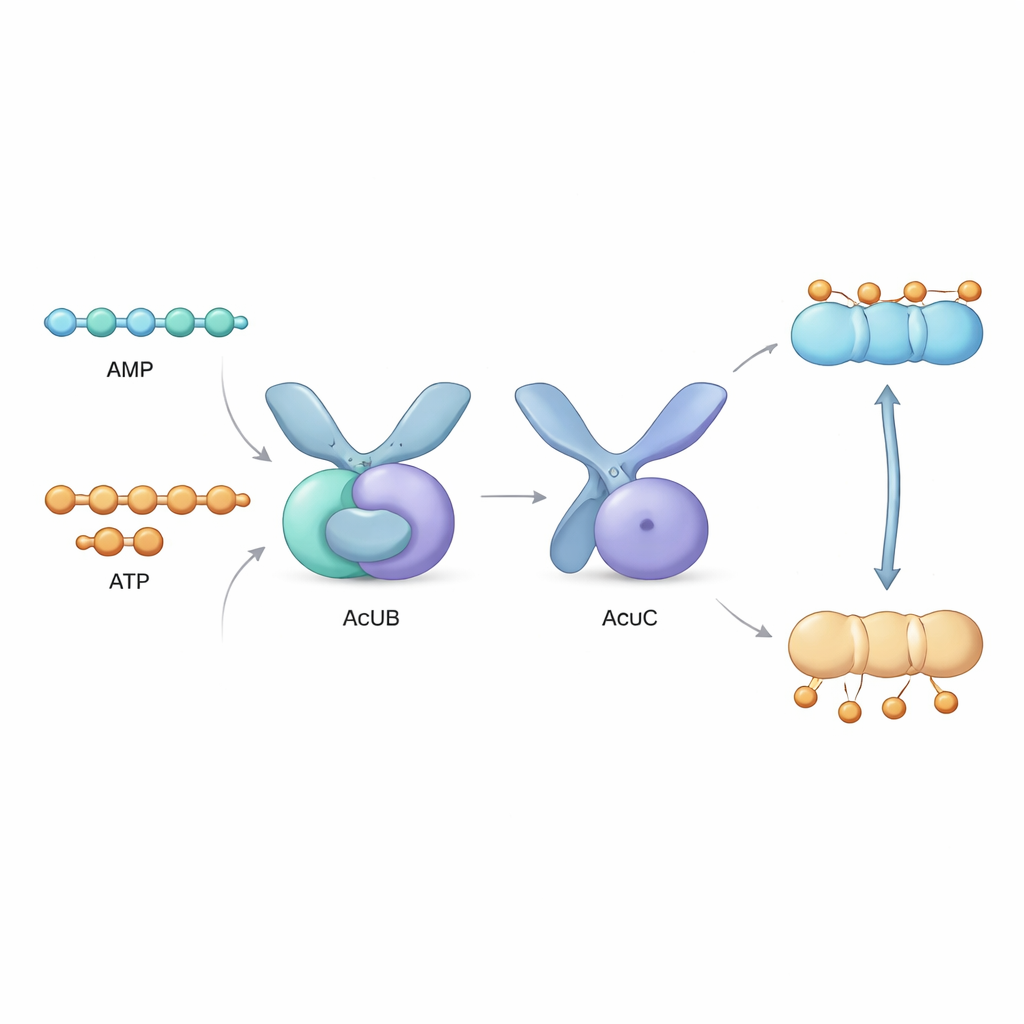
Şekil Değiştiren Proteinlerle Enerji Okuma
Bunun atomik düzeyde nasıl çalıştığını görmek için ekip, iki bakteriden elde ettikleri AcuB’nin üç boyutlu yapılarını X‑ray kristalografisiyle çözdü. AcuB, makas benzeri bir çift protein birimi oluşturuyor; her bir birimde adenine dayalı nükleotidleri bağlayan ikiz cepli bir “sensör” bölümü ve AcuC ile temas kuran bir “sap” bölümü bulunuyor. Her AcuB dimerine dört nükleotid molekülü yerleşebiliyor. Araştırmacılar, bu ceplerin AMP, ADP, ATP veya Ap4A ile farklı biçimlerde etkileşen pozitif yüklü amino asitlerle döşeli olduğunu gözlemledi. Bilgisayar simülasyonları, AMP bağlandığında AcuB’nin AcuC’yi kavrayıp bloke etmeye uygun, kompakt bir konformasyona eğilim gösterdiğini; buna karşın ATP veya ADP bağlandığında proteinin daha açık veya esnek şekillere kayıp AcuC üzerindeki kavramasının zayıfladığını ve deasetilazın işlev görmesine izin verdiğini gösterdi.
Yakıt Üretimi İçin Yerleşik Bir Güvenlik Mekanizması
Bu bulguları bir araya getiren yazarlar, AcuB’nin hücre içindeki AMP ile ATP dengesi arasını okuyan bir enerji sensörü olduğunu öne sürüyor. Enerji düşük olduğunda AMP seviyeleri yükselir. AcuB AMP’ye bağlanır, AcuC’ye sıkıca kenetlenir ve AcuC’nin AcsA’yı yeniden etkinleştirmesini engeller. Sonuç olarak AcsA asetillidir ve inaktiftir; hücre, karşılayamayacağı kadar fazla asetil‑CoA üretmeye kıymetli enerjiyi harcamamış olur. Enerji bol ve ATP baskın olduğunda AcuB, AcuC’yi serbest bırakır; AcuC daha sonra AcsA’daki asetil etiketlerini kaldırır ve asetatın asetil‑CoA’ya dönüşmesine, böylece biyosenteze yakıt sağlanmasına izin verilir.
Bu Keşfin Bir Bakterinin Ötesinde Önemi
Bu çalışma, iki zıt asetat yolunu hücrenin enerji durumu ile koordine eden uzun zamandır aranan bağlantı olarak AcuB’yi tanımlıyor. Kimyasal “enerji yükünü” tersinir protein–protein etkileşimleri ve konformasyonel değişiklikler aracılığıyla enzim aktivitesine bağlayarak bakteriler kaynakları verimli kullanıyor ve çatışan metabolik akışlardan kaçınıyor. Bu keşif ayrıca benzer enerji algılayıcı anahtarların yaygın olabileceğini ve Ap4A gibi stres sinyallerinin bu kontrolü ince ayar yaparak mikroorganizmaların zorlu koşullarla başa çıkmasına yardımcı olabileceğini düşündürüyor.
Atıf: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
Anahtar kelimeler: bakteriyel metabolizma, enerji algılama, asetil-CoA, protein asetilasyonu, allosterik düzenleme