Clear Sky Science · es
AcuB detecta la carga energética celular para coordinar la síntesis de acetil-CoA en bacterias
Cómo deciden las bacterias cuándo producir combustible celular
Las bacterias viven en entornos en constante cambio, donde el suministro de alimento y energía puede oscilar entre la abundancia y la escasez. Para sobrevivir, deben gestionar con cuidado una molécula central de combustible llamada acetil-CoA, que alimenta muchos procesos vitales. Este estudio desvela cómo una proteína bacteriana llamada AcuB actúa como un “medidor de energía” interno, ayudando a las células a decidir cuándo activar o desactivar la producción de acetil-CoA para que no malgasten recursos ni se queden sin energía. 
Un interruptor molecular para el uso del acetato
El trabajo se centra en la bacteria del suelo Bacillus subtilis y sus parientes, que pueden usar la molécula simple acetato tanto como residuo como nutriente. Una enzima, AcsA, convierte el acetato en acetil-CoA, alimentando el crecimiento cuando los azúcares preferidos como la glucosa escasean. Otra vía, que involucra dos enzimas llamadas Pta y Ack, empuja la reacción en sentido contrario, convirtiendo acetil-CoA de nuevo en acetato y liberándolo de la célula. Ejecutar ambas direcciones a la vez sería derrochador, por lo que la célula debe coordinar estas rutas. Estudios previos mostraron que AcsA puede desactivarse mediante la unión de una pequeña etiqueta química (un grupo acetilo) y reactivarse cuando esa etiqueta se elimina, pero no se sabía cómo se coordinaban esos dos pasos opuestos.
Se revela el papel oculto de AcuB
Junto al gen acsA se encuentra un conjunto de tres genes, llamado operón acu, que codifica las proteínas AcuA, AcuB y AcuC. AcuA coloca la etiqueta acetilo sobre AcsA, inactivándola, mientras que AcuC elimina la etiqueta y reactiva la enzima. El papel de AcuB había permanecido misterioso. En este estudio, los autores produjeron proteínas AcuB de varias especies bacterianas en el laboratorio y analizaron su comportamiento. Descubrieron que AcuB se une de forma natural a pequeñas moléculas transportadoras de energía—AMP, ADP y ATP—así como a una molécula señal de estrés llamada Ap4A. Mediante ensayos bioquímicos, mostraron que cuando AcuB está cargada con AMP, se une fuertemente a AcuC y apaga su actividad desacetilasica, impidiendo que AcsA vuelva a activarse. 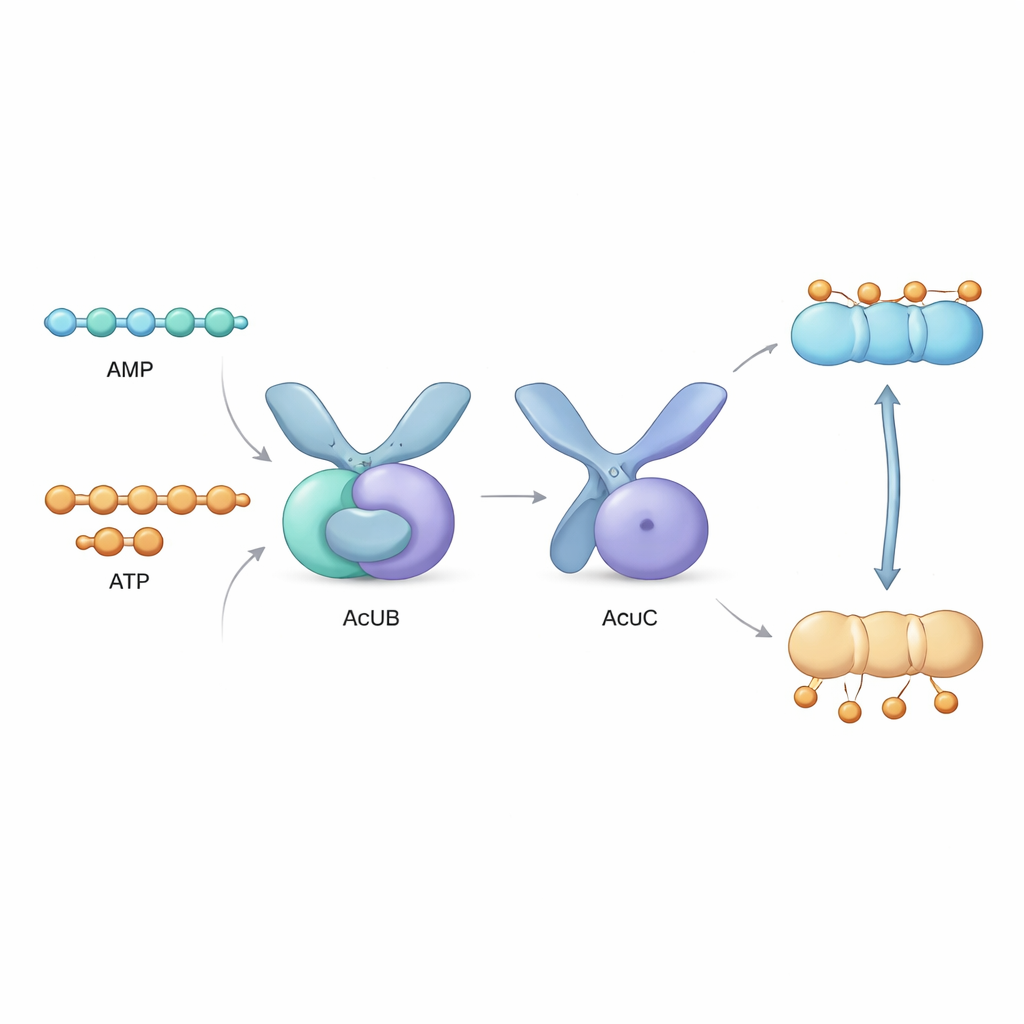
Lectura de energía por proteínas que cambian de forma
Para ver cómo funciona esto a nivel atómico, el equipo utilizó cristalografía de rayos X para resolver las estructuras tridimensionales de AcuB de dos bacterias. AcuB forma un par de unidades proteicas con forma de tijera, cada una con una sección “sensor” de doble bolsillo que une nucleótidos basados en adenina y una sección “mango” que contacta con AcuC. Cuatro moléculas de nucleótido pueden encajarse en cada dímero de AcuB. Los investigadores observaron cómo estos bolsillos están revestidos por aminoácidos cargados positivamente que interactúan de forma distinta con AMP, ADP, ATP o Ap4A. Simulaciones por ordenador mostraron que cuando se une AMP, AcuB tiende a adoptar una conformación compacta que es adecuada para abrazar y bloquear AcuC. En contraste, cuando se unen ATP o ADP, la proteína cambia hacia formas más extendidas o flexibles que debilitan su agarre sobre AcuC y permiten que la desacetilasa funcione.
Un mecanismo de seguridad incorporado para la producción de combustible
Integrando estos hallazgos, los autores proponen que AcuB es un sensor de energía que lee el equilibrio entre AMP y ATP en el interior de la célula. Cuando la energía es baja, los niveles de AMP aumentan. AcuB se une a AMP, se aferra a AcuC y evita que reactive a AcsA. Como resultado, AcsA permanece acetilada e inactiva, y la célula evita comprometer energía preciosa en producir más acetil-CoA de la que puede permitirse. Cuando la energía es abundante y el ATP domina, AcuB libera a AcuC, que entonces elimina las etiquetas acetilo de AcsA, permitiendo que el acetato se convierta en acetil-CoA y alimente la biosíntesis.
Por qué esto importa más allá de una sola bacteria
Este trabajo identifica a AcuB como el eslabón largamente buscado que coordina dos vías opuestas del acetato con el estado energético de la célula. Al acoplar la “carga energética” química a la actividad enzimática mediante interacciones reversibles proteína–proteína y cambios conformacionales, las bacterias aseguran un uso eficiente de los recursos y evitan flujos metabólicos conflictivos. El descubrimiento también sugiere que interruptores sensores de energía similares pueden ser generalizados, y que señales de estrés como Ap4A pueden afinar este control, ayudando a los microbios a enfrentar condiciones adversas.
Cita: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
Palabras clave: metabolismo bacteriano, detección de energía, acetil-CoA, acetilación de proteínas, regulación alostérica