Clear Sky Science · nl
AcuB voelt de cellulaire energielading om acetyl‑CoA‑synthese in bacteriën te coördineren
Hoe bacteriën beslissen wanneer ze cellaire brandstof maken
Bacteriën leven in voortdurend veranderende omgevingen, waar voedsel- en energieaanvoer kan schommelen tussen overvloed en schaarste. Om te overleven moeten ze zorgvuldig omgaan met een centraal brandstofmolecuul, acetyl‑CoA, dat veel vitale processen voedt. Deze studie onthult hoe een bacterieel eiwit genaamd AcuB fungeert als een interne “energiemeter” die cellen helpt te beslissen wanneer de productie van acetyl‑CoA aan- of uitgezet moet worden, zodat ze noch hulpbronnen verspillen noch verhongeren. 
Een moleculair schakelpaneel voor acetaatgebruik
Het werk richt zich op de bodembacterie Bacillus subtilis en verwanten, die het eenvoudige molecuul acetaat zowel als afvalproduct als als voedingsstof kunnen gebruiken. Eén enzym, AcsA, zet acetaat om in acetyl‑CoA en voedt de groei wanneer voorkeurssuikers zoals glucose schaars zijn. Een andere route, via twee enzymen genaamd Pta en Ack, duwt de reactie de andere kant op en zet acetyl‑CoA terug in acetaat en geeft het vrij uit de cel. Beide richtingen tegelijk laten lopen zou verspilling zijn, dus de cel moet deze routes coördineren. Eerdere studies toonden aan dat AcsA uitgeschakeld kan worden door een klein chemisch label (een acetylgroep) eraan te koppelen en weer ingeschakeld kan worden wanneer dat label wordt verwijderd, maar hoe die tegengestelde stappen op elkaar afgestemd worden was niet bekend.
De verborgen rol van AcuB onthuld
Direct naast het acsA‑gen ligt een cluster van drie genen, het zogeheten acu‑operon, dat de eiwitten AcuA, AcuB en AcuC codeert. AcuA plaatst het acetyl‑label op AcsA en inactiveert het, terwijl AcuC het label verwijdert en het enzym heractiveert. De rol van AcuB was onduidelijk gebleven. In deze studie maakten de auteurs AcuB‑eiwitten van meerdere bacteriesoorten in het lab en analyseerden hun gedrag. Ze ontdekten dat AcuB van nature kleine energiedragende moleculen bindt—AMP, ADP en ATP—en ook een stresssignaalmolecuul genaamd Ap4A. Met biochemische tests lieten ze zien dat wanneer AcuB AMP gebonden heeft, het sterk aan AcuC bindt en diens deacetylase‑activiteit uitschakelt, waardoor AcsA niet kan worden heractiveerd. 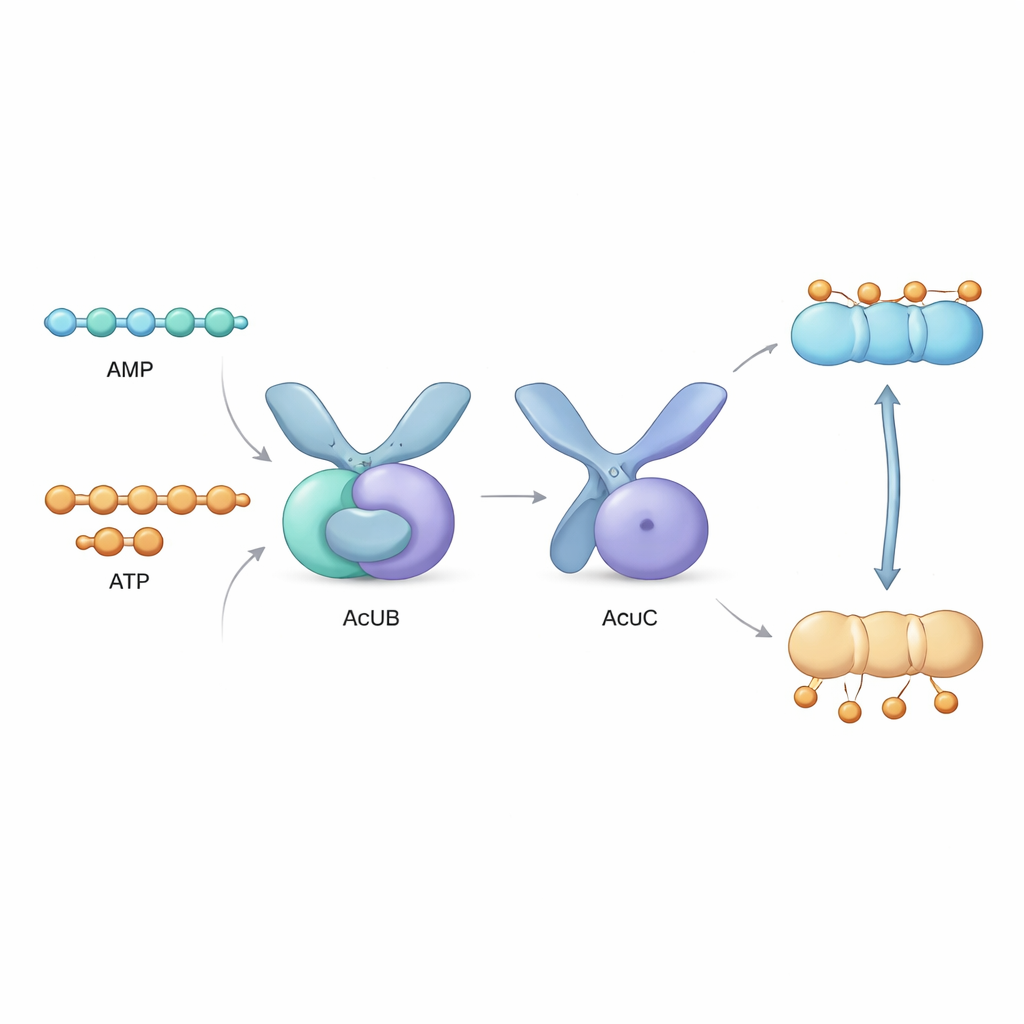
Energie aflezen door vormveranderende eiwitten
Om te zien hoe dit op atomair niveau werkt, gebruikte het team röntgendiffractie om de driedimensionale structuren van AcuB van twee bacteriën op te lossen. AcuB vormt een schaarachtige dimer van eiwiteenheden, elk met een dubbel‑pocket “sensor”‑deel dat adenine‑nucleotiden bindt en een “handvat”‑deel dat contact maakt met AcuC. Vier nucleotidemoleculen kunnen in elke AcuB‑dimeer passen. De onderzoekers zagen dat deze pockets zijn bekleed met positief geladen aminozuren die verschillend interageren met AMP, ADP, ATP of Ap4A. Computersimulaties toonden aan dat wanneer AMP gebonden is, AcuB de neiging heeft een compacte conformatie aan te nemen die goed geschikt is om AcuC te omarmen en te blokkeren. Daarentegen verschuift het eiwit bij binding van ATP of ADP naar meer uitgerekte of flexibele vormen die zijn greep op AcuC verzwakken en de deacetylase activiteit toelaten.
Een ingebouwde veiligheidsmechanisme voor brandstofproductie
Samenvattend stellen de auteurs dat AcuB een energiesensor is die de balans tussen AMP en ATP in de cel afleest. Wanneer de energievoorraad laag is, stijgt het AMP‑niveau. AcuB bindt AMP, klemt zich vast aan AcuC en verhindert dat AcuC AcsA heractiveert. Hierdoor blijft AcsA geacetyleerd en inactief, en voorkomt de cel dat ze kostbare energie inzet om meer acetyl‑CoA te maken dan ze zich kan veroorloven. Wanneer energie overvloedig is en ATP domineert, laat AcuB AcuC los; AcuC verwijdert dan de acetyllabels van AcsA, waardoor acetaat omgezet kan worden in acetyl‑CoA en de biosynthese wordt gevoed.
Waarom dit belangrijk is buiten één bacterie
Dit werk identificeert AcuB als de langgezochte schakel die twee tegengestelde acetaatroutes koppelt aan de energiestatus van de cel. Door de chemische “energielading” te koppelen aan enzymactiviteit via omkeerbare eiwit‑eiwitinteracties en conformationele veranderingen, zorgen bacteriën voor efficiënt gebruik van hulpbronnen en vermijden ze conflicterende metabole stromen. De ontdekking suggereert ook dat vergelijkbare energie‑sensorische schakelaars wijdverspreid kunnen zijn, en dat stresssignalen zoals Ap4A deze regeling fijn kunnen afstemmen, waardoor microben beter bestand zijn tegen zware omstandigheden.
Bronvermelding: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
Trefwoorden: bacteriële stofwisseling, energiesensing, acetyl‑CoA, proteïneacetylatie, allosterische regulatie