Clear Sky Science · ru
AcuB ощущает энергообеспеченность клетки, координируя синтез ацетил‑CoA у бактерий
Как бактерии решают, когда производить клеточное «топливо»
Бактерии живут в постоянно меняющихся условиях, где запасы пищи и энергии колеблются от изобилия до голода. Чтобы выжить, им нужно тщательно управлять центральной топливной молекулой — ацетил‑CoA, которая питает многие жизненно важные процессы. В этом исследовании показано, как белок бактерий под названием AcuB действует как внутренний «энергетический счётчик», помогая клеткам решать, когда включать или выключать производство ацетил‑CoA, чтобы не тратить ресурсы попусту и не погибнуть от голода. 
Молекулярный распределитель использования ацетата
Работа сосредоточена на почвенной бактерии Bacillus subtilis и её сородичах, которые могут использовать простой молекулу ацетат как отход, так и питательное вещество. Один фермент, AcsA, превращает ацетат в ацетил‑CoA, обеспечивая рост, когда предпочтительные сахара, такие как глюкоза, исчерпаны. Другой путь, включающий два фермента Pta и Ack, движет реакцию в обратном направлении, превращая ацетил‑CoA обратно в ацетат и выделяя его из клетки. Запускать оба направления одновременно было бы пустой тратой, поэтому клетка должна координировать эти пути. Ранние исследования показали, что AcsA можно отключить, присоединив небольшой химический ярлык (ацетильную группу), и вновь включить, когда этот ярлык удаляют, но не было ясно, как согласованы эти противоположные шаги.
Открыта скрытая роль AcuB
Прямо рядом с геном acsA располагается кластер из трёх генов, называемый опероном acu, кодирующий белки AcuA, AcuB и AcuC. AcuA присоединяет ацетильный ярлык к AcsA, инактивируя его, в то время как AcuC удаляет этот ярлык и реактивирует фермент. Роль AcuB оставалась загадкой. В этом исследовании авторы получили белки AcuB из нескольких видов бактерий в лабораторных условиях и проанализировали их поведение. Они обнаружили, что AcuB естественным образом связывается с малыми энергонесущими молекулами — AMP, ADP и ATP — а также с молекулой стрессового сигнала Ap4A. Биохимические тесты показали, что когда AcuB загружен AMP, он сильно связывается с AcuC и подавляет его деацетилазную активность, не позволяя AcsA быть реактивированным. 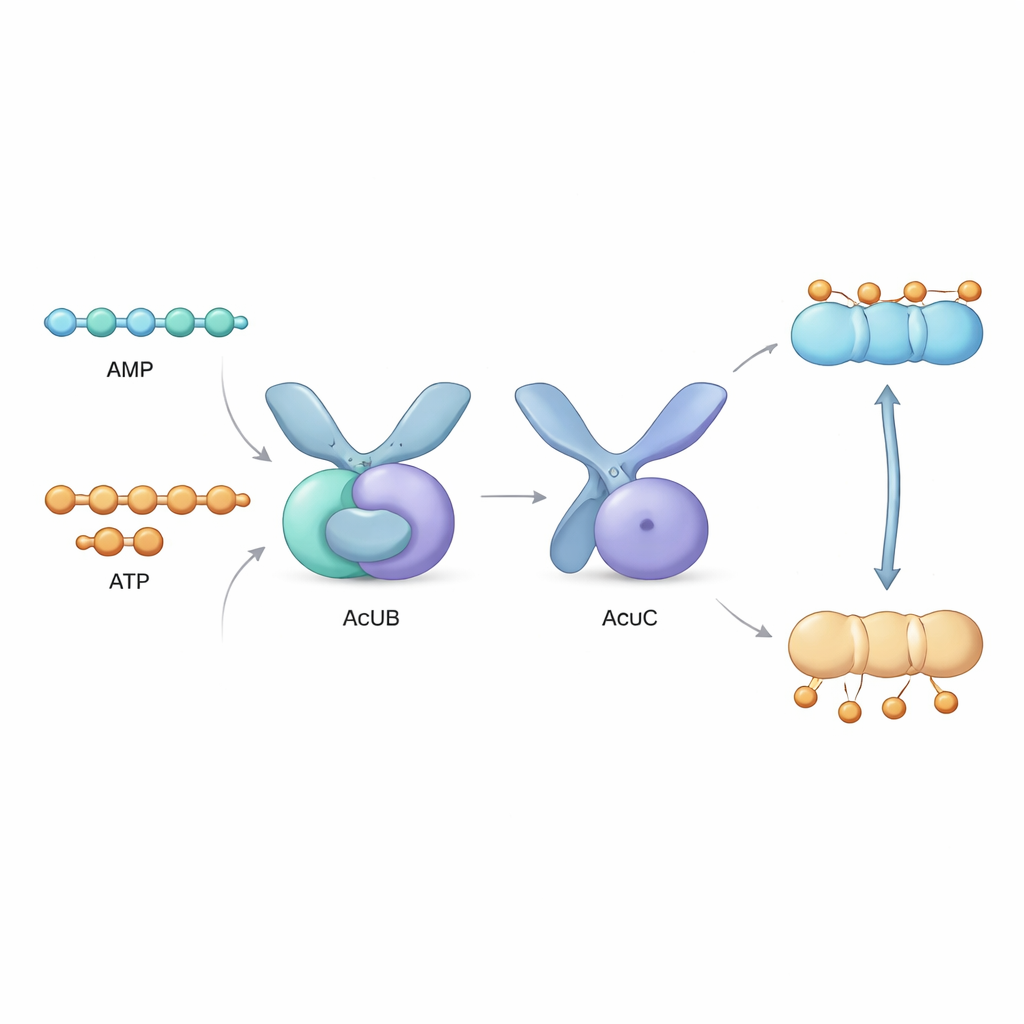
Чтение энергетического состояния через изменение формы белков
Чтобы увидеть, как это работает на атомном уровне, команда использовала рентгеновскую кристаллографию и решила трёхмерные структуры AcuB из двух бактерий. AcuB образует подобие ножниц из двух белковых субъединиц, каждая из которых имеет двойной «карман»‑сенсор, связывающий аденинсодержащие нуклеотиды, и «ручку», контактирующую с AcuC. В каждый димер AcuB могут войти четыре молекулы нуклеотидов. Исследователи заметили, что эти карманы выложены положительно заряженными аминокислотами, которые по‑разному взаимодействуют с AMP, ADP, ATP или Ap4A. Компьютерные моделирования показали, что при связывании AMP AcuB склонен принимать компактную конформацию, благоприятную для обхвата и блокирования AcuC. Напротив, при связывании ATP или ADP белок смещается к более растянутым или гибким формам, ослабляющим его захват AcuC и позволяющим деацетилазе работать.
Встроенный механизм предосторожности для производства топлива
Объединив эти данные, авторы предлагают, что AcuB является сенсором энергии, который считывает соотношение AMP и ATP внутри клетки. Когда энергии мало, уровень AMP растёт. AcuB связывает AMP, захватывает AcuC и препятствует его восстановительной активности по отношению к AcsA. В результате AcsA остаётся ацетилированным и неактивным, и клетка избегает вложения драгоценных энергетических ресурсов в образование большего количества ацетил‑CoA, чем она может себе позволить. Когда энергия в избытке и доминирует ATP, AcuB освобождает AcuC, который затем удаляет ацетильные метки с AcsA, позволяя преобразовывать ацетат в ацетил‑CoA и подпитывать биосинтез.
Почему это важно не только для одной бактерии
Эта работа идентифицирует AcuB как давно искомую связь, которая координирует два противоположных ацетатных пути с энергетическим статусом клетки. Связывая химический «энергетический заряд» с активностью ферментов через обратимо регулируемые белок–белковые взаимодействия и конформационные изменения, бактерии обеспечивают эффективное использование ресурсов и избегают конфликтующих потоков метаболизма. Открытие также намекает, что аналогичные энерго‑сенсорные выключатели могут быть широко распространены, а стрессовые сигналы вроде Ap4A способны тонко настраивать этот контроль, помогая микробам справляться с суровыми условиями.
Цитирование: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
Ключевые слова: бактериальный метаболизм, сенсор энергии, ацетил‑CoA, ацетилирование белков, аллостерическая регуляция