Clear Sky Science · fr
AcuB détecte la charge énergétique cellulaire pour coordonner la synthèse d'acétyl-CoA chez les bactéries
Comment les bactéries décident quand fabriquer du carburant cellulaire
Les bactéries vivent dans des environnements en perpétuel changement, où les apports en nourriture et en énergie peuvent osciller entre abondance et disette. Pour survivre, elles doivent gérer avec soin une molécule centrale de carburant appelée acétyl-CoA, qui alimente de nombreux processus vitaux. Cette étude révèle comment une protéine bactérienne nommée AcuB fonctionne comme un « indicateur d'énergie » interne, aidant les cellules à décider quand activer ou désactiver la production d'acétyl-CoA afin de ne pas gaspiller de ressources ni se priver inutilement. 
Un tableau de commande moléculaire pour l'utilisation de l'acétate
Les travaux se concentrent sur la bactérie du sol Bacillus subtilis et ses apparentées, qui peuvent utiliser la molécule simple acétate à la fois comme déchet et comme nutriment. Une enzyme, AcsA, convertit l'acétate en acétyl-CoA, alimentant la croissance quand les sucres privilégiés comme le glucose se font rares. Une autre voie, impliquant deux enzymes nommées Pta et Ack, pousse la réaction en sens inverse, transformant l'acétyl-CoA en acétate et l'expulsant de la cellule. Faire fonctionner les deux directions simultanément serait gaspilleur, la cellule doit donc coordonner ces voies. Des études antérieures montraient qu'AcsA peut être inactivée par l'ajout d'une petite étiquette chimique (un groupe acétyle) et réactivée lorsque cette étiquette est retirée, mais on ignorait comment ces deux étapes opposées étaient coordonnées.
Le rôle caché d'AcuB révélé
Juste à côté du gène acsA se trouve un groupe de trois gènes, appelé opéron acu, codant pour les protéines AcuA, AcuB et AcuC. AcuA ajoute l'étiquette acétyle sur AcsA, l'inactivant, tandis qu'AcuC retire l'étiquette et réactive l'enzyme. Le rôle d'AcuB était resté mystérieux. Dans cette étude, les auteurs ont produit des protéines AcuB issues de plusieurs espèces bactériennes en laboratoire et analysé leur comportement. Ils ont découvert qu'AcuB se lie naturellement à de petites molécules porteuses d'énergie — AMP, ADP et ATP — ainsi qu'à une molécule de signal de stress appelée Ap4A. Grâce à des tests biochimiques, ils ont montré que lorsque AcuB est chargé d'AMP, il se lie fortement à AcuC et inhibe son activité désacétylase, empêchant la réactivation d'AcsA. 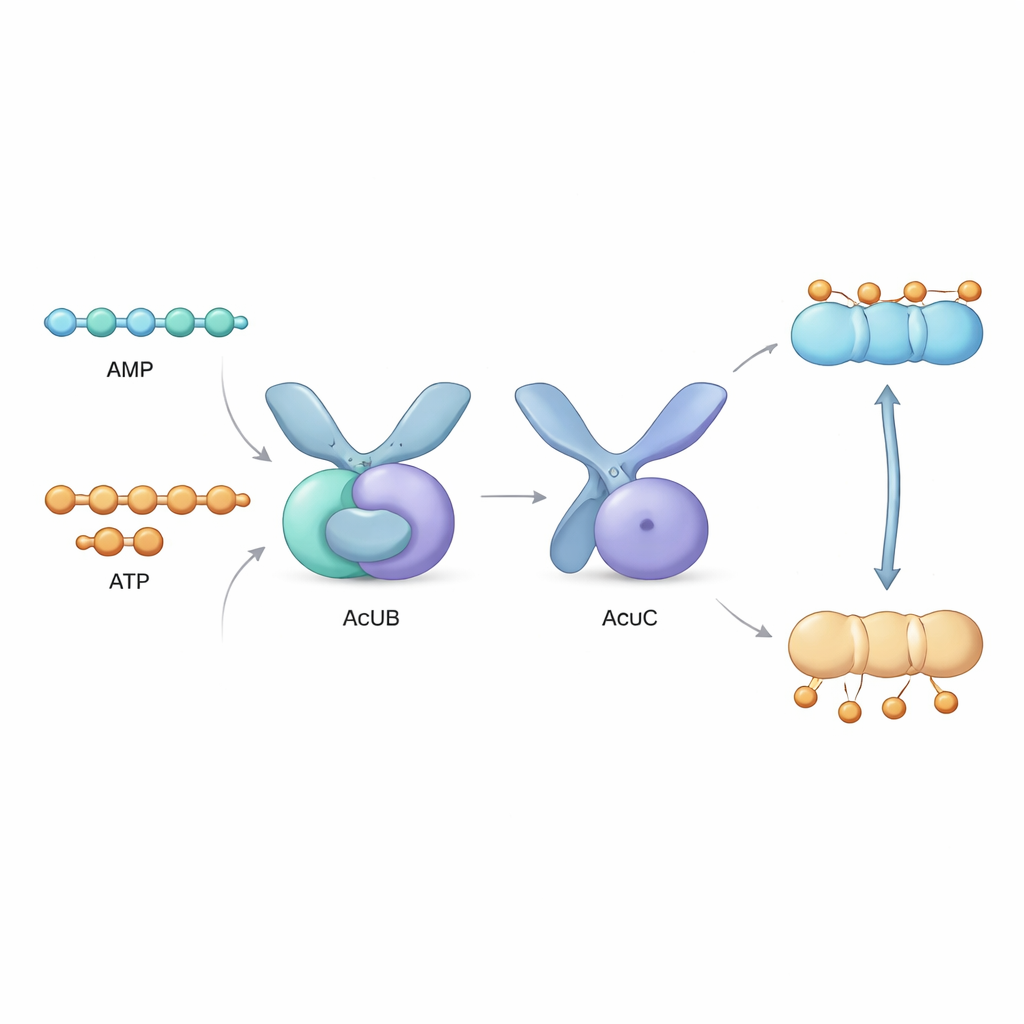
Lecture énergétique par des protéines changeant de forme
Pour comprendre le mécanisme au niveau atomique, l'équipe a utilisé la cristallographie aux rayons X pour résoudre les structures tridimensionnelles d'AcuB provenant de deux bactéries. AcuB se présente sous la forme d'une paire de monomères en ciseaux, chacun comportant une section « capteur » à double poche qui lie des nucléotides à base d'adénine et une section « poignée » qui contacte AcuC. Quatre molécules de nucléotides peuvent se loger dans chaque dimère d'AcuB. Les chercheurs ont observé que ces poches sont bordées d'acides aminés chargés positivement qui interagissent différemment avec AMP, ADP, ATP ou Ap4A. Des simulations informatiques ont montré que lorsque l'AMP est liée, AcuB tend à adopter une conformation compacte bien adaptée pour embrasser et bloquer AcuC. En revanche, lorsque l'ATP ou l'ADP sont liés, la protéine se déplace vers des formes plus étendues ou flexibles qui affaiblissent son emprise sur AcuC et permettent à la désacétylase de fonctionner.
Un mécanisme de sécurité intégré pour la production de carburant
En rassemblant ces résultats, les auteurs proposent qu'AcuB soit un capteur d'énergie qui lit l'équilibre entre AMP et ATP à l'intérieur de la cellule. Lorsque l'énergie est faible, le taux d'AMP augmente. AcuB se lie à l'AMP, s'enclenche sur AcuC et empêche celui-ci de réactiver AcsA. En conséquence, AcsA reste acétylé et inactif, et la cellule évite d'engager une énergie précieuse pour produire plus d'acétyl-CoA qu'elle ne peut se permettre. Lorsque l'énergie est abondante et que l'ATP domine, AcuB relâche AcuC, qui enlève alors les groupes acétyle d'AcsA, permettant la conversion de l'acétate en acétyl-CoA et l'alimentation des processus de biosynthèse.
Pourquoi cela compte au-delà d'une seule bactérie
Ce travail identifie AcuB comme le lien longtemps recherché qui coordonne deux voies d'acétate opposées avec l'état énergétique de la cellule. En couplant la « charge énergétique » chimique à l'activité enzymatique via des interactions protéine–protéine réversibles et des changements conformationnels, les bactéries assurent une utilisation efficace des ressources et évitent des flux métaboliques conflictuels. Cette découverte suggère également que des interrupteurs de détection d'énergie similaires pourraient être répandus, et que des signaux de stress comme Ap4A peuvent affiner ce contrôle, aidant les microbes à faire face à des conditions difficiles.
Citation: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
Mots-clés: métabolisme bactérien, détection d'énergie, acétyl-CoA, acétylation des protéines, régulation allostérique