Clear Sky Science · ja
細菌でアセチルCoA合成を調整するために細胞のエネルギー荷(チャージ)を感知するAcuB
細菌はいつ細胞の燃料を作るかをどう決めるか
細菌は、飢餓と豊富の間を揺れ動く環境で生きており、栄養やエネルギー供給が常に変化します。生き延びるために、彼らはアセチル-CoAという中心的な燃料分子を慎重に管理しなければなりません。アセチル-CoAは多くの重要なプロセスに供給されます。本研究は、AcuBと呼ばれる細菌タンパク質が内部の「エネルギーメーター」として働き、細胞がアセチル-CoAの生成をいつオンにするかオフにするかを決めるのを助け、資源を浪費したり飢えたりするのを防いでいることを明らかにします。 
酢酸の利用のための分子スイッチボード
研究は土壌細菌のBacillus subtilisとその近縁種に焦点を当てており、これらは単純な分子である酢酸を廃棄物としても栄養源としても利用できます。AcsAという酵素は酢酸をアセチル-CoAに変換し、グルコースのような好まれる糖が不足しているときに成長に供給します。別の経路では、PtaとAckという二つの酵素が関与し、反応を逆に進めてアセチル-CoAを酢酸に戻して細胞外に放出します。両方向を同時に走らせるのは無駄なので、細胞はこれらの経路を調整する必要があります。先行研究は、AcsAが小さな化学タグ(アセチル基)の付加で不活性化され、タグが除かれると再活性化されることを示していましたが、これら二つの相反するステップがどのように協調されているかは不明でした。
AcuBの隠れた役割を解明
acsA遺伝子のすぐ隣には、AcuA、AcuB、AcuCをコードする三つの遺伝子のクラスター(acuオペロン)が存在します。AcuAはAcsAにアセチルタグを付けて不活性化し、AcuCはタグを取り除いて酵素を再活性化します。AcuBの役割はこれまで謎に包まれていました。本研究では、著者らは複数の細菌種由来のAcuBタンパク質を実験室で作製し、その振る舞いを解析しました。彼らは、AcuBが自然にAMP、ADP、ATPといった小さなエネルギー担体分子や、Ap4Aというストレスシグナル分子を結合することを発見しました。生化学的検査により、AcuBがAMPを結合しているときにAcuCに強く結合し、AcuCの脱アセチル化活性を抑制してAcsAの再活性化を防ぐことを示しました。 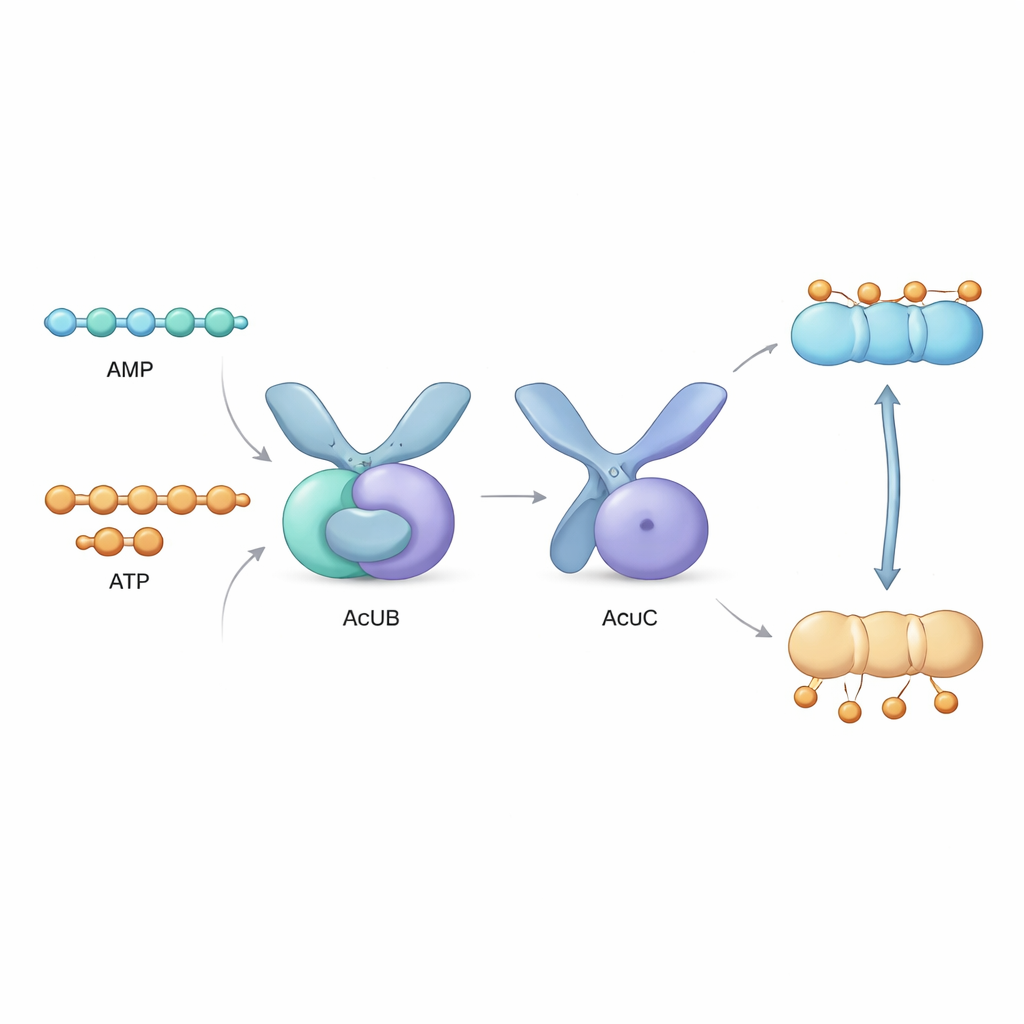
形を変えるタンパク質によるエネルギーの読み取り
この仕組みを原子レベルで見るために、チームはX線結晶構造解析を用いて二種の細菌由来AcuBの三次元構造を解きました。AcuBはハサミ状に対をなすユニットを形成し、それぞれがアデニン系ヌクレオチドを結合する双子ポケットの「センサー」部とAcuCに接触する「ハンドル」部を持ちます。各AcuB二量体には四つのヌクレオチド分子がはまり込みます。研究者たちは、これらのポケットが正に帯電したアミノ酸で裏打ちされており、AMP、ADP、ATP、あるいはAp4Aと異なる相互作用をする様子を観察しました。計算シミュレーションは、AMPが結合するとAcuBがコンパクトな構造を取りやすくなり、AcuCを抱え込んで阻害するのに適した形になることを示しました。対照的にATPやADPが結合すると、タンパク質はより伸びたまたは柔軟な形にシフトし、AcuCへの結びつきが弱まり脱アセチル化酵素が機能できるようになります。
燃料生産のための組み込み型セーフティ機構
これらの知見を総合すると、著者らはAcuBが細胞内のAMPとATPの比率を読み取るエネルギーセンサーであると提案します。エネルギーが乏しいときにはAMP濃度が上昇します。AcuBはAMPを結合してAcuCをしっかりとつかみ、AcuCがAcsAを再活性化するのを防ぎます。その結果、AcsAはアセチル化されたまま不活性となり、細胞は支払える以上のアセチル-CoAを作るために貴重なエネルギーを使うことを避けます。エネルギーが豊富でATPが優勢な場合、AcuBはAcuCを解放し、AcuCはAcsAからアセチル基を除去して酢酸をアセチル-CoAに変換し、合成代謝に燃料を供給します。
一つの細菌を超えて重要な理由
この研究は、酢酸に関する二つの相反する経路を細胞のエネルギー状態と結びつける長らく求められていたリンクとしてAcuBを特定しました。可逆的なタンパク質間相互作用と立体構造変化を通じて化学的な「エネルギーチャージ」を酵素活性に結び付けることで、細菌は資源を効率的に使い、代謝の矛盾を避けます。この発見は、同様のエネルギー感知スイッチが広く存在する可能性を示唆するとともに、Ap4Aのようなストレスシグナルがこの制御を微調整して過酷な条件に対処する助けになることをほのめかしています。
引用: Janetzky, M., Geist, N., Schulze, S. et al. AcuB senses cellular energy charge to coordinate acetyl-CoA synthesis in bacteria. Nat Commun 17, 3815 (2026). https://doi.org/10.1038/s41467-026-71006-w
キーワード: 細菌代謝, エネルギー感知, アセチル-CoA, タンパク質アセチル化, アロステリック制御