Clear Sky Science · zh
可编程纳米胶束重塑髓系免疫以持久控制原发及转移性乳腺癌
帮助免疫系统对抗乳腺癌的新方法
大多数癌症治疗着重直接杀死肿瘤细胞,但许多肿瘤通过悄悄将机体自身的免疫细胞变成“同盟”来幸存。该研究描述了一种微小且可编程的药物,旨在将这些细胞重新转回为抗癌战士,从而对已转移至其他器官的侵袭性乳腺癌实现长期控制。
为何乳腺癌难以治愈
乳腺癌是女性中诊断最常见的癌症,其最致命的特征是易发生转移,尤其是肺转移。三阴性乳腺癌是其中一种特别难治的亚型,因为它缺乏常见的激素受体和生长因子靶点。即便是现代免疫疗法,如阻断肿瘤细胞上PD‑L1“屏障”的疗法,也仅对一部分患者有效,且常常无法延长生存期。一个主要原因是肿瘤微环境——肿瘤周围的细胞与分子组成——充斥着被重新编程为抑制而非支持抗肿瘤反应的免疫细胞。
肿瘤周围辅助细胞的隐性影响
在这些周围细胞中,两类髓系细胞起着关键作用:树突状细胞和巨噬细胞。在健康状态下,树突状细胞担当哨兵,拾取异常分子并将其呈递给T细胞以触发针对性的免疫攻击。巨噬细胞可表现为支持炎症(类M1)并帮助清除威胁,或平息炎症并促进组织修复(类M2)。在患者和小鼠模型的乳腺肿瘤中,作者发现成熟的树突状细胞减少,而类M2的巨噬细胞大量存在。这些“和事佬”巨噬细胞与T细胞浸润减少和不良预后相关,提示如果能将这些细胞重新接线为战斗状态,可能会释放出更强大且持久的抗肿瘤免疫反应。
设计一种智能的多功能纳米药物
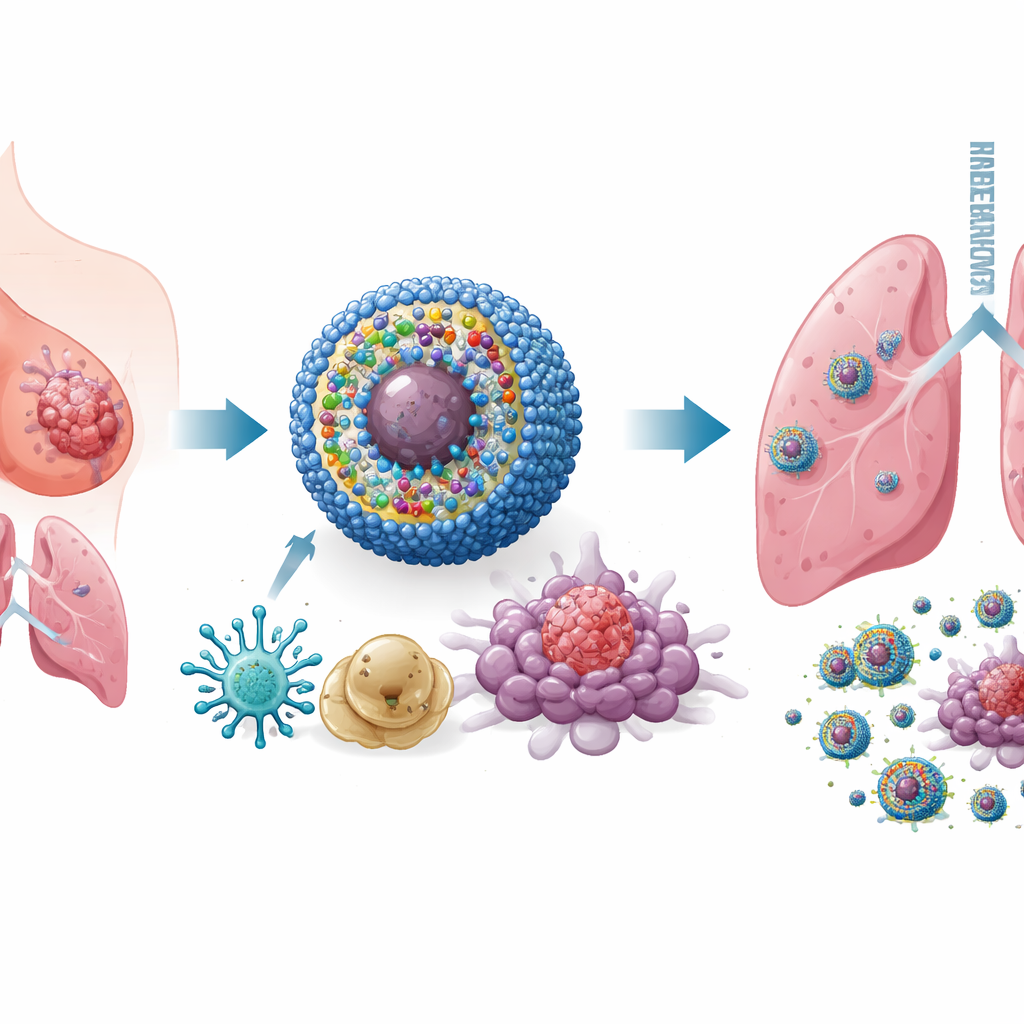
为了解决这一问题,研究人员构建了一种纳米级递送系统,称为IPANP——在血流中循环并在肿瘤处富集的微小球形胶束。每个纳米胶束携带三种成分。其一,是一种光激活染料(IR825),在体外用近红外光照射时产生活性分子,使肿瘤细胞以高度可被免疫识别的方式应激和死亡。其二,是针对PD‑L1的抗体,有助于移除肿瘤用以关闭T细胞的分子刹车。其三,是一段短的遗传材料(antagomiR‑182),可阻断在促肿瘤巨噬细胞中高表达的微小RNA miR‑182。载体对肿瘤内化学活性环境敏感,因此主要在需要的部位释放货物,限制对健康组织的暴露。
将抑制性细胞转变为攻击者
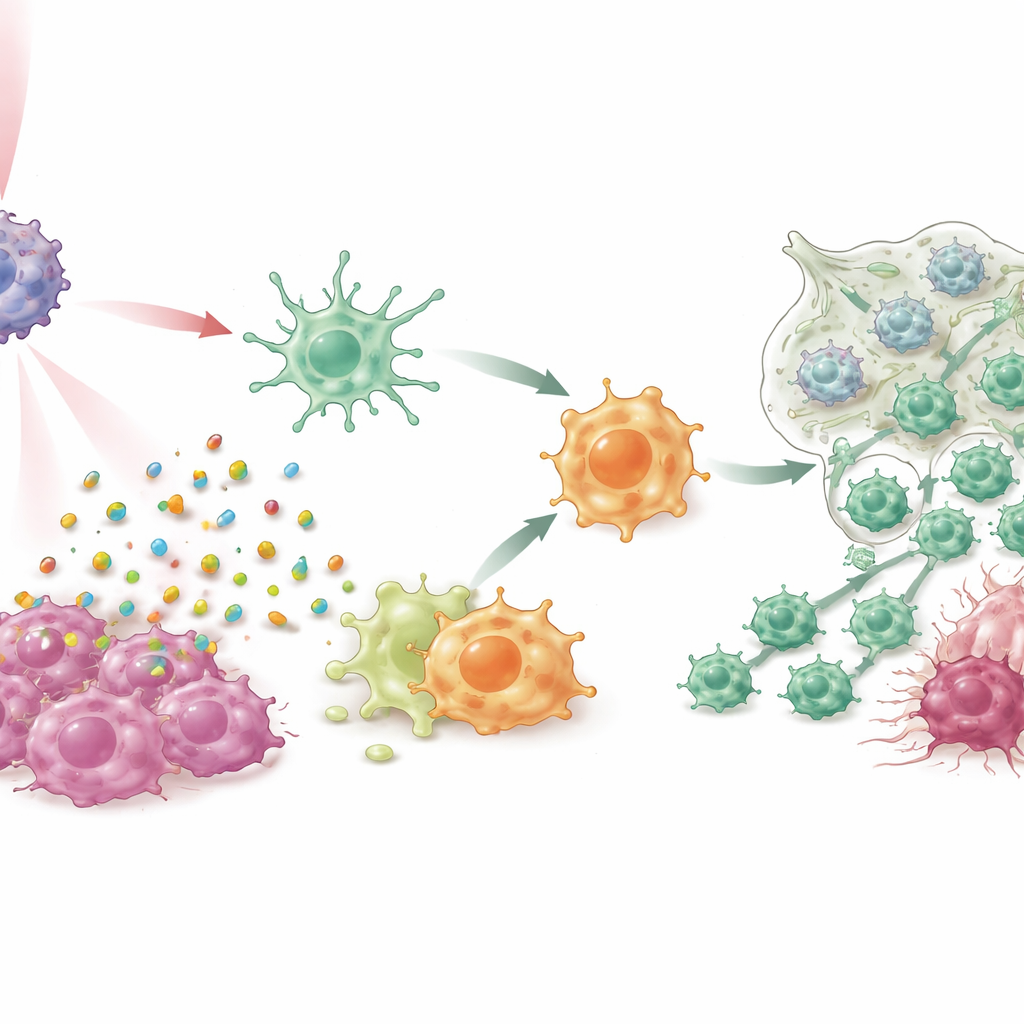
在细胞培养和多种乳腺癌小鼠模型中(包括难治的三阴性和自发性肿瘤模型),IPANP联合温和近红外光不仅仅缩小了肿瘤。光激活染料使癌细胞以“免疫原性”方式死亡,释放危险信号,促使树突状细胞成熟并更高效地将肿瘤碎片呈递给T细胞。与此同时,在巨噬细胞中阻断miR‑182解除对一个关键感应通路(TLR4/MYD88/NF‑κB)的抑制,使其从类M2的促肿瘤状态向类M1的炎性状态转变。随着这两类髓系细胞角色的转变,更多杀伤性T细胞涌入肿瘤、活性增强且较少陷入功能衰竭。结果是对原发肿瘤的强有力控制、肺转移显著减少以及被治疗动物生存期延长。
持久保护与现实应用的迹象
值得注意的是,经IPANP和光处理而清除肿瘤的小鼠,在数月后重新植入新肿瘤时表现出免疫保护,这表明形成了类似疫苗的免疫记忆。研究团队还在刚切除的患者乳腺癌样本(作为小组织块维持活性)和植入人源化小鼠的患者来源肿瘤移植模型中测试了该方法。在这些体系中,该治疗同样促使树突状细胞和巨噬细胞进入更活跃的抗肿瘤状态,降低促生长信号,增加有益的炎性分子,提高杀伤性T细胞的存在并导致肿瘤细胞死亡——同时在长期动物研究中显示出良好的安全性。
对未来癌症治疗的意义
这项工作表明,可通过重新教育肿瘤周围的免疫细胞来治疗侵袭性乳腺癌,而不仅仅是直接攻击肿瘤细胞。通过将光激活疗法、免疫检查点阻断和遗传重编程打包进单一智能纳米胶束,研究人员创造了一个协调的驱动,使抑制性的肿瘤环境转变为支持持久免疫防御的环境。尽管在该策略进入临床之前仍需大量测试,但它为未来通过重塑免疫环境以对原发和转移性肿瘤实现长期控制的治疗方案提供了蓝图。
引用: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
关键词: 乳腺癌免疫治疗, 纳米药物学, 肿瘤微环境, 巨噬细胞重编程, 树突状细胞激活