Clear Sky Science · fr
Nanomicelles programmables réorientent l’immunité myéloïde pour un contrôle durable du cancer du sein primaire et métastatique
Une nouvelle façon d’aider le système immunitaire à combattre le cancer du sein
La plupart des traitements anticancéreux visent à tuer directement les cellules tumorales, mais de nombreuses tumeurs survivent en transformant discrètement les propres cellules immunitaires de l’organisme en alliées. Cette étude décrit un médicament minuscule et programmable qui vise à rebasculer ces cellules pour qu’elles redeviennent des combattantes du cancer, offrant un contrôle durable des cancers du sein agressifs ayant disséminé vers d’autres organes.
Pourquoi le cancer du sein peut être si difficile à guérir
Le cancer du sein est le cancer le plus fréquemment diagnostiqué chez les femmes, et sa caractéristique la plus meurtrière est sa propension à se propager, notamment vers les poumons. Un sous‑type, le cancer du sein triple négatif, est particulièrement difficile à traiter car il manque de cibles hormonales et de facteurs de croissance usuels. Même les immunothérapies modernes qui bloquent le « bouclier » PD‑L1 des cellules tumorales ne bénéficient qu’à une fraction des patientes et échouent souvent à prolonger la survie. Une raison majeure est le microenvironnement tumoral — le voisinage immédiat de cellules et de molécules autour de la tumeur — qui est chargé de cellules immunitaires reprogrammées pour supprimer, plutôt que soutenir, les attaques anti‑tumorales.
L’influence cachée des cellules de soutien autour des tumeurs
Parmi ces cellules environnantes, deux types de cellules myéloïdes jouent un rôle disproportionné : les cellules dendritiques et les macrophages. Dans des conditions saines, les cellules dendritiques agissent comme des sentinelles, captant des molécules suspectes et les présentant aux lymphocytes T pour déclencher une attaque immunitaire ciblée. Les macrophages peuvent soit soutenir l’inflammation (de type M1) et aider à éliminer les menaces, soit calmer la réaction et favoriser la réparation tissulaire (de type M2). Dans les tumeurs mammaires de patientes et les modèles murins, les auteurs ont observé moins de cellules dendritiques matures et une abondance de macrophages de type M2. Ces macrophages « pacificateurs » étaient associés à une faible infiltration des lymphocytes T et à de mauvais résultats, suggérant que si l’on parvient à reprogrammer ces cellules en combattantes, on pourrait libérer des réponses immunitaires antitumorales plus puissantes et durables.
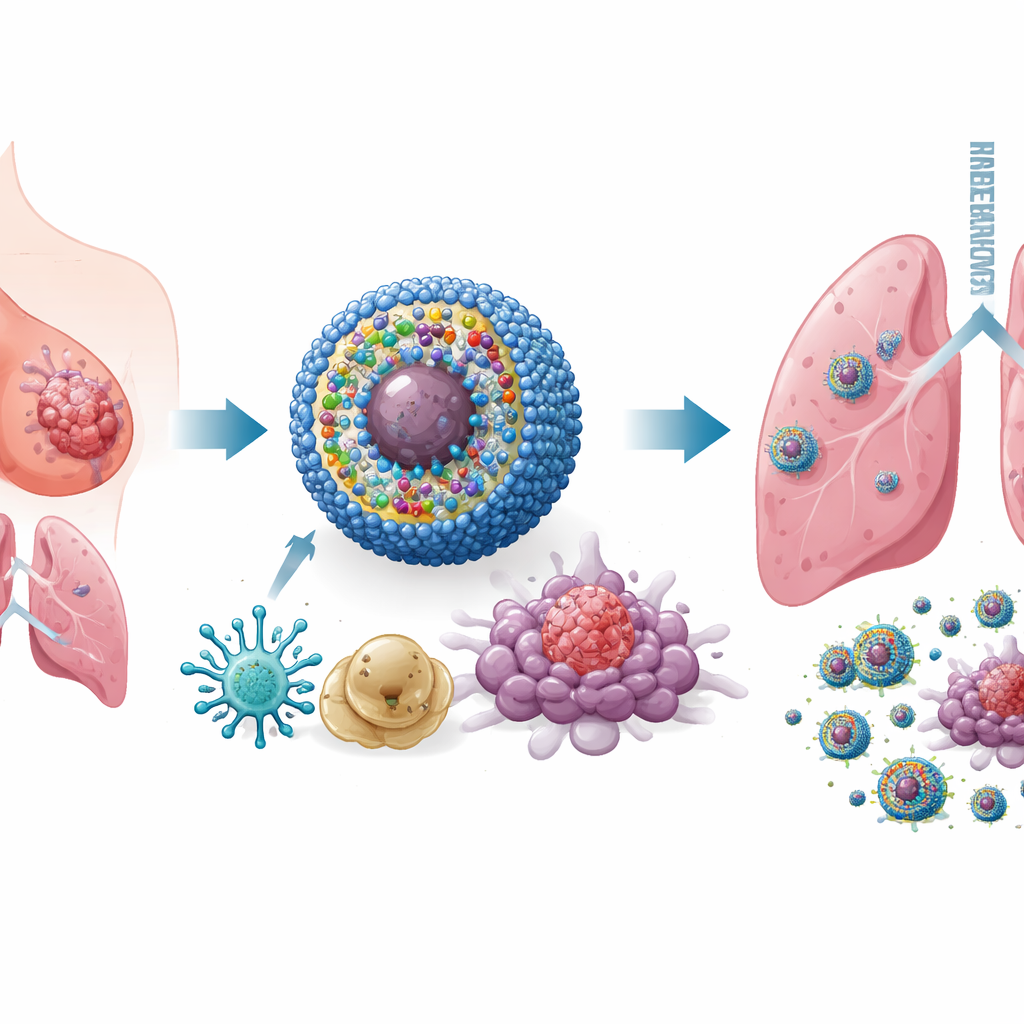
Concevoir une nanomédecine intelligente multi‑outils
Pour relever ce défi, les chercheurs ont construit un système d’administration à l’échelle nanométrique qu’ils appellent IPANP — de petites micelles sphériques qui circulent dans le sang et s’accumulent dans les tumeurs. Chaque nanomicelle transporte trois composants. D’abord, un colorant activable par la lumière (IR825) qui, lorsqu’il est illuminé par une lumière proche infrarouge depuis l’extérieur du corps, génère des espèces réactives stressant et tuant les cellules tumorales d’une manière qui les rend très visibles pour le système immunitaire. Ensuite, un anticorps contre PD‑L1, qui aide à lever un frein moléculaire que les tumeurs utilisent pour désactiver les lymphocytes T. Enfin, un court fragment d’acide nucléique (antagomiR‑182) qui bloque un microARN, miR‑182, présent à des niveaux élevés dans les macrophages promoteurs de tumeur. Le vecteur est sensible à l’environnement chimiquement réactif à l’intérieur des tumeurs, de sorte qu’il libère sa charge principalement là où elle est nécessaire, limitant l’exposition aux tissus sains.
Transformer les cellules suppresseuses en attaquantes
En cultures cellulaires et dans plusieurs modèles murins de cancer du sein, y compris des systèmes difficiles triple négatif et des tumeurs spontanées, IPANP associé à une lumière proche infrarouge douce a fait plus que réduire la taille des tumeurs. Le colorant activé par la lumière a provoqué une mort des cellules cancéreuses de type « immunogénique », libérant des signaux de danger qui ont poussé les cellules dendritiques à mûrir et à présenter plus efficacement des fragments tumoraux aux lymphocytes T. Parallèlement, le blocage de miR‑182 dans les macrophages a levé un frein sur une voie de détection clé (TLR4/MYD88/NF‑κB), les incitant à passer d’un état de soutien tumoral de type M2 à un état inflammatoire de type M1. À mesure que ces deux types cellulaires myéloïdes changeaient de rôle, davantage de lymphocytes T cytotoxiques ont afflué dans les tumeurs, sont devenus plus actifs et ont été moins sujets à l’épuisement. Le résultat a été un contrôle marqué des tumeurs primaires, une réduction nette des métastases pulmonaires et une survie prolongée chez les animaux traités.
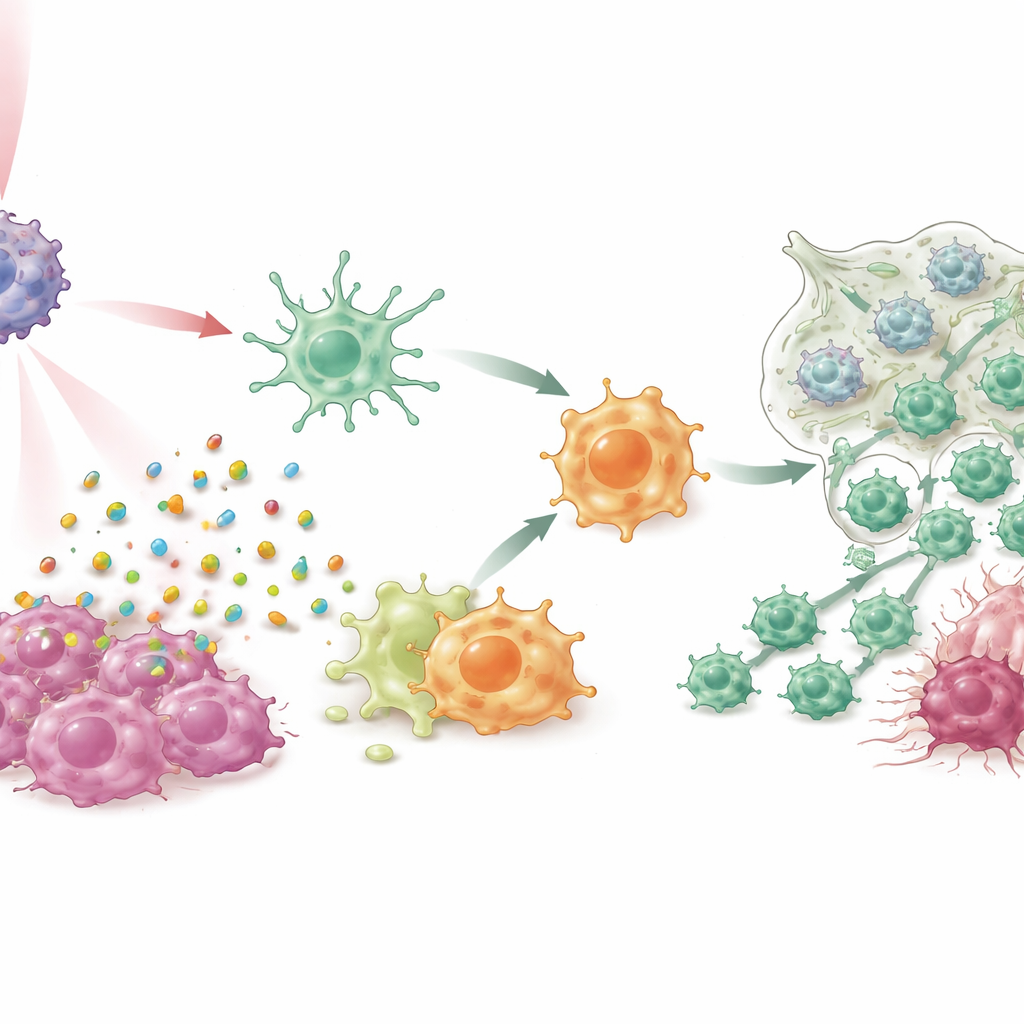
Protection durable et signes d’un potentiel clinique
Fait marquant, les souris dont les tumeurs avaient été éliminées par IPANP et lumière étaient protégées lorsque les chercheurs ont tenté de réimplanter de nouvelles tumeurs plusieurs mois plus tard, indiquant la formation d’une mémoire immunitaire similaire à celle induite par un vaccin. L’équipe a aussi testé l’approche sur des échantillons de cancers du sein fraîchement prélevés chez des patientes, maintenus vivants sous forme de petits fragments de tissu, et sur des greffons tumoraux dérivés de patientes chez des souris humanisées. Dans ces contextes, le traitement a de nouveau poussé les cellules dendritiques et les macrophages vers des états plus actifs et antitumoraux, réduit les signaux favorisant la croissance, augmenté les molécules inflammatoires bénéfiques, accru la présence de lymphocytes T cytotoxiques et provoqué la mort des cellules tumorales — tout en montrant une bonne sûreté dans des études animales à long terme.
Ce que cela pourrait signifier pour les traitements futurs du cancer
Ce travail montre qu’il pourrait être possible de traiter les cancers du sein agressifs non seulement en attaquant directement les cellules tumorales, mais aussi en rééduquant les cellules immunitaires qui les entourent. En combinant dans une seule nanomicelle intelligente une thérapie activée par la lumière, un blocage de points de contrôle et une reprogrammation génétique, les chercheurs ont créé une action coordonnée qui a transformé un microenvironnement tumoral suppressif en un milieu soutenant une défense immunitaire durable. Bien que de nombreux tests supplémentaires soient nécessaires avant que cette stratégie puisse être proposée aux patientes, elle offre un modèle pour des traitements futurs visant à remodeler l’environnement immunitaire afin de maintenir sous contrôle, à long terme, les tumeurs primaires et métastatiques.
Citation: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
Mots-clés: immunothérapie du cancer du sein, nanomédecine, microenvironnement tumoral, reprogrammation des macrophages, activation des cellules dendritiques