Clear Sky Science · it
Nanomicelle programmabili riconnettono l’immunità mieloide per il controllo duraturo del carcinoma mammario primario e metastatico
Un nuovo modo per aiutare il sistema immunitario a combattere il cancro al seno
La maggior parte dei trattamenti antitumorali si concentra sull’uccisione diretta delle cellule tumorali, ma molti tumori sopravvivono trasformando silenziosamente le cellule immunitarie dell’organismo in alleate. Questo studio descrive una piccola medicina programmabile che mira a riportare quelle cellule a uno stato combattente contro il cancro, offrendo un controllo duraturo di forme aggressive di carcinoma mammario che si sono diffuse ad altri organi.
Perché il cancro al seno può essere così difficile da curare
Il cancro al seno è il tumore più frequentemente diagnosticato nelle donne, e la sua caratteristica più letale è la tendenza a metastatizzare, in particolare ai polmoni. Un sottotipo, il carcinoma mammario triplo negativo, è particolarmente difficile da trattare perché manca dei comuni bersagli ormonali e dei fattori di crescita. Anche le immunoterapie moderne che bloccano lo “scudo” PD‑L1 sulle cellule tumorali aiutano solo una frazione di pazienti e spesso non riescono a prolungare la sopravvivenza. Una ragione importante è il microambiente del tumore — il vicinato immediato di cellule e molecole attorno al cancro — che è pieno di cellule immunitarie riprogrammate a sopprimere, anziché sostenere, gli attacchi anti‑tumorali.
L’influenza nascosta delle cellule di supporto intorno ai tumori
Tra queste cellule circostanti, due tipi di cellule mieloidi svolgono un ruolo sproporzionato: le cellule dendritiche e i macrofagi. In condizioni di salute, le cellule dendritiche agiscono da sentinelle, catturano molecole sospette e le mostrano alle cellule T per innescare un attacco immunitario mirato. I macrofagi possono supportare l’infiammazione (simili a M1) e contribuire a eliminare le minacce, oppure calmare la risposta e promuovere la riparazione tissutale (simili a M2). Nei tumori mammari di pazienti e modelli murini, gli autori hanno riscontrato meno cellule dendritiche mature e un’abbondanza di macrofagi di tipo M2. Questi macrofagi “pacificatori” erano associati a scarsa infiltrazione delle cellule T e a esiti peggiori, suggerendo che se gli scienziati potessero riprogrammare queste cellule in combattenti, si potrebbero sbloccare risposte immunitarie più potenti e durature contro il cancro.
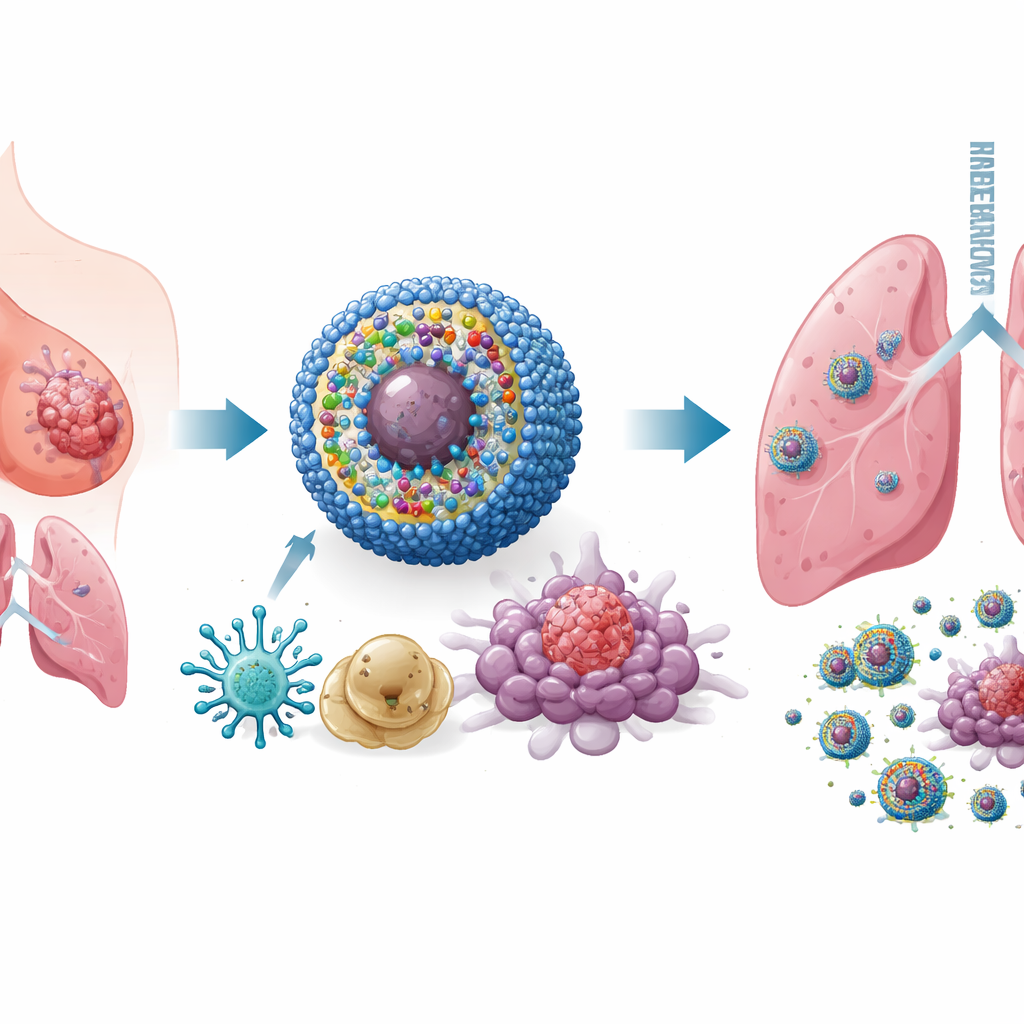
Progettare una nanomedicina intelligente e multifunzione
Per affrontare questo problema, i ricercatori hanno costruito un sistema di veicolazione su scala nanometrica che chiamano IPANP — piccole micelle sferiche che circolano nel flusso sanguigno e si accumulano nei tumori. Ogni nanomicella trasporta tre componenti. Primo, un colorante attivabile dalla luce (IR825) che, quando illuminato con luce nel vicino infrarosso dall’esterno del corpo, genera molecole reattive che stressano e uccidono le cellule tumorali in modo da renderle altamente visibili al sistema immunitario. Secondo, un anticorpo contro PD‑L1, che contribuisce a rimuovere un freno molecolare che i tumori usano per spegnere le cellule T. Terzo, un breve frammento di materiale genetico (antagomiR‑182) che blocca un microRNA, miR‑182, presente ad alti livelli nei macrofagi che favoriscono il tumore. Il vettore è sensibile all’ambiente chimicamente reattivo all’interno dei tumori, quindi rilascia il suo carico principalmente dove è necessario, limitando l’esposizione ai tessuti sani.
Trasformare le cellule soppressive in attaccanti
In colture cellulari e in più modelli murini di carcinoma mammario, inclusi i difficili sistemi triplo negativi e tumori spontanei, IPANP combinato con una leggera luce nel vicino infrarosso ha fatto più che ridurre i tumori. Il colorante attivato dalla luce ha indotto la morte delle cellule cancerose in modo “immunogenico”, rilasciando segnali di pericolo che hanno spinto le cellule dendritiche a maturare e a presentare frammenti tumorali in modo più efficiente alle cellule T. Allo stesso tempo, il blocco di miR‑182 nei macrofagi ha tolto un freno a una via di riconoscimento chiave (TLR4/MYD88/NF‑κB), inducendoli a passare dallo stato di supporto tumorale simile a M2 verso uno stato infiammatorio simile a M1. Man mano che questi due tipi di cellule mieloidi cambiavano ruolo, più cellule T citotossiche affluivano nei tumori, diventavano più attive e avevano meno probabilità di spegnersi per esaurimento. Il risultato è stato un forte controllo dei tumori primari, nette riduzioni delle metastasi polmonari e una sopravvivenza prolungata negli animali trattati.
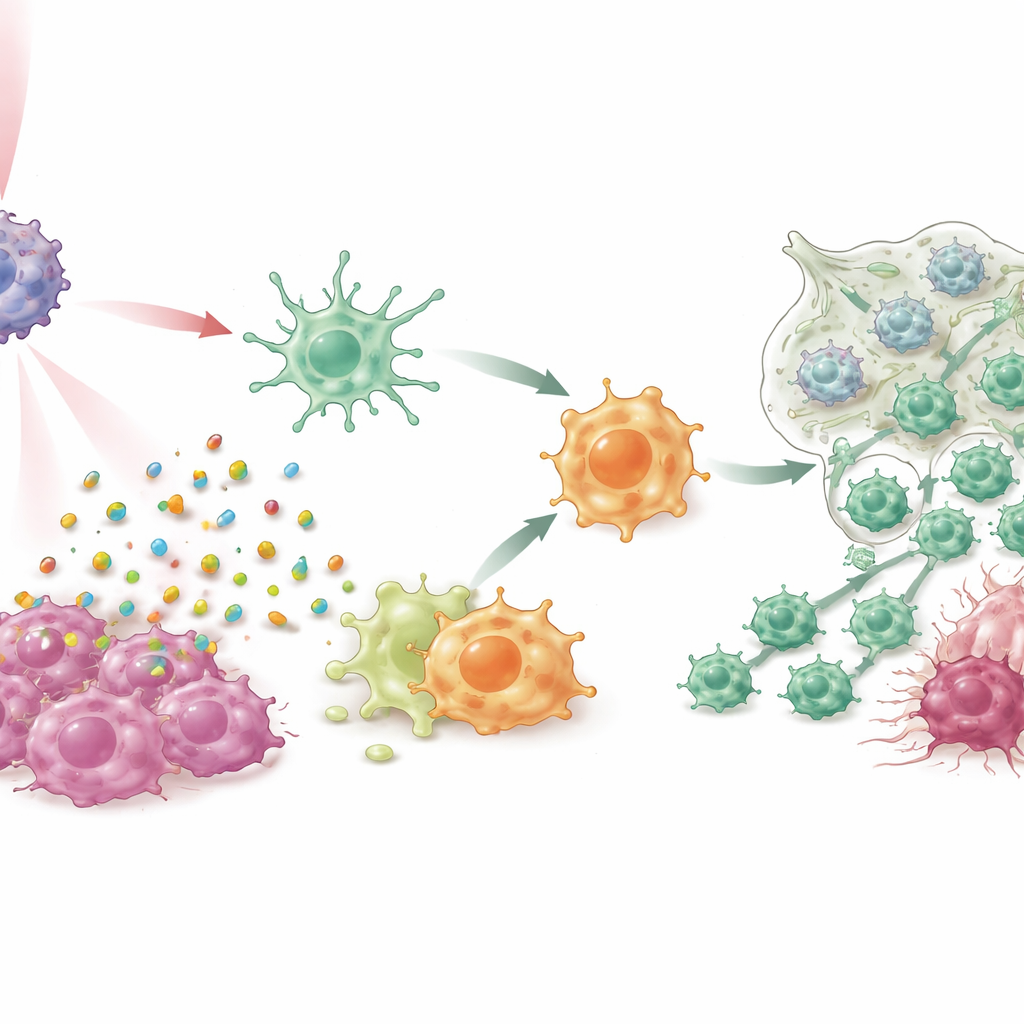
Protezione duratura e segnali di potenziale applicabilità clinica
In modo sorprendente, i topi i cui tumori erano stati eliminati da IPANP e luce sono stati protetti quando i ricercatori hanno tentato di reimpiantare nuovi tumori mesi dopo, indicando la formazione di memoria immunitaria simile a quella indotta da un vaccino. Il gruppo ha anche testato l’approccio su campioni freschi di carcinoma mammario prelevati da pazienti, mantenuti vitali come piccoli frammenti tissutali, e su trapianti tumorali derivati da pazienti in topi “umanizzati”. In questi contesti, il trattamento ha nuovamente spinto cellule dendritiche e macrofagi verso stati più attivi e anti‑tumorali, ha ridotto segnali che promuovono la crescita, ha aumentato molecole infiammatorie benefiche, ha incrementato la presenza di cellule T citotossiche e ha provocato la morte delle cellule tumorali — il tutto mostrando una buona sicurezza negli studi animali a lungo termine.
Cosa potrebbe significare per i futuri trattamenti del cancro
Questo lavoro mostra che potrebbe essere possibile trattare tumori mammari aggressivi non solo attaccando direttamente le cellule tumorali, ma rieducando le cellule immunitarie che le circondano. Impacchettando terapia attivata dalla luce, blocco dei checkpoint e riprogrammazione genetica in una singola nanomicella intelligente, i ricercatori hanno creato una spinta coordinata che ha trasformato un microambiente tumorale soppressivo in uno che sostiene una difesa immunitaria duratura. Pur richiedendo molti altri test prima che questa strategia possa raggiungere i pazienti, offre un progetto di riferimento per trattamenti futuri che rimodellano l’ambiente immunitario per mantenere sotto controllo a lungo termine sia i tumori primari sia le metastasi.
Citazione: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
Parole chiave: immunoterapia del cancro al seno, nanomedicina, microambiente tumorale, riprogrammazione dei macrofagi, attivazione delle cellule dendritiche