Clear Sky Science · pl
Programowalne nanomicelle przeprogramowują odporność mieloidalną dla trwałej kontroli pierwotnego i przerzutowego raka piersi
Nowy sposób wspierania układu odpornościowego w walce z rakiem piersi
Większość terapii przeciwnowotworowych koncentruje się na bezpośrednim zabijaniu komórek nowotworowych, ale wiele guzów przetrwa dzięki temu, że potajemnie zmienia własne komórki odpornościowe w sojuszników. W badaniu opisano maleńki, programowalny lek, który ma na celu przywrócenie tym komórkom roli bojowników z rakiem, oferując długotrwałą kontrolę agresywnych raków piersi, które rozprzestrzeniły się do innych narządów.
Dlaczego rak piersi bywa trudny do wyleczenia
Rak piersi jest najczęściej rozpoznawanym nowotworem u kobiet, a jego najgroźniejszą cechą jest skłonność do przerzutów, zwłaszcza do płuc. Jeden z podtypów, rak potrójnie ujemny, jest szczególnie trudny w leczeniu, ponieważ brak mu typowych celów hormonalnych i wzrostowych. Nawet nowoczesne immunoterapie blokujące „tarcza” PD‑L1 na komórkach guza pomagają tylko części pacjentek i często nie wydłużają przeżycia. Główną przyczyną jest mikrośrodowisko guza — bezpośrednie sąsiedztwo komórek i cząsteczek wokół nowotworu — w którym gromadzą się komórki odpornościowe przeprogramowane tak, by hamować, zamiast wspierać, odpowiedź przeciwnowotworową.
Ukryty wpływ komórek wspierających guz
Wśród tych otaczających komórek dwie populacje mieloidalne odgrywają niezwykle istotną rolę: komórki dendrytyczne i makrofagi. W warunkach zdrowych komórki dendrytyczne działają jak wartownicy, wychwytując podejrzane molekuły i prezentując je limfocytom T, by wywołać ukierunkowaną odpowiedź immunologiczną. Makrofagi mogą wspierać stan zapalny (fenotyp podobny do M1) i pomagać w usuwaniu zagrożeń, albo łagodzić reakcję i promować naprawę tkanek (fenotyp podobny do M2). W guzach piersi u pacjentek i w modelach mysich autorzy stwierdzili zmniejszoną liczbę dojrzałych komórek dendrytycznych i nadmiar makrofagów o fenotypie M2. Te „stróże pokoju” były powiązane ze słabym napływem limfocytów T i gorszymi wynikami, co sugeruje, że przeprogramowanie tych komórek z powrotem na walczące mogłoby odblokować silniejsze i trwalsze odpowiedzi odpornościowe przeciw nowotworowi.
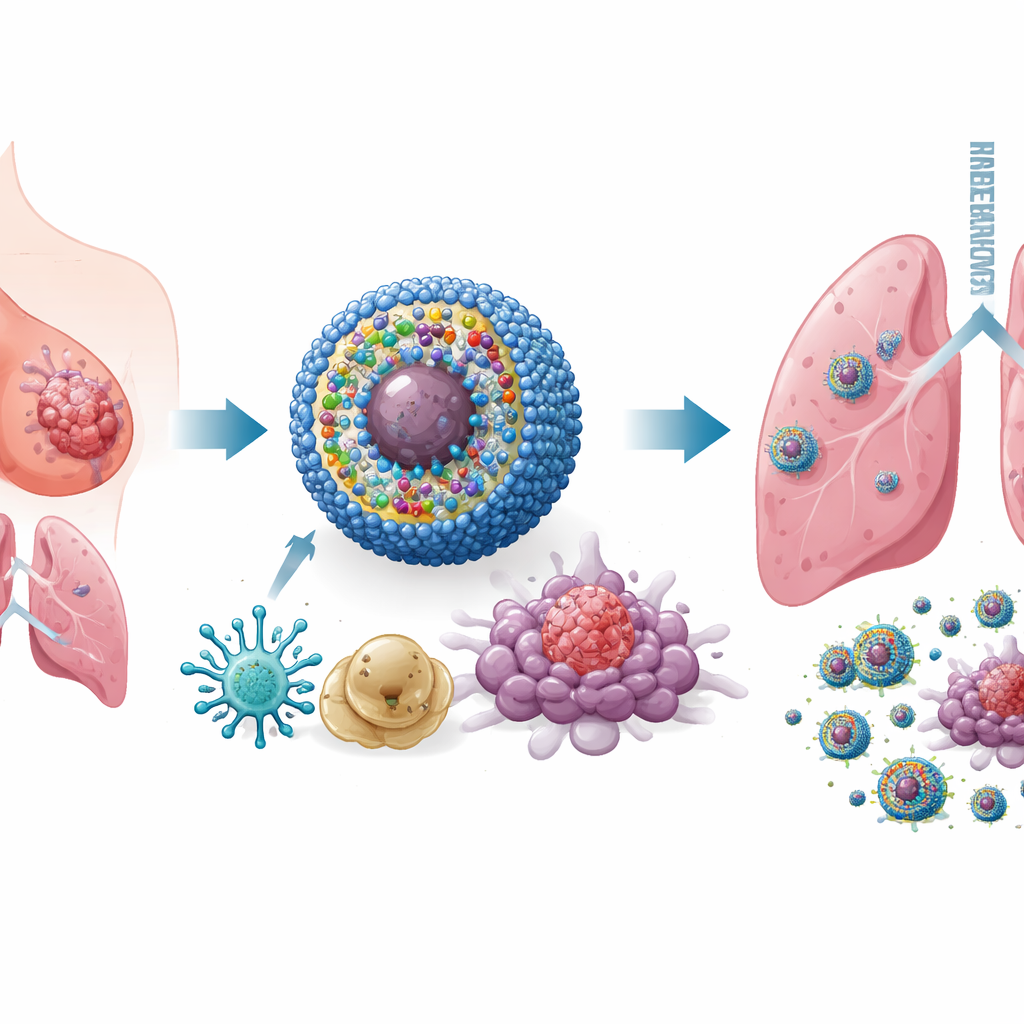
Projektowanie inteligentnej, wielofunkcyjnej nanomedycyny
Aby rozwiązać ten problem, badacze stworzyli układ dostarczania w skali nanometrowej, który nazwali IPANP — maleńkie sferyczne micele krążące we krwi i kumulujące się w guzach. Każda nanomicele niesie trzy składniki. Po pierwsze barwnik aktywowany światłem (IR825), który po oświetleniu bliską podczerwienią z zewnątrz generuje reaktywne cząsteczki stresujące i zabijające komórki nowotworowe w sposób czyniący je wyraźnie widocznymi dla układu odpornościowego. Po drugie przeciwciało przeciw PD‑L1, które pomaga usunąć molekularny hamulec używany przez guzy do wyłączania limfocytów T. Po trzecie krótki fragment materiału genetycznego (antagomiR‑182), blokujący mikroRNA miR‑182, występujący w dużych ilościach w makrofagach promujących wzrost guza. Nośnik jest wrażliwy na chemicznie reaktywne środowisko wewnątrz guzów, więc uwalnia ładunek głównie tam, gdzie jest potrzebny, ograniczając ekspozycję zdrowych tkanek.
Przeobrażanie komórek supresyjnych w atakujące
W hodowlach komórkowych i wielu modelach mysich raka piersi, w tym trudnych modelach potrójnie ujemnych i spontanicznych guzów, IPANP w połączeniu z delikatnym światłem bliskiej podczerwieni robił więcej niż tylko zmniejszał guzy. Barwnik aktywowany światłem powodował, że komórki nowotworowe umierały w sposób „immunogenny”, uwalniając sygnały zagrożenia, które skłaniały komórki dendrytyczne do dojrzewania i efektywniejszego prezentowania fragmentów guza limfocytom T. Równocześnie blokada miR‑182 w makrofagach zdjemowała hamulec z kluczowej ścieżki detekcji (TLR4/MYD88/NF‑κB), popychając je z fenotypu wspierającego guz M2 w kierunku prozapalnego, przypominającego M1. W miarę jak te dwa typy komórek mieloidalnych zmieniały role, do guzów napływało więcej zabójczych limfocytów T, stawały się one bardziej aktywne i mniej podatne na wyłączenie wskutek wyczerpania. Efektem była silna kontrola guzów pierwotnych, znaczące zmniejszenie przerzutów do płuc i wydłużone przeżycie leczonych zwierząt.
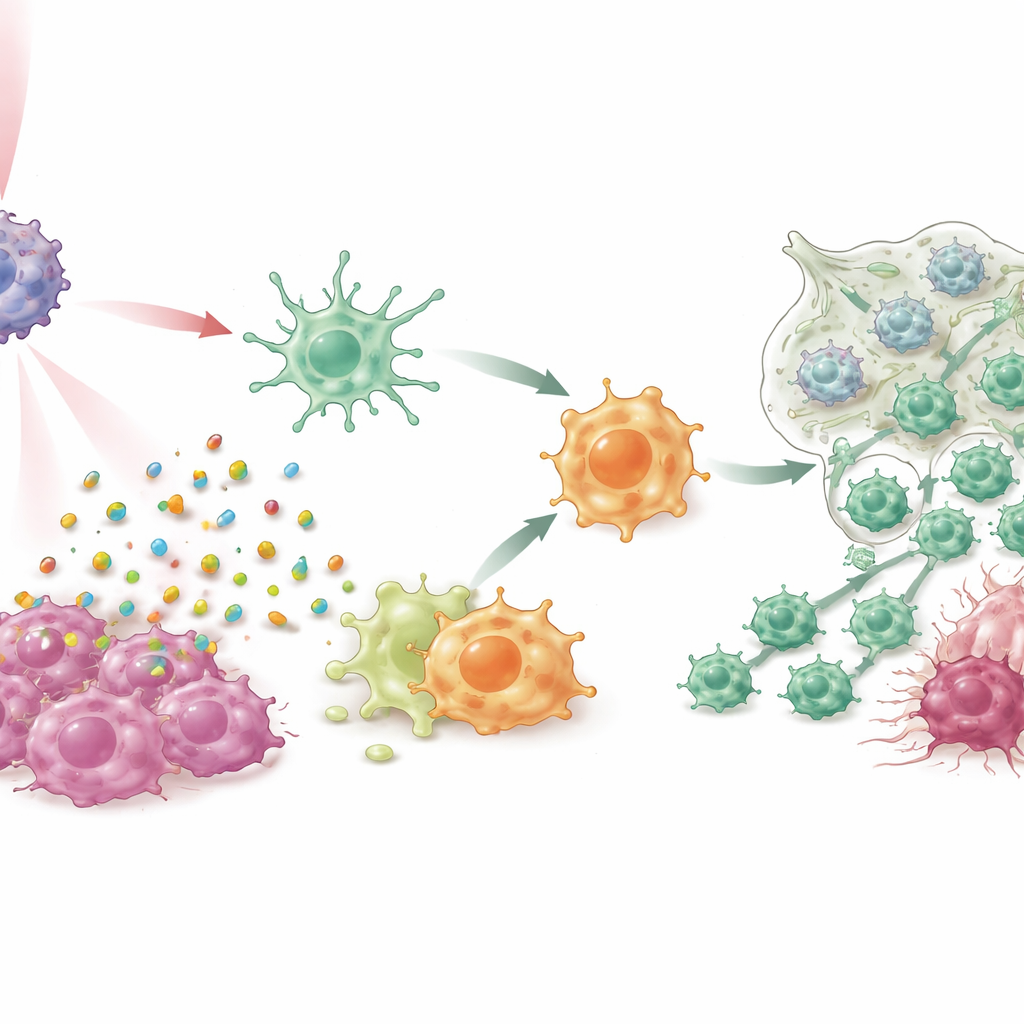
Trwała ochrona i sygnały obiecujące zastosowania kliniczne
Co zaskakujące, myszy, u których guzów pozbyto się dzięki IPANP i światłu, były chronione, gdy badacze próbowali ponownie wszczepić nowe guzy miesiące później, co wskazuje na powstanie pamięci immunologicznej podobnej do tej, jaką daje szczepionka. Zespół przetestował podejście także na świeżo pobranych próbkach raka piersi od pacjentek, utrzymywanych w stanie żywym jako małe fragmenty tkanki, oraz w przeszczepach nowotworowych pochodzących od pacjentek w zhumanizowanych myszach. W tych warunkach terapia ponownie przesunęła komórki dendrytyczne i makrofagi w kierunku bardziej aktywnych, przeciwnowotworowych stanów, zmniejszyła sygnały sprzyjające wzrostowi, zwiększyła korzystne cząsteczki prozapalne, zwiększyła obecność zabójczych limfocytów T i wywołała śmierć komórek nowotworowych — wszystko przy wykazaniu dobrej tolerancji w długoterminowych badaniach na zwierzętach.
Co to może znaczyć dla przyszłego leczenia raka
Praca ta pokazuje, że możliwe jest leczenie agresywnych raków piersi nie tylko przez bezpośrednie atakowanie komórek nowotworowych, lecz także przez przeszkolenie otaczających je komórek odpornościowych. Łącząc terapię aktywowaną światłem, blokadę punktów kontrolnych i przeprogramowywanie genetyczne w jedną inteligentną nanomicele, badacze stworzyli skoordynowany impuls, który przemienił supresyjne sąsiedztwo guza w środowisko wspierające trwałą obronę immunologiczną. Choć potrzeba znacznie więcej badań, zanim strategia ta trafi do pacjentek, stanowi ona plan działania dla przyszłych terapii, które przebudowują środowisko immunologiczne, by utrzymać pod kontrolą zarówno guzy pierwotne, jak i przerzutowe przez długi czas.
Cytowanie: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
Słowa kluczowe: immunoterapia raka piersi, nanomedycyna, mikrośrodowisko guza, przeprogramowywanie makrofagów, aktywacja komórek dendrytycznych