Clear Sky Science · pt
Nanomicelas programáveis reprogramam a imunidade mieloide para controle duradouro do câncer de mama primário e metastático
Uma nova forma de ajudar o sistema imunológico a combater o câncer de mama
A maioria dos tratamentos contra o câncer foca em matar as células tumorais diretamente, mas muitos tumores sobrevivem ao converter silenciosamente as próprias células imunes do corpo em aliadas. Este estudo descreve uma medicina minúscula e programável que visa reverter essas células para o papel de combatentes do câncer, oferecendo controle duradouro de carcinomas de mama agressivos que se espalharam para outros órgãos.
Por que o câncer de mama pode ser tão difícil de curar
O câncer de mama é o tumor mais diagnosticado em mulheres, e sua característica mais letal é a tendência de metastizar, especialmente para os pulmões. Um subtipo, o câncer de mama triplo‑negativo, é particularmente difícil de tratar porque carece dos alvos hormonais e de fatores de crescimento comuns. Mesmo imunoterapias modernas que bloqueiam o “escudo” PD‑L1 nas células tumorais beneficiam apenas uma fração dos pacientes e frequentemente não prolongam a sobrevida. Uma razão importante é o microambiente tumoral — o entorno imediato de células e moléculas ao redor do câncer — que está repleto de células imunes reprogramadas para suprimir, em vez de apoiar, os ataques antitumorais.
A influência oculta das células de suporte ao redor dos tumores
Entre essas células ao redor, dois tipos de células mieloides têm papel excessivo: células dendríticas e macrófagos. Em condições saudáveis, as células dendríticas atuam como sentinelas, captando moléculas suspeitas e exibindo‑as às células T para provocar um ataque imune direcionado. Macrófagos podem tanto apoiar a inflamação (semelhança M1) e ajudar a eliminar ameaças, quanto acalmar a resposta e promover reparo tecidual (semelhança M2). Em tumores de mama de pacientes e em modelos murinos, os autores encontraram menos células dendríticas maduras e um excesso de macrófagos com fenótipo M2. Esses macrófagos “pacificadores” estavam associados a baixa infiltração de células T e piores desfechos, sugerindo que, se os cientistas conseguissem reprogramar essas células de volta a combatentes, poderiam desbloquear respostas imunes mais potentes e duradouras contra o câncer.
Projetando uma nanomedicina inteligente e multifunção
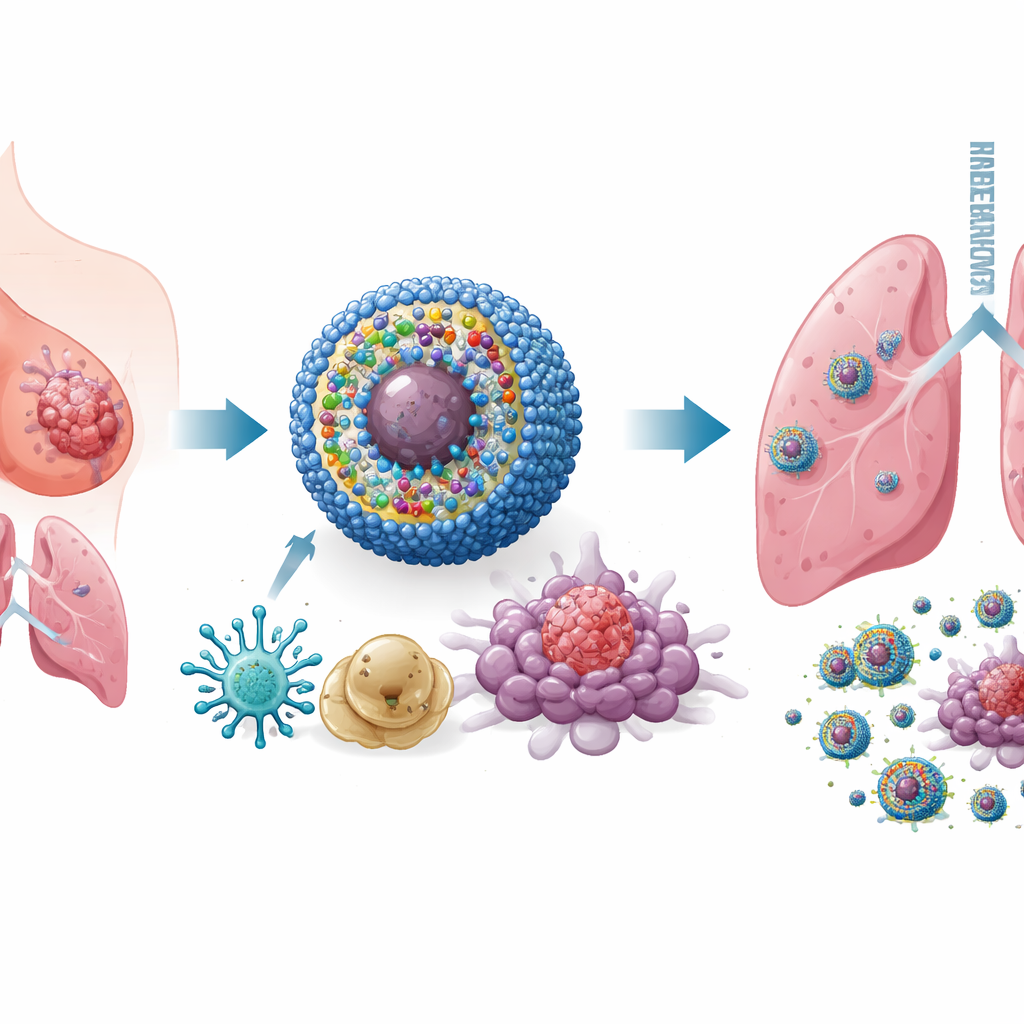
Para enfrentar esse problema, os pesquisadores construíram um sistema de entrega em escala nanométrica que chamam IPANP — micelas esféricas minúsculas que circulam na corrente sanguínea e se acumulam em tumores. Cada nanomicela carrega três componentes. Primeiro, um corante ativado por luz (IR825) que, quando iluminado com luz no infravermelho próximo vinda de fora do corpo, gera moléculas reativas que estressam e matam células tumorais de modo a torná‑las altamente visíveis ao sistema imunológico. Segundo, um anticorpo contra PD‑L1, que ajuda a remover um freio molecular que os tumores usam para desligar células T. Terceiro, um pequeno trecho de material genético (antagomiR‑182) que bloqueia um microRNA, miR‑182, encontrado em altos níveis em macrófagos que promovem tumor. O veículo é sensível ao ambiente quimicamente reativo presente dentro dos tumores, de modo que libera sua carga principalmente onde é necessário, limitando a exposição a tecidos saudáveis.
Transformando células supressoras em atacantes
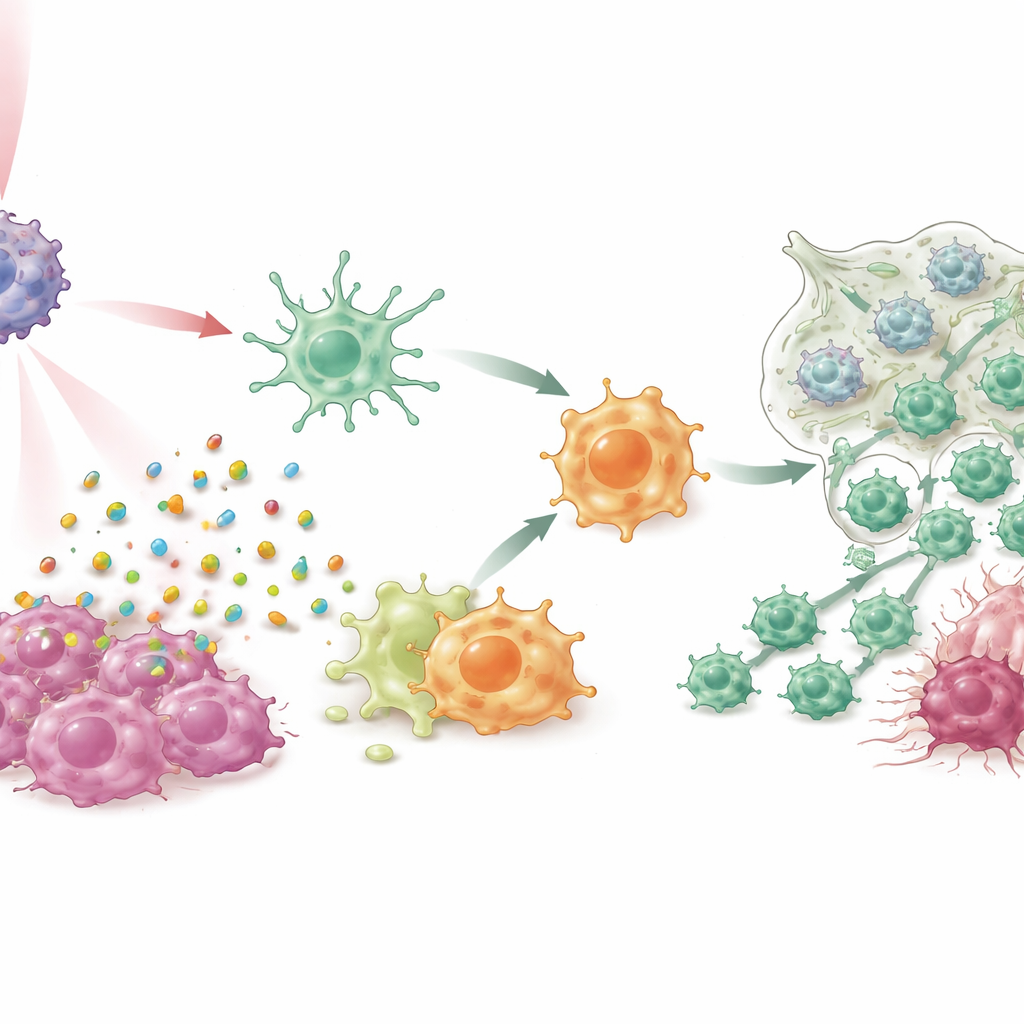
Em culturas celulares e em múltiplos modelos murinos de câncer de mama, incluindo casos difíceis triplo‑negativos e tumores espontâneos, o IPANP combinado com luz suave no infravermelho próximo fez mais do que apenas encolher tumores. O corante ativado por luz fez com que as células cancerosas morressem de maneira “imunogênica”, liberando sinais de perigo que incentivaram as células dendríticas a amadurecer e apresentar fragmentos tumorais de forma mais eficiente às células T. Ao mesmo tempo, bloquear o miR‑182 nos macrófagos removeu um freio em uma via sensora chave (TLR4/MYD88/NF‑κB), inclinando‑os do estado M2, que suporta tumores, para um estado M1, pró‑inflamatório. À medida que esses dois tipos de células mieloides mudaram de papel, mais células T citotóxicas infiltraram os tumores, tornaram‑se mais ativas e foram menos propensas a entrar em exaustão. O resultado foi controle robusto dos tumores primários, reduções acentuadas nas metástases pulmonares e sobrevida prolongada nos animais tratados.
Proteção duradoura e sinais de potencial no mundo real
De forma impressionante, camundongos cujos tumores foram eliminados pelo IPANP e pela luz estavam protegidos quando os pesquisadores tentaram reimplantar novos tumores meses depois, indicando formação de memória imune semelhante à criada por uma vacina. A equipe também testou a abordagem em amostras de câncer de mama recém‑removidas de pacientes, mantidas vivas como pequenos fragmentos de tecido, e em enxertos tumorais derivados de pacientes em camundongos humanizados. Nesses contextos, o tratamento novamente empurrou células dendríticas e macrófagos para estados mais ativos e antitumorais, reduziu sinais que promovem crescimento, aumentou moléculas inflamatórias benéficas, elevou a presença de células T citotóxicas e causou morte de células tumorais — tudo isso mostrando boa segurança em estudos animais de longo prazo.
O que isso pode significar para tratamentos futuros do câncer
Este trabalho mostra que pode ser possível tratar cânceres de mama agressivos não apenas atacando as células tumorais diretamente, mas reeducando as células imunes que as cercam. Ao embalar terapia ativada por luz, bloqueio de checkpoint e reprogramação genética em uma única nanomicela inteligente, os pesquisadores criaram um impulso coordenado que transformou um entorno tumoral supressivo em um que apoia defesa imune duradoura. Embora sejam necessários muitos testes antes que essa estratégia alcance pacientes, ela oferece um roteiro para tratamentos futuros que remodelam o ambiente imune para manter tanto tumores primários quanto metastáticos sob controle a longo prazo.
Citação: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
Palavras-chave: imunoterapia do câncer de mama, nanomedicina, microambiente tumoral, reprogramação de macrófagos, ativação de células dendríticas