Clear Sky Science · ar
نانوميشيئات قابلة للبرمجة تعيد توصيل مناعة الخلايا النخاعية للسيطرة طويلة الأمد على سرطان الثدي الأساسي والمنتشر
طريقة جديدة لمساعدة الجهاز المناعي على مقاومة سرطان الثدي
تركز معظم علاجات السرطان على قتل خلايا الورم مباشرة، لكن العديد من الأورام تنجو عن طريق تحويل خلايا المناعة في الجسم بهدوء إلى حلفاء. تصف هذه الدراسة دواءً دقيقًا قابلاً للبرمجة يهدف إلى قلب حالة تلك الخلايا لتصبح مقاتلة للسرطان مرة أخرى، مقدّمًا سيطرة طويلة الأمد على سرطانات الثدي العدوانية التي انتشرت إلى أعضاء أخرى.
لماذا قد يصعب علاج سرطان الثدي
يعد سرطان الثدي أكثر السرطانات تشخيصًا بين النساء، والخاصية الأكثر فتكا به هي ميله للانتشار، خاصة إلى الرئتين. أحد الأنماط الفرعية، سرطان الثدي ثلاثي السلبي، يصعب علاجه بشكل خاص لأنه يفتقر إلى أهداف هرمونية وعوامل نمو شائعة. حتى العلاجات المناعية الحديثة التي تمنع «الدرع» PD‑L1 على خلايا الورم تفيد نسبة صغيرة فقط من المرضى وغالبًا لا تطيل البقاء. سبب رئيسي لذلك هو الوسط الميكروورمي للورم—الحيّز المحيط من الخلايا والجزيئات حول السرطان—الذي يكتظ بخلايا مناعية تم إعادة برمجتها لقمع، بدلًا من دعم، الهجمات المناعية المضادة للورم.
التأثير الخفي للخلايا الداعمة حول الأورام
من بين هذه الخلايا المحيطة، يلعب نوعان من الخلايا النخاعية دورًا بارزًا: الخلايا الشجيرية (الدندريتية) والبلعميات الكبيرة (الماكروفاج). في الحالات الصحية، تعمل الخلايا الشجيرية كحراس، تلتقط جزيئات مريبة وتعرضها على الخلايا التائية لإطلاق هجوم مناعي موجه. يمكن للبلعميات الكبيرة أن تدعم الالتهاب (شبيهة M1) وتساعد في إزالة التهديدات، أو تهدئ الأمور وتدعم إصلاح الأنسجة (شبيهة M2). في أورام الثدي لدى المرضى ونماذج الفئران، وجد الباحثون نقصًا في الخلايا الشجيرية الناضجة وكثرة في البلعميات الكبيرة الشبيهة بـM2. ارتبطت هذه البلعميات "حارسات السلام" بمعدلات أقل من توغل الخلايا التائية ونتائج أسوأ، ما يوحي بأنه إذا تمكن العلماء من إعادة توصيل هذه الخلايا لتصبح مقاتلة مرة أخرى، فقد يفتح ذلك استجابات مناعية أقوى وأكثر دوامًا ضد السرطان.
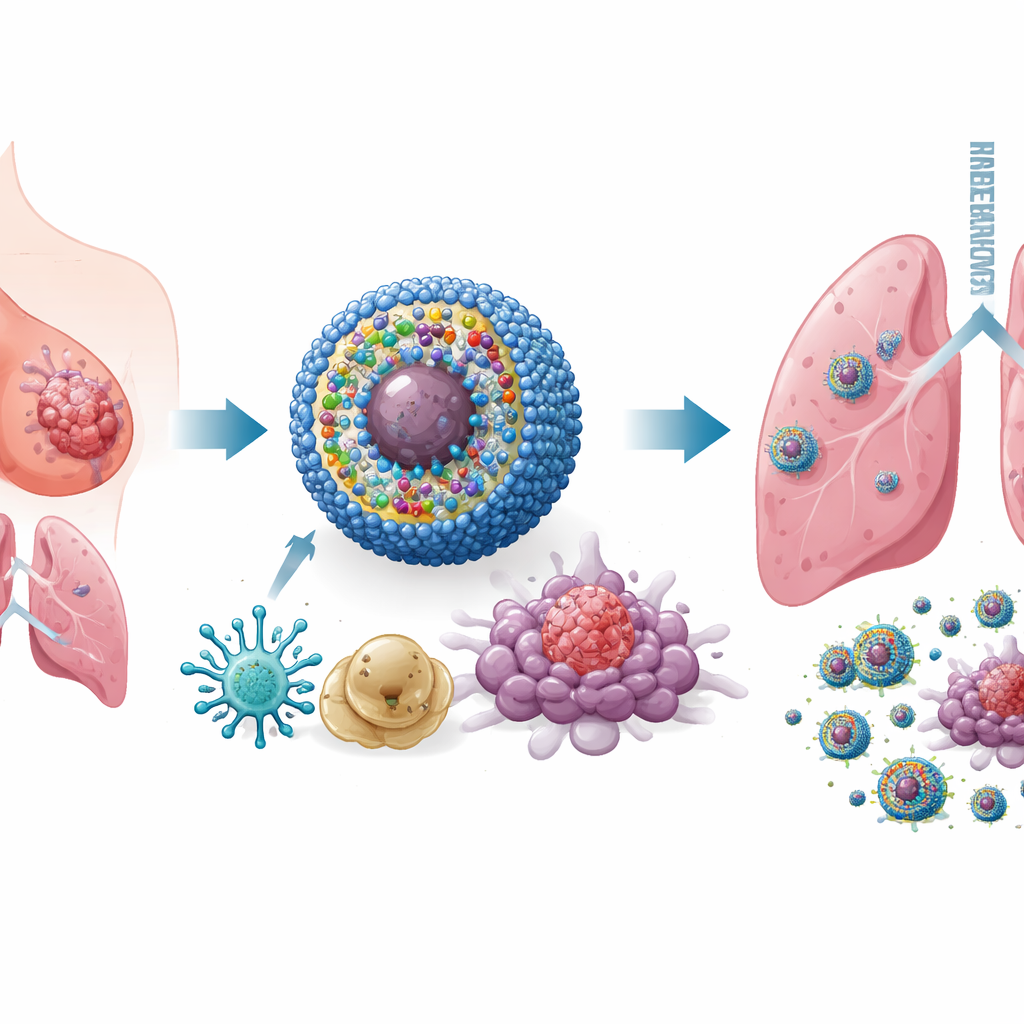
تصميم دواء نانوي ذكي متعدد الأدوات
لمعالجة هذه المشكلة، بنى الباحثون نظام توصيل على مقياس نانوي أسموه IPANP—ميشيئات كروية مجهرية تدور في مجرى الدم وتتراكم في الأورام. تحمل كل نانوميشيئة ثلاثة مكوّنات. أولًا، صبغة مفعلة بالضوء (IR825) التي عند تسليط ضوء قرب الأشعة تحت الحمراء من خارج الجسم تولّد جزيئات تفاعلية تجهد وتقتل خلايا الورم بطريقة تجعلها مرئية جدًا للجهاز المناعي. ثانيًا، جسم مضاد ضد PD‑L1 يساعد على إزالة مكبح جزيئي تستخدمه الأورام لإيقاف الخلايا التائية. ثالثًا، قطعة قصيرة من مادة جينية (antagomiR‑182) تحجب ميكروRNA، miR‑182، الموجود بمستويات عالية في البلعميات الكبيرة المحفّزة للورم. الحامل حساس للبيئة الكيميائية التفاعلية داخل الأورام، لذا يطلق حمولته بشكل أساسي حيث تكون الحاجة إليها، محددًا التعرض للأنسجة السليمة.
تحويل الخلايا الكابحة إلى مهاجمة
في مزروعات خلوية والعديد من نماذج الفئران لسرطان الثدي، بما في ذلك الأنظمة الثلاثية السلبي والصفيحة العفوية، أدى IPANP مع ضوء قرب‑الأشعة تحت الحمراء الخفيف إلى أكثر من مجرد تقليص الأورام. تسببت الصبغة المفعلة بالضوء في موت الخلايا السرطانية بطريقة «مناعية التحفيز»، مفجرة إشارات خطر دفعت الخلايا الشجيرية للنضج وعرض شظايا الورم بفعالية أكبر على الخلايا التائية. في الوقت نفسه، رفع حجب miR‑182 في البلعميات الكبيرة مكبحًا عن مسار استشعار رئيسي (TLR4/MYD88/NF‑κB)، دافعًا إياها من حالة دعم الورم الشبيهة بـM2 نحو حالة التهابية شبيهة بـM1. مع تحوّل هذين النوعين من الخلايا النخاعية، اجتاحت خلايا تائية قاتلة المزيد من الأورام، أصبحت أكثر نشاطًا، وكانت أقل عرضة للتعطّل بسبب الإرهاق. كانت النتيجة سيطرة قوية على الأورام الأولية، انخفاضات حادة في النقائل الرئوية، وبقاء مطوَّل في الحيوانات المعالجة.
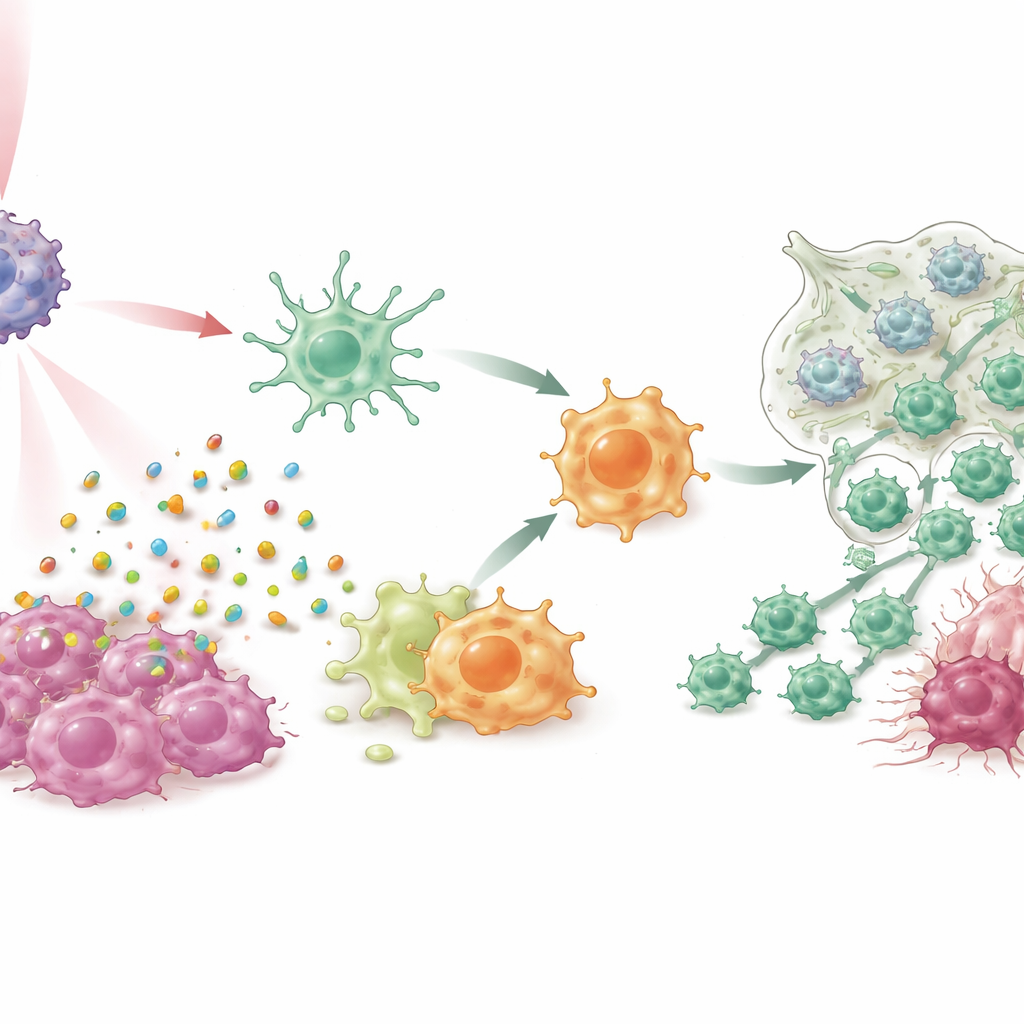
حماية طويلة الأمد ودلائل على وعد سريري
لافتٌ للنظر، أن الفئران التي أُزيلت أورامها بواسطة IPANP والضوء كانت محمية عندما حاول الباحثون زرع أورام جديدة بعد أشهر، مما يشير إلى تكوّن ذاكرة مناعية شبيهة بالتي يخلقها اللقاح. اختبر الفريق أيضًا النهج على عينات سرطان ثدي مستأصلة حديثًا من مرضى، أُبقيت حية كقطع نسيجية صغيرة، وفي طعوم ورمية مشتقة من المرضى في فئران مُؤَنَّسة بشريًا. في هذه الإعدادات، دفعت المعالجة مرة أخرى الخلايا الشجيرية والبلعميات الكبيرة نحو حالات أكثر نشاطًا مضادة للورم، خفّضت إشارات تعزيز النمو، عزّزت الجزيئات الالتهابية المفيدة، زادت وجود الخلايا التائية القاتلة، وتسببت في موت خلايا الورم—كل ذلك مع إظهار سلامة جيدة في دراسات طويلة الأمد على الحيوانات.
ما الذي قد يعنيه هذا لعلاج السرطان في المستقبل
تُظهر هذه العمل أنه قد يكون ممكنًا علاج سرطانات الثدي العدوانية ليس فقط بمهاجمة خلايا الورم مباشرة، بل بإعادة تعليم خلايا المناعة المحيطة بها. من خلال حزم علاج مفعل بالضوء، وكسر نقاط التفتيش المناعي، وإعادة برمجة جينية في نانوميشيئة ذكية واحدة، خلق الباحثون دفعة منسقة حوّلت الحيّز المثبط للورم إلى بيئة تدعم دفاعًا مناعيًا دائمًا. بينما ثمة حاجة لاختبارات كثيرة إضافية قبل أن يصل هذا النهج إلى المرضى، فإنه يقدم مخططًا لعلاجات مستقبلية تُعيد تشكيل البيئة المناعية لإبقاء كل من الأورام الأولية والنقائل تحت سيطرة طويلة الأمد.
الاستشهاد: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
الكلمات المفتاحية: العلاج المناعي لسرطان الثدي, الطب النانوي, الوسط الميكروورمي للورم, إعادة برمجة البالعات الكبيرة, تنشيط الخلايا الشجيرية