Clear Sky Science · tr
Programlanabilir nanomiselar, miyeloid bağışıklığı yeniden yönlendirerek primer ve metastatik meme kanserini kalıcı olarak kontrol altına alıyor
Bağışıklık sisteminin meme kanseriyle savaşmasına yardım etmenin yeni bir yolu
Çoğu kanser tedavisi tümör hücrelerini doğrudan öldürmeye odaklanır, ancak birçok tümör, vücudun kendi bağışıklık hücrelerini sessizce müttefik haline getirerek hayatta kalır. Bu çalışma, bu hücreleri tekrar kanserle savaşan hale çevirmeyi amaçlayan, programlanabilir küçük bir ilacı tanımlıyor ve diğer organlara yayılmış agresif meme kanserlerinin uzun süreli kontrolünü vad ediyor.
Meme kanserinin neden iyileştirilmesi zor olabilir
Meme kanseri kadınlarda en sık teşhis edilen kanserdir ve en ölümcül özelliği özellikle akciğerlere yayılma eğilimidir. Üçlü negatif meme kanseri adı verilen bir alt tür, yaygın hormon ve büyüme faktörü hedeflerinden yoksun olduğu için özellikle zordur. Tümör hücrelerindeki PD‑L1 “kalkanını” engelleyen modern immünoterapiler yalnızca hastaların bir kısmına yardımcı oluyor ve sıklıkla sağkalımı uzatamıyor. Bunun başlıca nedenlerinden biri, tümörün mikroçevresi—kanserin etrafındaki hücre ve moleküllerin oluşturduğu yakın çevre—ki burada, anti‑tümör saldırıları baskılayacak şekilde yeniden programlanmış bağışıklık hücreleri yoğunlaşmıştır.
Tümör çevresindeki destek hücrelerin gizli etkisi
Bu çevre hücreler arasında iki tip miyeloid hücre özellikle etkili: dendritik hücreler ve makrofajlar. Sağlıklı koşullarda dendritik hücreler nöbetçi gibi davranır; şüpheli molekülleri alıp T hücrelerine göstererek hedefe yönelik bir bağışıklık yanıtı başlatır. Makrofajlar ise iltihabı destekleyebilir (M1‑benzeri) ve tehditleri temizlemeye yardım edebilir veya durumu yatıştırıp doku onarımını teşvik edebilir (M2‑benzeri). Hastalardan ve fare modellerinden alınan meme tümörlerinde, yazarlar daha az olgun dendritik hücre ve bol miktarda M2‑benzeri makrofaj buldular. Bu “barışçı” makrofajlar, T hücre infiltrasyonunun zayıf olması ve daha kötü sonuçlarla ilişkiliydi; bu da bilim insanlarının bu hücreleri yeniden savaşçı hale getirebilirse, kansera karşı daha güçlü ve kalıcı bağışıklık yanıtları açığa çıkarabileceğini düşündürüyor.
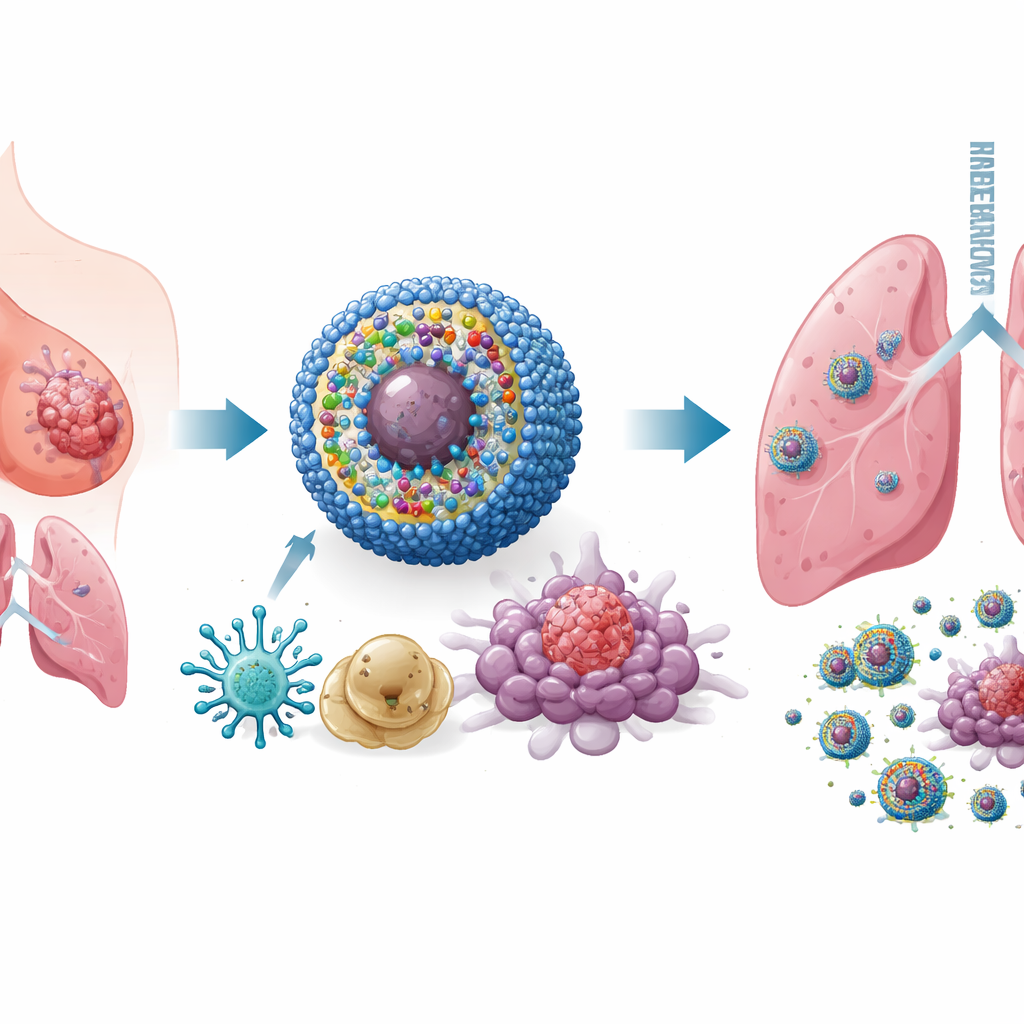
Akıllı, çok amaçlı bir nanotıp tasarlamak
Bu sorunu çözmek için araştırmacılar IPANP adını verdikleri nanoskaladaki bir taşıma sistemi geliştirdiler—kan dolaşımında seyreden ve tümörlerde biriken küçük küresel miseller. Her nanomiselde üç bileşen bulunuyor. Birincisi, dışarıdan uygulanan yakın‑kızılötesi ışıkla aydınlatıldığında reaktif moleküller üreten ve tümör hücrelerini bağışıklık sistemi için daha görünür kılacak biçimde strese ve ölüme sokan ışıkla aktive olan bir boya (IR825). İkincisi, tümörlerin T hücrelerini kapatan moleküler bir freni kaldırmaya yardımcı olan PD‑L1’e karşı bir antikor. Üçüncüsü ise tümör destekleyici makrofajlarda yüksek düzeyde bulunan miR‑182 mikroRNA’sını bloke eden kısa bir genetik materyal parçası (antagomiR‑182). Taşıyıcı, tümör içindeki kimyasal olarak reaktif ortama duyarlı olduğundan, yükünü esas olarak gerekli olduğu yerde serbest bırakıyor ve sağlıklı dokuların maruziyetini sınırlıyor.
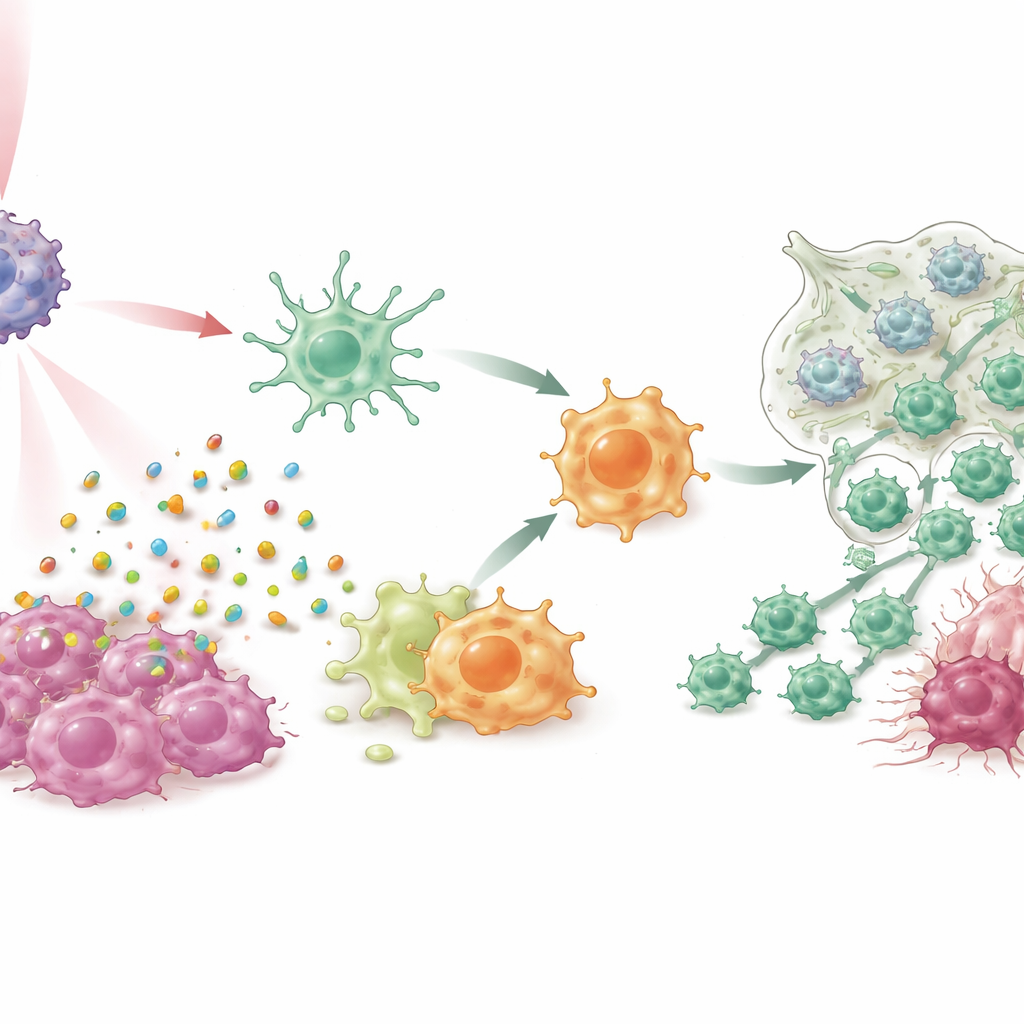
Baskılayıcı hücreleri saldırganlara çevirme
Hücre kültürlerinde ve zorlu üçlü negatif ile spontan tümör sistemleri dahil olmak üzere birden çok meme kanseri fare modelinde, IPANP hafif yakın‑kızılötesi ışıkla birlikte kullanıldığında tümörleri sadece küçültmekle kalmadı. Işıkla aktive olan boya, kanser hücrelerinin “immünojenik” bir biçimde ölmesine yol açtı; bu hücreler tehlike sinyallerini dışarı salarak dendritik hücreleri olgunlaşmaya ve tümör parçalarını T hücrelerine daha verimli sunmaya itti. Aynı zamanda makrofajlarda miR‑182’nin bloke edilmesi, önemli bir algılama yolunun (TLR4/MYD88/NF‑κB) üzerindeki freni kaldırdı ve onları M2‑benzeri, tümör destekleyici durumdan M1‑benzeri, iltihabi duruma doğru itekledi. Bu iki miyeloid hücre tipi rol değiştirirken, daha fazla öldürücü T hücresi tümörlere akın etti, daha aktif hale geldi ve tükenme nedeniyle kapanmaya daha az eğilimli oldu. Sonuç, primer tümörlerin güçlü kontrolü, akciğer metastazlarında keskin azalmalar ve tedavi edilen hayvanlarda uzunlamasına sağkalım oldu.
Kalıcı koruma ve gerçek dünya vaadi işaretleri
Çarpıcı biçimde, IPANP ve ışık ile tümörleri temizlenen fareler, araştırmacıların aylar sonra yeni tümörleri yeniden ekme girişimlerinde korunmuştu; bu, bir aşı tarafından oluşturulana benzer bağışıklık belleğinin oluştuğunu gösteriyor. Ekip aynı yaklaşımı hasta kaynaklı yeni çıkarılmış meme kanseri örneklerinde, canlı küçük doku parçaları olarak tutulduğunda ve insanize farelerde hasta kaynaklı tümör greftlerinde test etti. Bu ortamlarda da tedavi dendritik hücreleri ve makrofajları daha aktif, anti‑tümör durumlara itti, büyümeyi destekleyen sinyalleri azalttı, faydalı iltihabi molekülleri artırdı, öldürücü T hücresi varlığını yükseltti ve tümör hücresi ölümüne yol açtı—tüm bunlar uzun dönem hayvan çalışmalarında iyi bir güvenlik profili gösterirken gerçekleşti.
Gelecekteki kanser tedavileri için anlamı
Bu çalışma, agresif meme kanserlerini sadece tümör hücrelerine doğrudan saldırarak değil, onları çevreleyen bağışıklık hücrelerini yeniden eğiterek de tedavi etmenin mümkün olabileceğini gösteriyor. Işıkla aktive edilen terapiyi, kontrol noktası engellemeyi ve genetik yeniden programlamayı tek bir akıllı nanomisel içinde paketleyerek araştırmacılar, baskıcı bir tümör mahallesini kalıcı bağışıklık savunmasını destekleyen bir ortama dönüştüren koordineli bir itki yarattı. Bu stratejinin hastalara ulaşmadan önce çok daha fazla test gerektireceği doğruyken, yaklaşım primer ve metastatik tümörleri uzun vadeli kontrol altında tutmak için bağışıklık ortamını yeniden şekillendiren gelecekteki tedaviler için bir yol haritası sunuyor.
Atıf: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
Anahtar kelimeler: meme kanseri immünoterapisi, nanotıp, tümör mikroçevresi, makrofaj yeniden programlama, dendritik hücre aktivasyonu