Clear Sky Science · he
ננו‑מיצלות מתכנתות מחדש את מערכת החיסון המיאלואידית לשליטה ממושכת בסרטן השד הראשוני ומטסטטי
דרך חדשה לסייע למערכת החיסון להילחם בסרטן השד
רוב טיפולי הסרטן מתמקדים בהרוגת תאי הגידול ישירות, אך גידולים רבים שורדים על ידי הפיכת תאי החיסון של הגוף לבעלי ברית שקטים. המחקר מתאר תרופה זעירה ומתכנתת שמטרתה להפוך את התאים הללו חזרה ללוחמים נגד סרטן, ולספק שליטה ממושכת על סוגי סרטן שד אגרסיביים שהתפשטו לאיברים אחרים.
למה סרטן השד כל כך קשה לריפוי
סרטן השד הוא הסרטן הנפוץ ביותר שנאבחן בנשים, והתכונה הקטלנית שלו היא נטייתו להתפשט, במיוחד לריאות. תת‑סוג אחד, סרטן שד טריפל‑נגטיבי, קשה במיוחד לטיפול כי הוא חסר מטרות הורמונליות וגידול נפוצות. אפילו אימונותרפיות מודרניות שחוסמות את "המגן" PD‑L1 על תאי הגידול מסייעות רק לחלק מהחולים ולעתים כושלות בהארכת ההישרדות. סיבה מרכזית לכך היא מיקרו‑סביבת הגידול — השכונה המיידית של תאים ומולקולות סביב הסרטן — שמלאה בתאי חיסון שתוכנתו לדכא במקום לתמוך במתקפות נגד הגידול.
השפעתם המוסתרת של תאי התמיכה סביב הגידול
מבין התאים המקיפים הללו, שני סוגים של תאים מיאלואידיים ממלאים תפקיד משמעותי: תאים דנדריטיים ומאקרופאגים. בתנאים בריאים, תאים דנדריטיים פועלים כמשמרים, אוספים מולקולות חשודות ומציגים אותן לתאי T כדי להצית מתקפת חיסון ממוקדת. מאקרופאגים יכולים לתמוך בדלקת (בדומה ל‑M1) ולסייע בניקוי איומים, או להרגיע ולקדם תיקון רקמות (בדומה ל‑M2). בגידולי שד של מטופלות ובמודלים בעכברים, המחברים מצאו פחות תאים דנדריטיים בוגרים ולעומת זאת שפע של מאקרופאגים בדמיון ל‑M2. מאקרופאגים אלה, ״שומרי השלום״, נקשרו לפלישה נמוכה של תאי T ולתוצאות קליניות גרועות, מה שמרמז שאם אפשר יהיה לתכנת אותם חזרה ללוחמים, הדבר עשוי לשחרר תגובות חיסוניות עוצמתיות ועמידות יותר נגד הסרטן.
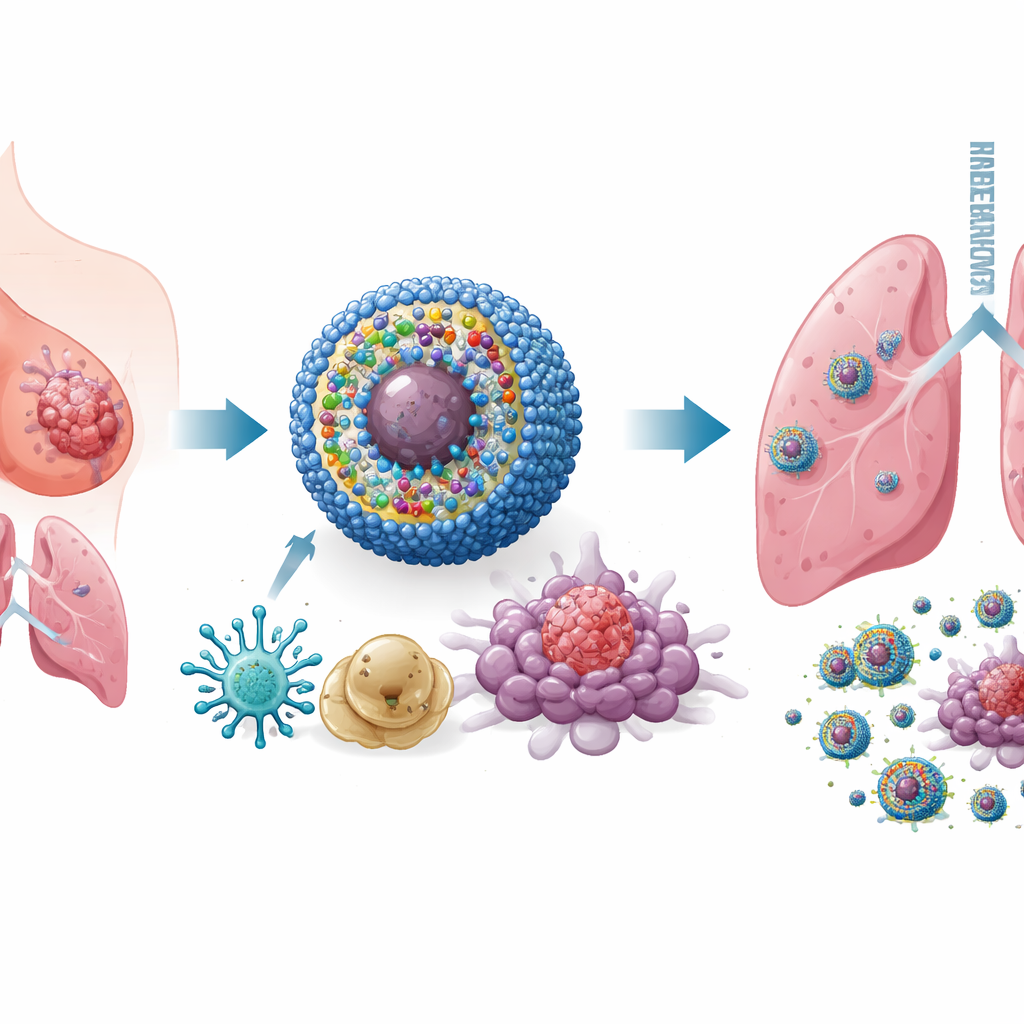
עיצוב ננו‑תרופה חכמה ורב‑כלי
כדי להתמודד עם הבעיה, החוקרים בנו מערכת נשיאה בננו‑קנה מידה שהם קוראים לה IPANP — מיצלות כדוריות זעירות שמסוגלות להסתובב במחזור הדם ולהצטבר בגידולים. כל ננו‑מיצלה נושאת שלושה מרכיבים. ראשית, צבע פעיל לאור (IR825) שברגע שמוארת באור תת‑אדום קרוב מבחוץ, יוצר מולקולות תגובתיות שמפעילות סטרס והרג תאי גידול באופן שהופך אותם בולט במיוחד למערכת החיסון. שנית, נוגדן נגד PD‑L1, שמסייע להסרת הברקס המולקולרי שבו משתמשים התאים הסרטניים כדי לכבות תאי T. שלישית, חתיכת חומר גנטי קצרה (antagomiR‑182) שחוסמת מיקרו‑RNA, miR‑182, הנמצא ברמות גבוהות במאקרופאגים המקדמים גידול. הנשא רגיש לסביבה הכימית הריאקטיבית בתוך הגידול, ולכן משחרר את המטען בעיקר במקום הנדרש, מה שמגביל חשיפה לרקמות בריאות.
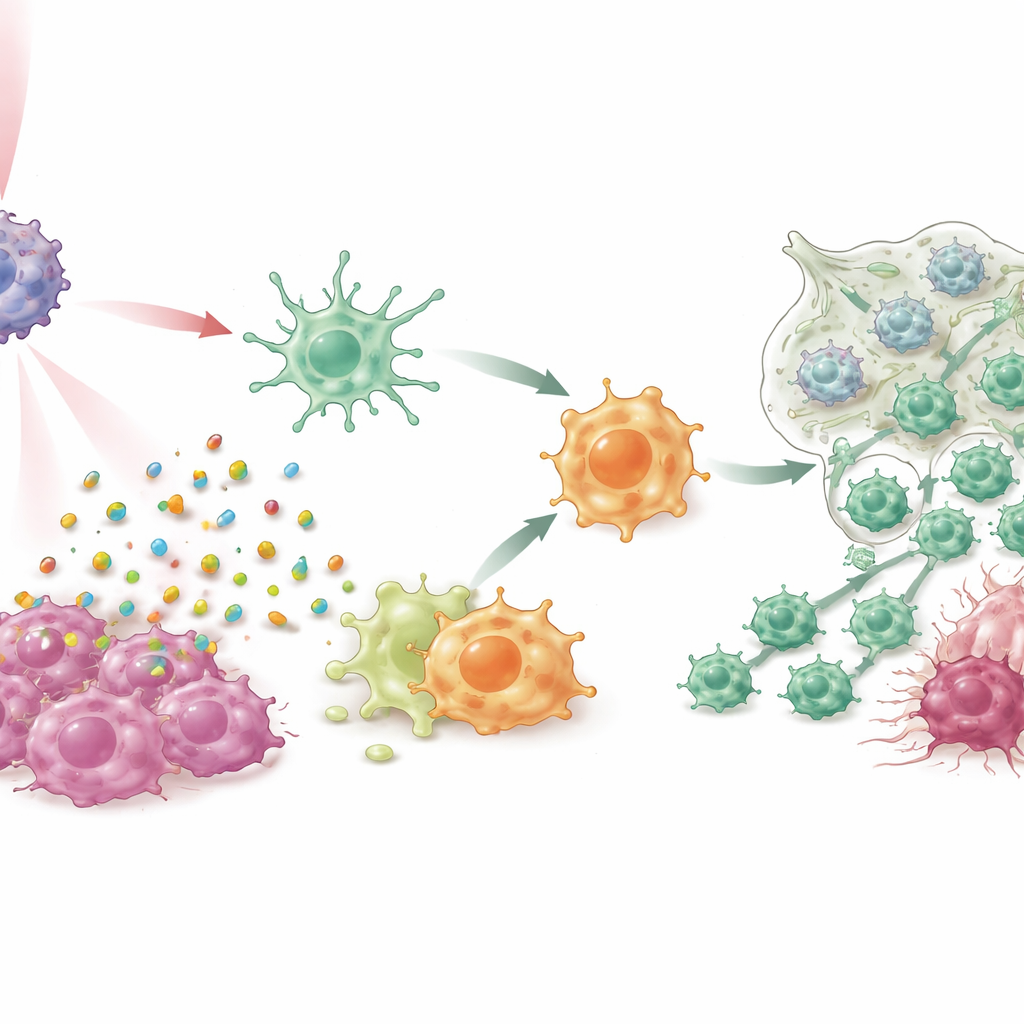
הפיכת תאי דיכוי לתוקפים
בתרביות תאים ובכמה מודלים של עכברים לסרטן שד, כולל סוגים קשים כמו הטריפל‑נגטיבי ומערכות גידול ספונטניות, IPANP בשילוב עם אור תת‑אדום עדין עשה יותר מסתם הקטנת גידולים. הצבע המופעל באור גרם לתאי הסרטן למות באופן "אימונוגני", כשהם משחררים אותות סכנה שדוחפים את התאים הדנדריטיים לבגרות ולהצגת שברי גידול ל‑T בצורה יעילה יותר. במקביל, חסימת miR‑182 במאקרופגים הסירה מעצור על מסלול חישה מרכזי (TLR4/MYD88/NF‑κB), ודחפה אותם ממצב תומך‑גידול בדומה ל‑M2 למצב דלקתי ותומך בפינוי בדומה ל‑M1. כאשר שני סוגי התאים המיאלואידיים הללו שונו תפקיד, יותר תאי T קטלניים חדרו לגידולים, הפכו פעילים יותר והיו פחות מועדים לשיתוק מעייפות. התוצאה הייתה שליטה חזקה על הגידולים הראשוניים, ירידה חדה במטסטזות ריאתיות והארכת חיי החיות המטופלות.
הגנה ממושכת ואיתותים להבטחה בעולם האמיתי
בממצא בולט, עכברים שהגידולים שלהם הוסרו על‑ידי IPANP ואור היו מוגנים כאשר החוקרים ניסו לשתל שוב גידולים חדשים חודשים לאחר מכן, מה שמעיד על יצירת זיכרון חיסוני דומה לזה שמיוצר על‑ידי חיסון. הצוות גם בחן את השיטה על דגימות סרטן שד שהוסרו טרי ממטופלות, שהוחזקו כחתיכות רקמה חיות, ובשתלי גידול נגזרים מחולים בעכברים עם מערכת חיסון מועתקת לבני אדם. בהגדרות אלה הטיפול שוב דחף תאים דנדריטיים ומאקרופאגים למצבים פעילים יותר ונגד‑גידוליים, צמצם אותות שמקדמים גדילה, הגביר מולקולות דלקתיות מועילות, הגדיל את נוכחות תאי T הקטלניים וגרם למות תאי גידול — וכל זאת תוך הצגת פרופיל בטיחות טוב במחקרים ארוכי‑טווח בחיות.
מה זה יכול לומר על טיפולי סרטן בעתיד
העבודה מראה שאולי ניתן לטפל בסוגים אגרסיביים של סרטן השד לא רק על‑ידי תקיפת תאי הגידול ישירות, אלא על‑ידי חינוך מחדש של תאי החיסון שמקיפים אותם. על‑ידי אריזה של טיפול פעיל‑אור, חסימת נקודות עצירה וגיוס תכנות גנטי לתוך ננו‑מיצלה חכמה אחת, יצרו החוקרים דחיפה מתואמת שהפכה שכונת גידול מדכאת לשכונה שתומכת בהגנה חיסונית ממושכת. למרות שנדרש עוד הרבה מחקר לפני שהאסטרטגיה הזו תוכל להגיע לחולים, היא מציעה תבנית לטיפולים עתידיים שמשנים את סביבת החיסון כדי לשמור על שליטה ממושכת גם על גידולים ראשוניים וגם על מטסטזות.
ציטוט: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
מילות מפתח: אימונותרפיה של סרטן השד, ננרפואה, מיקרו‑סביבת הגידול, תכנות מחדש של מאקרופאגים, הפעלת תאים דנדריטיים