Clear Sky Science · sv
Programmerbara nanomiceller omkopplar myeloid immunitet för bestående kontroll av primär och metastaserande bröstcancer
En ny metod för att hjälpa immunförsvaret mot bröstcancer
De flesta cancerbehandlingar fokuserar på att döda tumörceller direkt, men många tumörer överlever genom att i tysthet omvandla kroppens egna immunceller till allierade. Denna studie beskriver ett litet, programmerbart läkemedel som syftar till att vända dessa celler tillbaka till cancerbekämpare och därigenom erbjuda långvarig kontroll över aggressiv bröstcancer som spritt sig till andra organ.
Varför bröstcancer kan vara svår att bota
Bröstcancer är den vanligaste diagnostiserade cancersjukdomen hos kvinnor, och dess dödligaste egenskap är dess benägenhet att sprida sig, särskilt till lungorna. En undergrupp, trippelnegativ bröstcancer, är särskilt svårbehandlad eftersom den saknar vanliga hormon- och tillväxtfaktormål. Även moderna immunoterapier som blockerar tumörcellernas PD‑L1 "sköld" hjälper bara en del av patienterna och förlänger ofta inte överlevnaden. En viktig orsak är tumörens mikromiljö — den omedelbara omgivningen av celler och molekyler kring cancern — som är full av immunceller som omprogrammerats för att undertrycka snarare än stödja antitumörsangrepp.
Den dolda påverkan från stödjeceller runt tumörer
Bland dessa omkringliggande celler spelar två typer av myeloida celler en oproportionerligt stor roll: dendritiska celler och makrofager. I friska förhållanden fungerar dendritiska celler som vaktposter, plockar upp misstänkta molekyler och visar dem för T‑celler för att utlösa ett riktat immunangrepp. Makrofager kan antingen stödja inflammation (M1‑liknande) och hjälpa till att rensa hot, eller dämpa reaktionen och främja vävnadsreparation (M2‑liknande). I brösttumörer från patienter och i musemodeller fann författarna färre mogna dendritiska celler och ett överflöd av M2‑liknande makrofager. Dessa "fredsstiftande" makrofager var kopplade till låg T‑cellsinfiltration och sämre utfall, vilket tyder på att om forskare kunde omkoppla dessa celler tillbaka till kämpar så skulle de kanske kunna låsa upp mer kraftfulla och bestående immunrespons mot cancer.
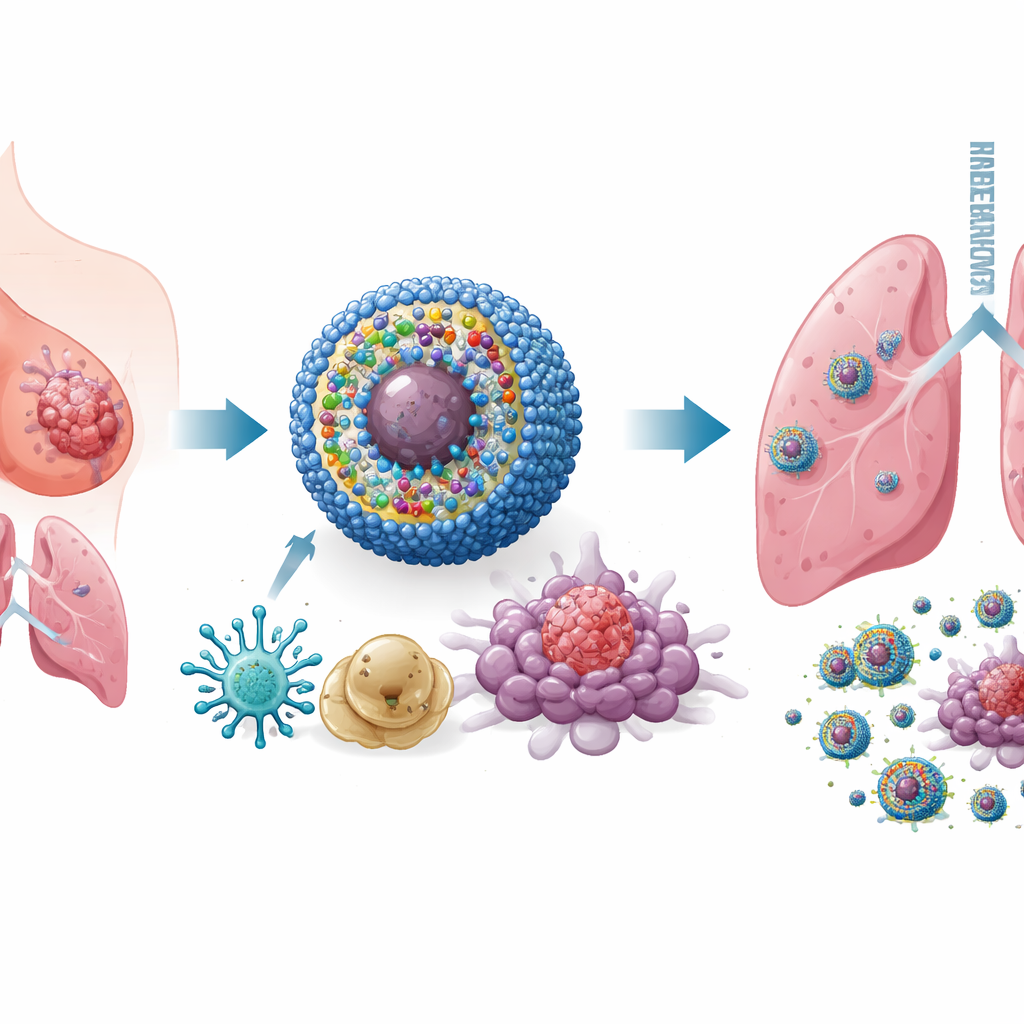
Att designa en smart, multifunktions nanomedicin
För att tackla detta problem byggde forskarna ett nanoskaligt transportsystem de kallar IPANP — små sfäriska miceller som cirkulerar i blodomloppet och ackumuleras i tumörer. Varje nanomicell bär på tre komponenter. För det första en ljusaktiverad färg (IR825) som, när den belyses med nära‑infrarött ljus utifrån kroppen, genererar reaktiva molekyler som stressar och dödar tumörceller på ett sätt som gör dem lättare för immunsystemet att upptäcka. För det andra en antikropp mot PD‑L1, som hjälper till att ta bort den molekylära broms tumörer använder för att stänga av T‑celler. För det tredje en kort bit genetiskt material (antagomiR‑182) som blockerar en mikroRNA, miR‑182, som finns i höga nivåer i tumörfrämjande makrofager. Bäraren är känslig för den kemiskt reaktiva miljön inne i tumörer, så den släpper sin last främst där den behövs och begränsar exponering för frisk vävnad.
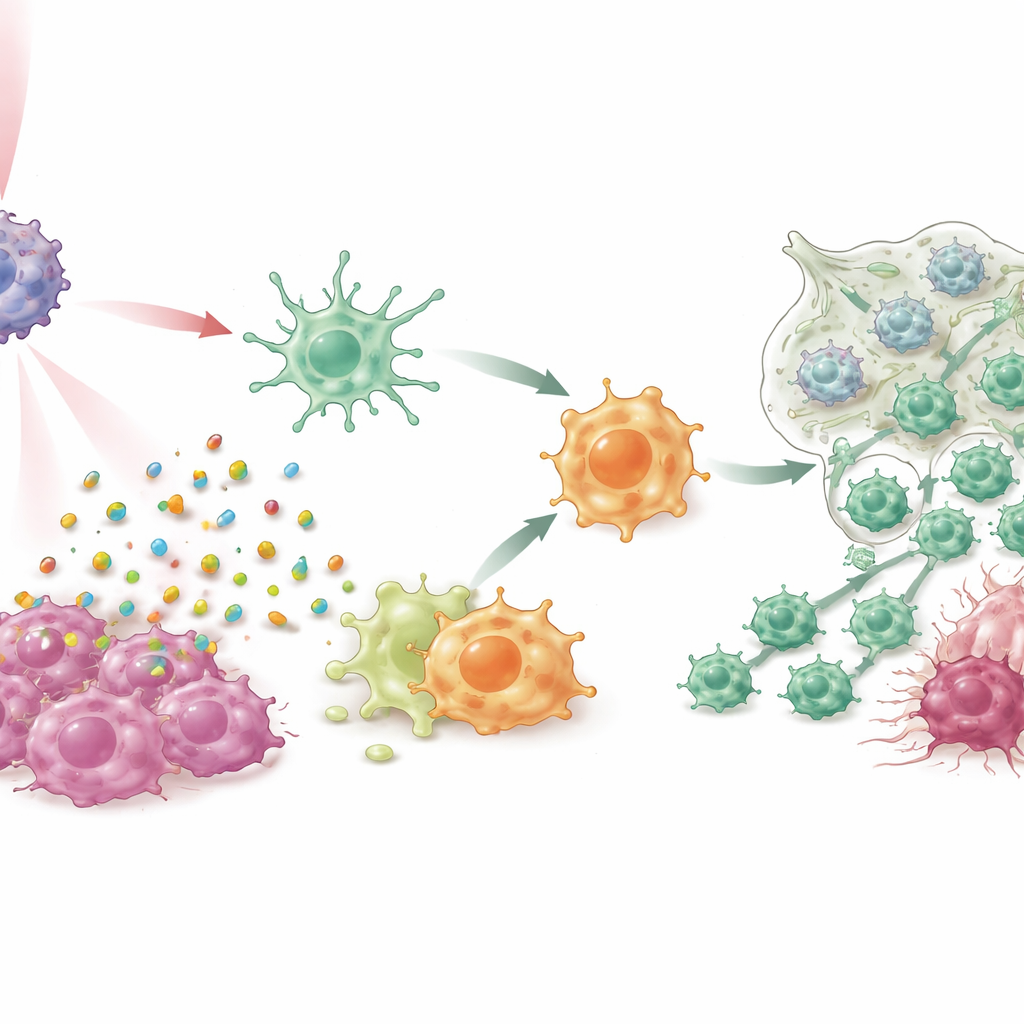
Att förvandla suppressorceller till angripare
I cellkulturer och i flera musemodeller av bröstcancer, inklusive svårbehandlade trippelnegativa och spontana tumörsystem, gjorde IPANP i kombination med svagt nära‑infrarött ljus mer än att bara krympa tumörer. Den ljusaktiverade färgen orsakade att cancerceller dog på ett "immunogent" sätt, vilket spillde ut larmsignaler som drev dendritiska celler att mogna och presentera tumörfragment mer effektivt för T‑celler. Samtidigt lyfte blockering av miR‑182 i makrofager en broms på en viktig sensorsignalväg (TLR4/MYD88/NF‑κB), vilket knuffade dem från det M2‑liknande, tumörstödjande tillståndet mot ett M1‑liknande, inflammatoriskt tillstånd. När dessa två myeloida celltyper skiftade roller, strömmade fler mördande T‑celler in i tumörer, blev mer aktiva och var mindre benägna att stängas av av utmattning. Resultatet var stark kontroll av primärtumörer, kraftiga minskningar av lungmetastaser och förlängd överlevnad hos behandlade djur.
Bestående skydd och tecken på verklig potential
Anmärkningsvärt var att möss vars tumörer rensats av IPANP och ljus var skyddade när forskarna försökte implantera nya tumörer flera månader senare, vilket indikerar bildandet av immunologiskt minne liknande det som skapas av ett vaccin. Teamet testade också metoden på nyligen borttaget bröstcancervävnad från patienter, hållna vid liv som små vävnadsfragment, och i patient‑härledda tumörimplantat i humaniserade möss. I dessa system drev behandlingen återigen dendritiska celler och makrofager mot mer aktiva, antitumöriska tillstånd, minskade tillväxtfrämjande signaler, ökade gynnsamma inflammatoriska molekyler, ökade förekomsten av mördande T‑celler och orsakade tumörcellsdöd — allt medan god säkerhet visades i långtidsstudier på djur.
Vad detta kan betyda för framtida cancerbehandling
Detta arbete visar att det kan vara möjligt att behandla aggressiva bröstcancerformer inte bara genom att angripa tumörceller direkt, utan genom att omskola de immunceller som omger dem. Genom att paketera ljusaktiverad terapi, checkpoint‑blockering och genetisk omprogrammering i en smart nanomicell skapade forskarna en samordnad drivkraft som gjorde om en suppressiv tumöromgivning till en som stödjer bestående immunförsvar. Även om mycket mer forskning behövs innan denna strategi kan nå patienter, erbjuder den en ritning för framtida behandlingar som omformar immummiljön för att hålla både primära och metastaserande tumörer under långsiktig kontroll.
Citering: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
Nyckelord: immunoterapi mot bröstcancer, nanomedicin, tumörmikromiljö, omprogrammering av makrofager, aktivering av dendritiska celler