Clear Sky Science · ru
Программируемые наномицеллы перенастраивают миелоидный иммунитет для длительного контроля первичного и метастатического рака молочной железы
Новый способ помочь иммунной системе бороться с раком молочной железы
Большинство методов лечения рака направлены на прямое уничтожение опухолевых клеток, но многие опухоли выживают, тихо превращая собственные иммунные клетки организма в союзников. В этом исследовании описывается крошечный программируемый препарат, который стремится вернуть этим клеткам роль борцов с раком, обеспечивая длительный контроль агрессивных форм рака молочной железы, распространившихся в другие органы.
Почему рак молочной железы бывает трудно вылечить
Рак молочной железы — наиболее часто диагностируемый рак у женщин, а его смертельная черта — склонность к метастазированию, особенно в лёгкие. Один из подтипов, тройной отрицательный рак молочной железы, особенно трудно поддаётся лечению, поскольку в нём отсутствуют обычные гормональные и факторные мишени. Даже современные иммунотерапии, блокирующие «щит» PD‑L1 на опухолевых клетках, помогают лишь части пациентов и часто не продлевают выживание. Главная причина — микроокружение опухоли, то есть ближайшее соседство клеток и молекул вокруг опухоли, которое заполнено иммунными клетками, перепрограммированными на подавление, а не на поддержку антиопухолевых атак.
Скрытое влияние клеток‑сателлитов вокруг опухолей
Среди окружающих клеток два типа миелоидных клеток играют ключевую роль: дендритные клетки и макрофаги. В норме дендритные клетки действуют как стражи, улавливая подозрительные молекулы и демонстрируя их Т‑клеткам, чтобы вызвать целенаправленную иммунную атаку. Макрофаги могут либо поддерживать воспаление (подобно M1) и помогать устранять угрозы, либо успокаивать процесс и способствовать восстановлению тканей (подобно M2). В опухолях молочной железы у пациентов и в мышиных моделях авторы обнаружили меньше зрелых дендритных клеток и избыток макрофагов M2‑подобного типа. Эти «миротворческие» макрофаги связывали с плохой инфильтрацией Т‑клеток и худшими исходами, что указывает на то, что перенастройка этих клеток в борцов может открыть более мощные и долговечные иммунные ответы против рака.
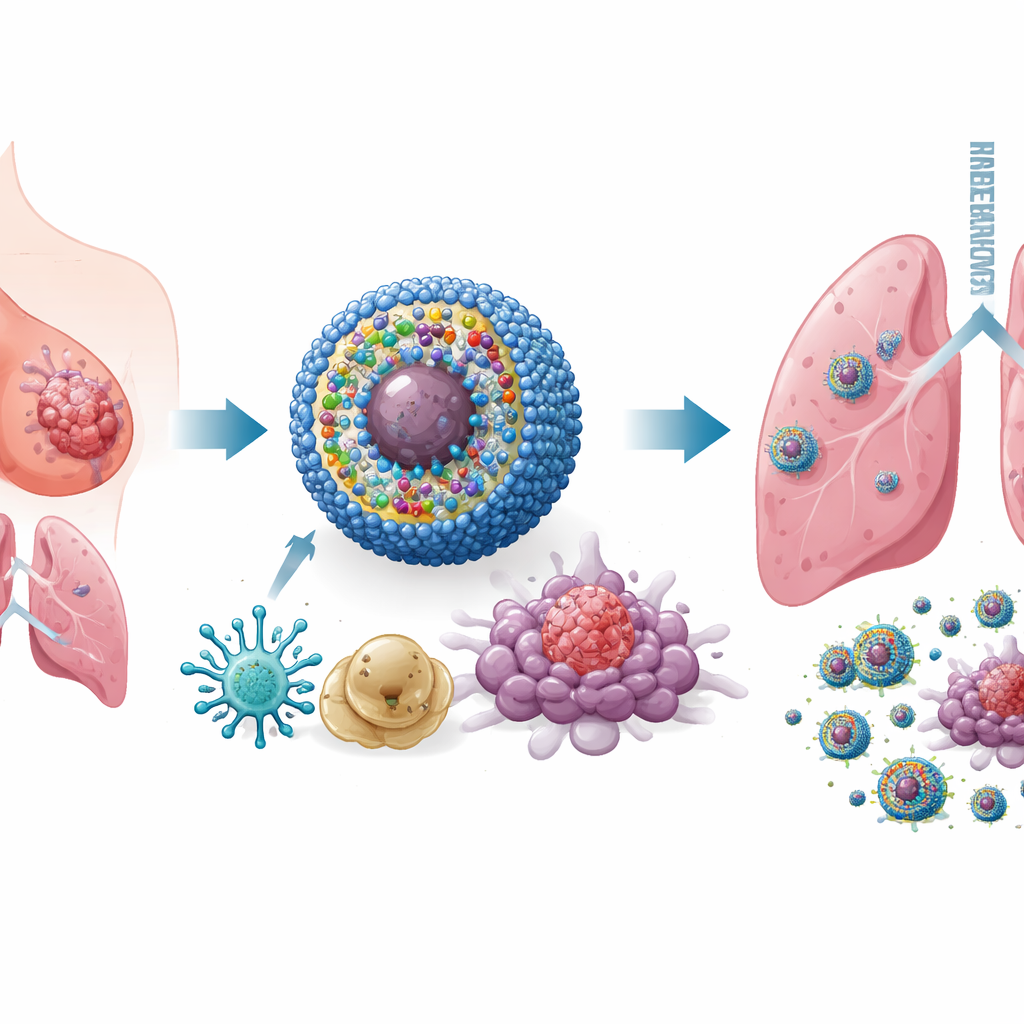
Создание умной многокомпонентной наномедицины
Чтобы решить эту задачу, исследователи создали наносистему доставки, которую назвали IPANP — крошечные сферические мицеллы, циркулирующие в кровотоке и накапливающиеся в опухолях. Каждая наномицелла несёт три компонента. Во‑первых, светочувствительный краситель (IR825), который при облучении ближним инфракрасным светом снаружи генерирует реактивные молекулы, создающие стресс и убивающие опухолевые клетки таким образом, что те становятся особенно заметны для иммунной системы. Во‑вторых, антитело против PD‑L1, которое помогает снимать молекулярный тормоз, используемый опухолями для выключения Т‑клеток. В‑третьих, короткий фрагмент генетического материала (antagomiR‑182), блокирующий микрорНК miR‑182, обнаруживаемую в высокой концентрации в макрофагах, поддерживающих опухоль. Несущий компонент чувствителен к химически реактивной среде внутри опухолей, поэтому он высвобождает груз преимущественно там, где это нужно, ограничивая воздействие на здоровые ткани.
Перевод подавляющих клеток в атакующие
В культурах клеток и в нескольких мышиных моделях рака молочной железы, включая трудноизлечимые тройные отрицательные и спонтанные опухолевые модели, IPANP в сочетании с мягким ближним инфракрасным светом сделал больше, чем просто уменьшил опухоли. Светоактивируемый краситель вызвал гибель раковых клеток в «иммуногенном» режиме, выпустив сигналы опасности, которые стимулировали созревание дендритных клеток и более эффективное представление фрагментов опухоли Т‑клеткам. Одновременно блокирование miR‑182 в макрофагах сняло тормоз с ключевого пути распознавания (TLR4/MYD88/NF‑κB), подтолкнув их от M2‑подобного, поддерживающего опухоль состояния к M1‑подобному, провоспалительному состоянию. По мере того как эти два типа миелоидных клеток меняли роль, в опухоли хлынуло больше убивающих Т‑клеток, они стали более активными и реже выключались из‑за истощения. Результатом стал сильный контроль первичных опухолей, резкое снижение метастазов в лёгких и продление выживания лечёных животных.
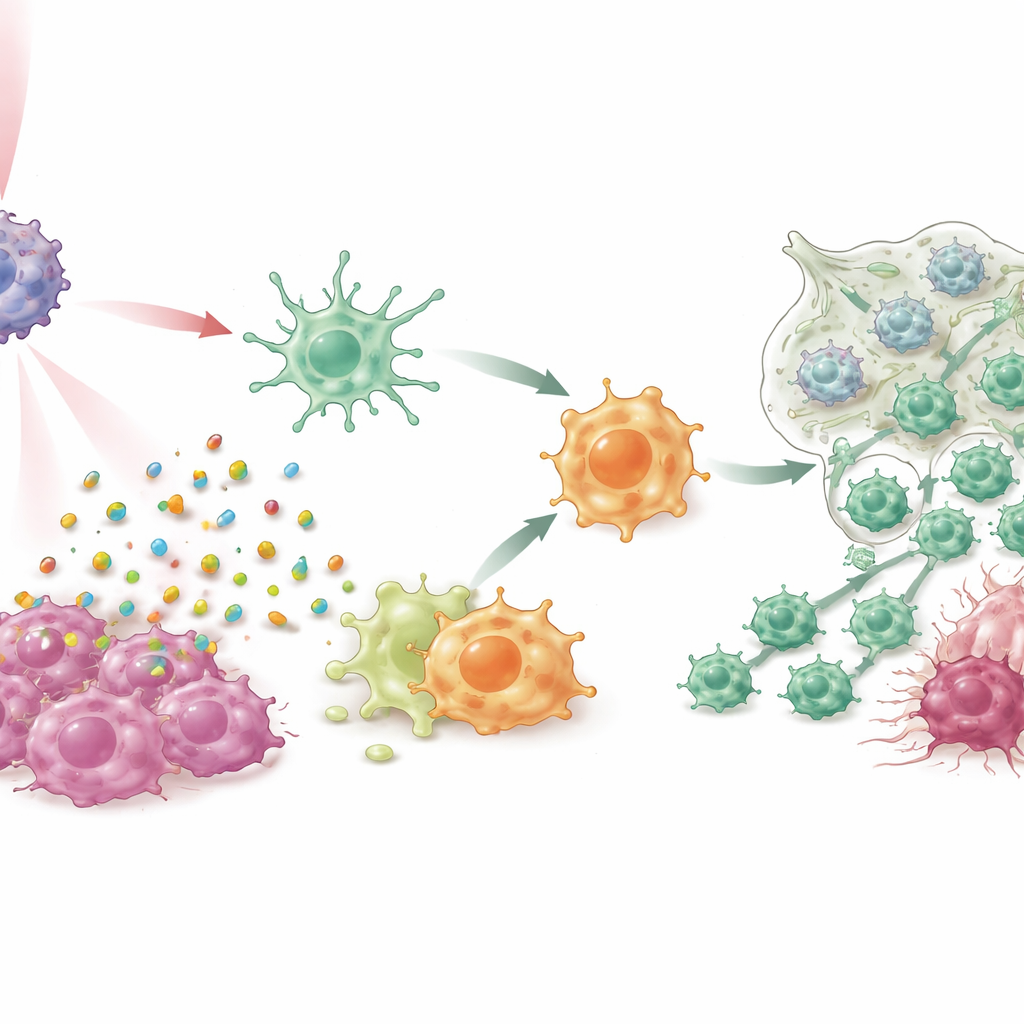
Длительная защита и признаки клинического потенциала
Поразительно, что мыши, у которых опухоли были устранены с помощью IPANP и света, оказались защищены при попытке реимплантации новых опухолей через несколько месяцев, что свидетельствует о формировании иммунной памяти, похожей на вакцинную. Команда также протестировала подход на свежесрезанных образцах рака молочной железы от пациентов, поддерживаемых в живом состоянии в виде небольших фрагментов ткани, и на трансплантатах опухолей, полученных от пациентов, в гуманизированных мышах. В этих условиях лечение снова переводило дендритные клетки и макрофаги в более активные антиопухолевые состояния, уменьшало сигналы, способствующие росту, усиливало полезные провоспалительные молекулы, повышало присутствие убивающих Т‑клеток и вызывало гибель опухолевых клеток — всё это при хорошей безопасности в долгосрочных исследованиях на животных.
Что это может значить для будущего лечения рака
Эта работа показывает, что возможно лечить агрессивные формы рака молочной железы не только за счёт прямой атаки опухолевых клеток, но и путём переобучения окружающих их иммунных клеток. Упаковав светоиндуцируемую терапию, блокирование иммунных контрольных точек и генетическую перепрограммовку в одну умную наномицеллу, исследователи создали скоординированный импульс, который превратил подавляющее опухолевое окружение в такое, что поддерживает длительную иммунную защиту. Хотя до применения у пациентов необходимо ещё много испытаний, это даёт шаблон для будущих терапий, которые будут перестраивать иммунную среду, чтобы надолго удерживать под контролем как первичные, так и метастатические опухоли.
Цитирование: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
Ключевые слова: иммунотерапия рака молочной железы, наномедицина, микроокружение опухоли, перепрограммирование макрофагов, активация дендритных клеток