Clear Sky Science · nl
Programmeerbare nanomicellen herschakelen myeloïde immuniteit voor duurzame controle van primaire en metastatische borstkanker
Een nieuwe manier om het immuunsysteem te helpen borstkanker te bestrijden
De meeste kankerbehandelingen richten zich op het direct doden van tumorcellen, maar veel tumoren overleven door stilletjes de eigen immuuncellen van het lichaam tot bondgenoten te maken. Deze studie beschrijft een klein, programmeerbaar middel dat erop gericht is die cellen weer terug te zetten in strijders tegen kanker, en zo langdurige controle biedt over agressieve borstkankers die naar andere organen zijn uitgezaaid.
Waarom borstkanker zo moeilijk te genezen kan zijn
Borstkanker is de meest gediagnosticeerde kanker bij vrouwen en het dodelijkste kenmerk is het vermogen om uit te zaaien, vooral naar de longen. Een subtype, triple-negatieve borstkanker, is bijzonder moeilijk te behandelen omdat het ontbreekt aan de gebruikelijke hormoon- en groeifactortargets. Zelfs moderne immunotherapieën die het PD-L1 "schild" op tumoren blokkeren helpen maar een deel van de patiënten en verlengen vaak de overleving niet. Een belangrijke reden is de tumormicro-omgeving — de directe buurt van cellen en moleculen rond de tumor — die vol zit met immuuncellen die zijn geherprogrammeerd om te onderdrukken in plaats van aan te vallen.
De verborgen invloed van ondersteunende cellen rond tumoren
Onder deze omringende cellen spelen twee typen myeloïde cellen een buitenproportionele rol: dendritische cellen en macrofagen. Onder gezonde omstandigheden fungeren dendritische cellen als wachters: ze nemen verdachte moleculen op en tonen die aan T‑cellen om een gerichte immuunreactie te activeren. Macrofagen kunnen ontsteking ondersteunen (M1‑achtig) en helpen bedreigingen op te ruimen, of juist kalmeren en weefselherstel bevorderen (M2‑achtig). In borstkankers van patiënten en muismodellen vonden de auteurs minder rijpe dendritische cellen en een overvloed aan M2‑achtige macrofagen. Deze "vredebewarende" macrofagen waren gekoppeld aan slechte T‑celinfiltratie en slechtere uitkomsten, wat suggereert dat als wetenschappers deze cellen weer tot strijders kunnen maken, zij krachtigere en duurzamere immuunreacties tegen kanker zouden kunnen ontgrendelen.
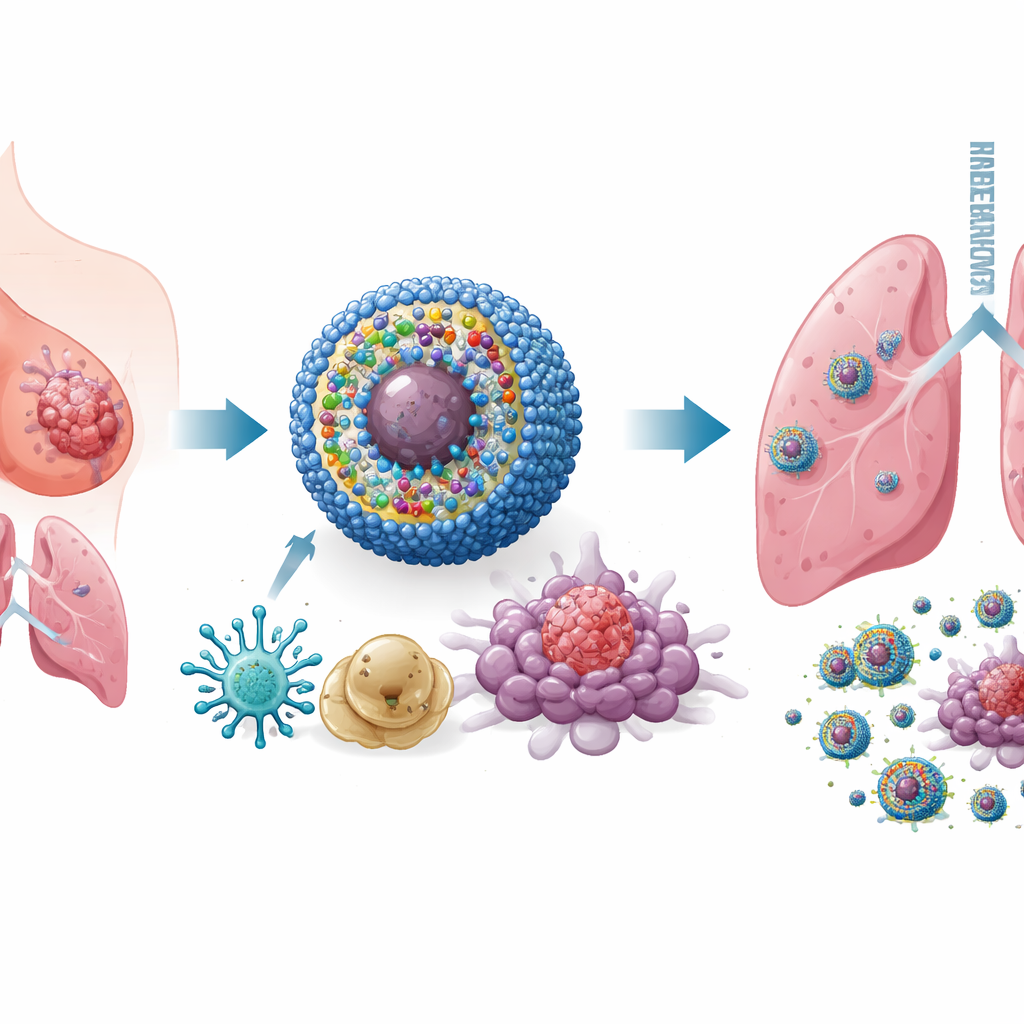
Ontwerp van een slimme, multifunctionele nanomedicine
Om dit probleem aan te pakken bouwden de onderzoekers een nanoschaal afleveringssysteem dat ze IPANP noemen — kleine sferische micellen die in de bloedbaan circuleren en zich in tumoren ophopen. Elke nanomicel draagt drie componenten. Ten eerste een licht‑geactiveerde kleurstof (IR825) die, wanneer belicht met nabij-infrarood licht van buiten het lichaam, reactieve deeltjes genereert die tumorcellen zodanig beschadigen dat ze het immuunsysteem sterk aantrekken. Ten tweede een antilichaam tegen PD‑L1, dat helpt een moleculaire rem te verwijderen die tumoren gebruiken om T‑cellen uit te schakelen. Ten derde een kort stuk genetisch materiaal (antagomiR‑182) dat een microRNA, miR‑182, blokkeert dat in hoge niveaus voorkomt in tumorpromoterende macrofagen. De drager is gevoelig voor de chemisch reactieve omgeving binnen tumoren, zodat het zijn lading voornamelijk vrijgeeft waar het nodig is, waardoor blootstelling van gezond weefsel beperkt blijft.
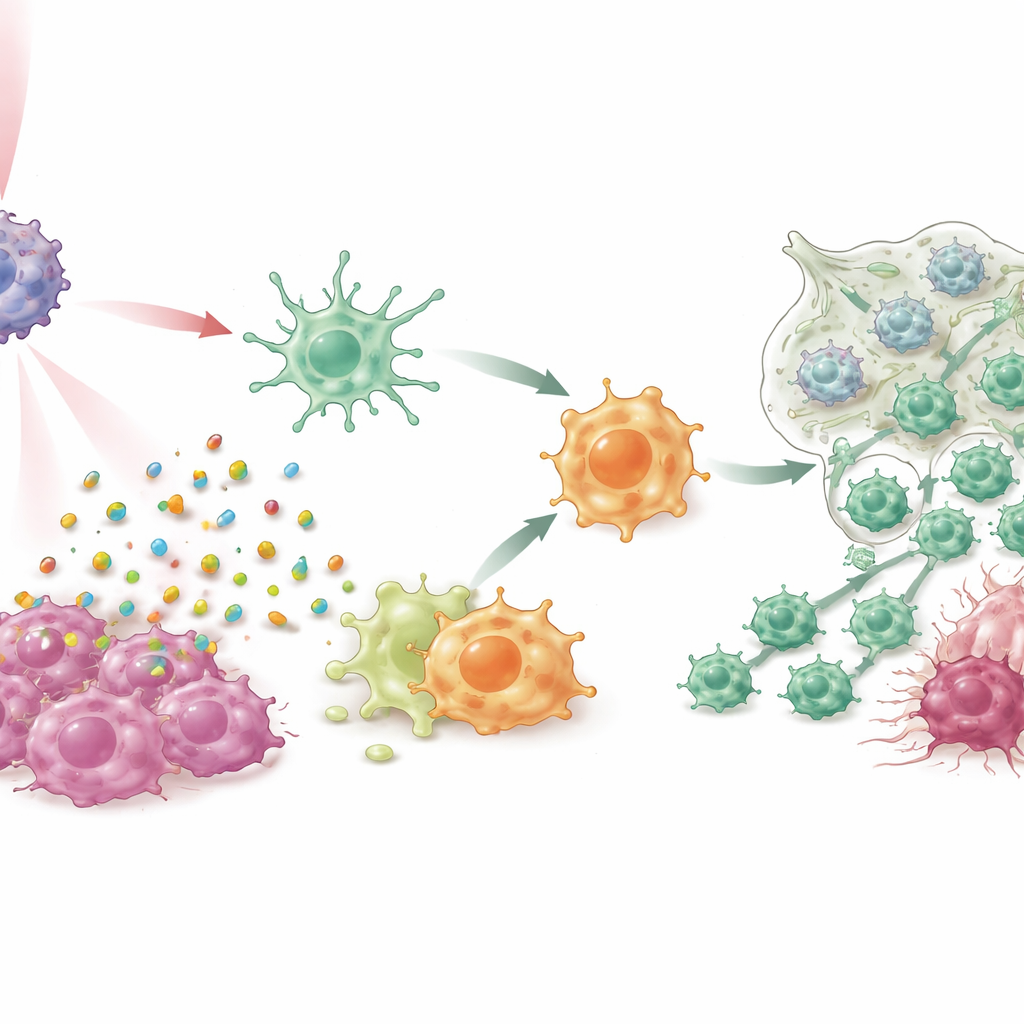
Onderdrukkende cellen veranderen in aanvallers
In celkweken en meerdere muismodellen van borstkanker, waaronder moeilijk te behandelen triple‑negatieve en spontane tumormodellen, deed IPANP in combinatie met zacht nabij-infrarood licht meer dan alleen tumoren verkleinen. De licht‑geactiveerde kleurstof veroorzaakte dat kankercellen op een "immunogene" manier stierven, waarbij alarmsignalen vrijkwamen die dendritische cellen aanzetten te rijpen en tumordeeltjes efficiënter aan T‑cellen te presenteren. Tegelijkertijd hief het blokkeren van miR‑182 in macrofagen een rem op een belangrijke sensorsignaalweg (TLR4/MYD88/NF‑κB), waardoor ze van de M2‑achtige, tumorondersteunende toestand naar een M1‑achtige, pro‑ontstekingsachtige toestand werden geduwd. Terwijl deze twee myeloïde celtypes van rol veranderden, stroomden er meer cytotoxische T‑cellen de tumoren binnen, werden ze actiever en waren ze minder geneigd uit te putten. Het resultaat was sterke controle van primaire tumoren, scherpe verminderingen van longmetastasen en verlengde overleving bij behandelde dieren.
Langdurige bescherming en tekenen van praktische beloften
Opvallend was dat muizen wier tumoren waren uitgeroeid door IPANP en licht beschermd waren toen onderzoekers maanden later probeerden nieuwe tumoren te herimplanteren, wat wijst op de vorming van immuungeheugen vergelijkbaar met dat van een vaccin. Het team testte de benadering ook op recent verwijderde borstkankerfragmenten van patiënten, levend gehouden als kleine weefselstukjes, en in patiënt-afgeleide tumorgrafts in gehumaniseerde muizen. In deze settings duwde de behandeling opnieuw dendritische cellen en macrofagen in actievere, antitumorale toestanden, verminderde groeibevorderende signalen, verhoogde gunstige ontstekingsmoleculen, nam de aanwezigheid van cytotoxische T‑cellen toe en veroorzaakte tumorceldood—en dat alles terwijl lange‑termijn dierstudies een goede veiligheid aangaven.
Wat dit kan betekenen voor toekomstige kankerbehandeling
Dit werk laat zien dat het mogelijk kan zijn agressieve borstkankers te behandelen niet alleen door tumorcellen direct aan te vallen, maar door de immuuncellen die hen omringen te heropvoeden. Door lichtgeactiveerde therapie, checkpoint‑blokkering en genetische herscholing in één slimme nanomicel te combineren, creëerden de onderzoekers een gecoördineerde impuls die een onderdrukkende tumoromgeving veranderde in een omgeving die duurzame immuunafweer ondersteunt. Hoewel er nog veel meer testen nodig zijn voordat deze strategie patiënten kan bereiken, biedt het een blauwdruk voor toekomstige behandelingen die de immuunomgeving herequiveren om zowel primaire als metastatische tumoren op de lange termijn onder controle te houden.
Bronvermelding: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
Trefwoorden: immunotherapie bij borstkanker, nanomedicine, tumormicro-omgeving, herschakeling van macrofagen, activatie van dendritische cellen