Clear Sky Science · ja
プログラム可能なナノミセルが骨髄系免疫を再配線し、原発および転移性乳がんの持続的制御を実現する
免疫系が乳がんと戦うのを助ける新たな手法
多くのがん治療は腫瘍細胞を直接殺すことに焦点を当てますが、多くの腫瘍は身体の免疫細胞を静かに味方に変えることで生き残ります。本研究は、そうした細胞を再びがんと戦う側に戻すことを目指した、小さくプログラム可能な薬剤を紹介しており、他の臓器に転移した攻撃的な乳がんを長期にわたって制御する可能性を提示します。
乳がんが治りにくい理由
乳がんは女性で最も一般的に診断されるがんであり、最も致死的なのは特に肺への転移しやすさです。サブタイプの一つであるトリプルネガティブ乳がんは、一般的なホルモンや成長因子の標的がなく、特に治療が難しい。腫瘍細胞のPD‑L1という「盾」をブロックする現代の免疫療法でさえ、患者のごく一部にしか効果がなく、多くの場合生存期間を延ばせません。主要な原因の一つは腫瘍の微小環境――がんの周囲にある細胞や分子の局所的な状態――で、そこには抗腫瘍攻撃を抑えるように書き換えられた免疫細胞が大勢詰まっています。
腫瘍周辺の補助細胞がもたらす隠れた影響
こうした周辺細胞の中で、二種類の骨髄系細胞が大きな役割を担います:樹状細胞とマクロファージです。正常な状態では、樹状細胞は見張り役として働き、疑わしい分子を取り込みそれをT細胞に提示して標的を絞った免疫応答を引き起こします。マクロファージは炎症を支持して脅威を排除する(M1様)こともあれば、鎮めて組織修復を促す(M2様)こともあります。患者やマウスモデルの乳腫瘍では、成熟した樹状細胞が少なく、M2様マクロファージが過剰に存在していることが確認されました。これらの“平和維持者”マクロファージはT細胞の浸潤低下や最終成績不良と関連しており、もし研究者がこれらの細胞を戦う側へ書き換えられれば、より強力で持続的な抗腫瘍免疫を引き出せる可能性を示唆しています。
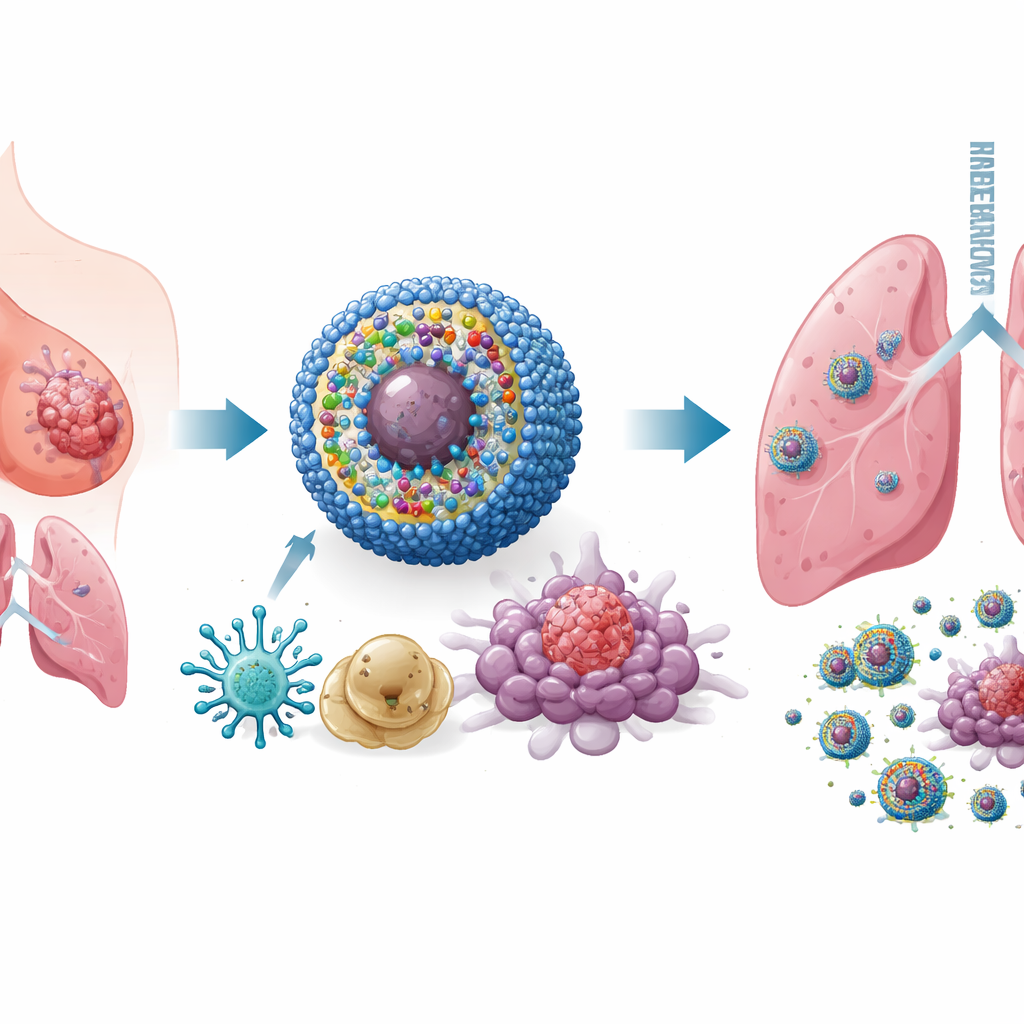
スマートな多機能ナノ医薬の設計
この問題に取り組むために、研究者らはIPANPと呼ぶナノスケールの送達システムを構築しました――血流中を循環し腫瘍に集積する小さな球状ミセルです。各ナノミセルは三つの成分を運びます。第一に、近赤外光で励起すると反応性分子を生成し、腫瘍細胞を免疫系に見えやすい形でストレス・死に至らしめる光活性化色素(IR825)。第二に、腫瘍がT細胞をオフにするために使う分子的ブレーキを取り除くPD‑L1に対する抗体。第三に、腫瘍促進性マクロファージで高発現するマイクロRNA miR‑182を阻害する短い遺伝子断片(antagomiR‑182)。キャリアは腫瘍内部の化学的に反応的な環境に感受性があり、主に必要な場所での薬物放出を行うため、健常組織への曝露を制限します。
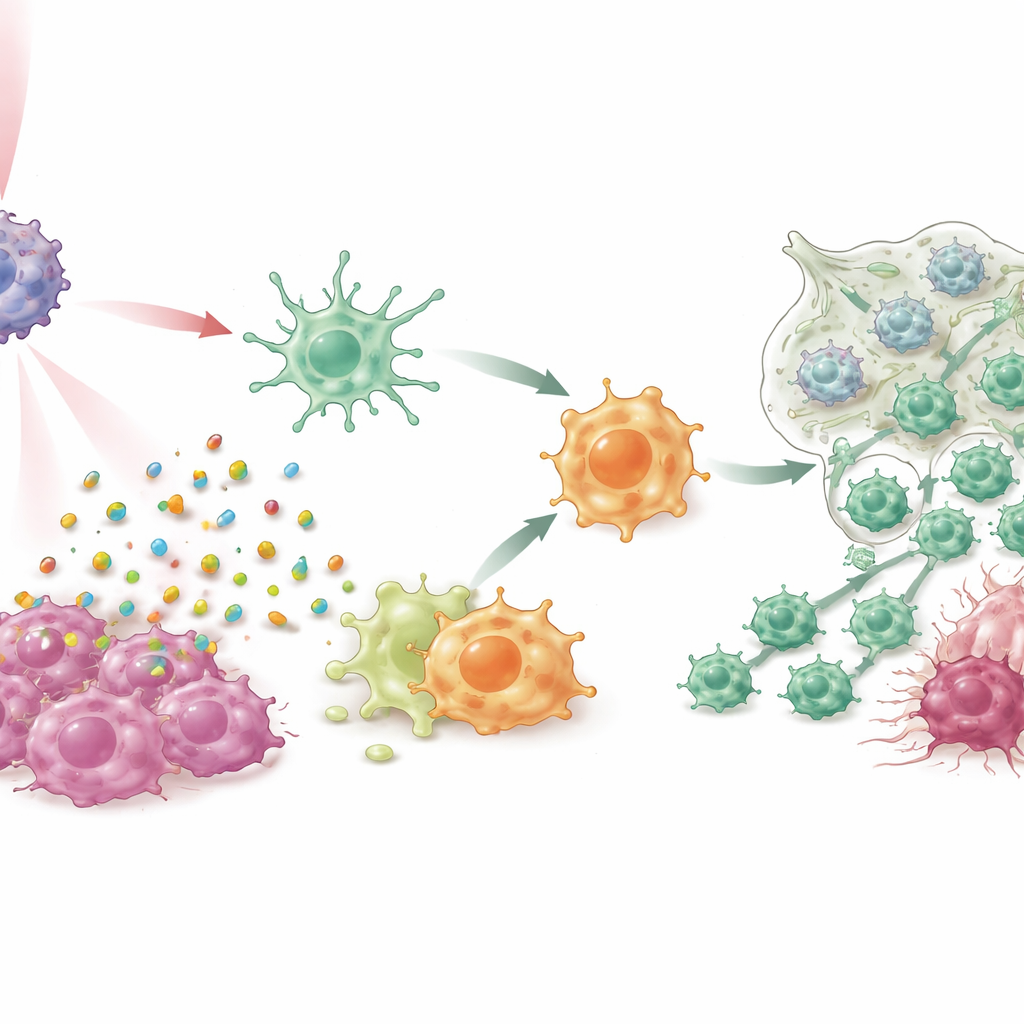
抑制細胞を攻撃者へ変える
培養細胞や複数の乳がんマウスモデル(治療困難なトリプルネガティブや自発腫瘍モデルを含む)において、IPANPと低強度の近赤外光の併用は単に腫瘍を縮小する以上の効果を示しました。光活性化色素はがん細胞を「免疫原性」に死滅させ、危険シグナルを放出して樹状細胞を成熟させ、腫瘍断片をT細胞により効率的に提示させました。同時に、マクロファージ内のmiR‑182をブロックすることで主要なセンシング経路(TLR4/MYD88/NF‑κB)にかかっていたブレーキが解除され、マクロファージはM2様の腫瘍支持状態からM1様の炎症促進状態へと移行しました。これら二つの骨髄系細胞の役割が変わるにつれ、より多くのキラーT細胞が腫瘍に流入して活性化され、疲弊による機能喪失を起こしにくくなりました。その結果、原発腫瘍の強力な制御、肺転移の大幅な減少、治療動物の生存延長が得られました。
持続する防御と実用性を示す兆し
注目すべきことに、IPANPと光で腫瘍が消失したマウスは、数か月後に研究者が新たに腫瘍を移植しても防御されており、ワクチンが作るような免疫記憶の形成を示しました。研究チームはまた、患者から切除したばかりの乳がん試料を小片として生体外で維持する系やヒト化マウスの患者由来腫瘍移植モデルでもこのアプローチを検証しました。これらの条件下でも治療は樹状細胞とマクロファージをより活性化された抗腫瘍状態へと押し、増殖促進シグナルを低下させ、有益な炎症性分子を増やし、キラーT細胞の存在を高め、腫瘍細胞死を引き起こしました――しかも長期の動物試験で良好な安全性が示されました。
将来のがん治療にとって意味するところ
この研究は、攻撃的な乳がんを単に腫瘍細胞を直接攻撃するだけでなく、それらを取り巻く免疫細胞を再教育することで治療できる可能性を示しています。光活性化療法、チェックポイント阻害、および遺伝子による再プログラミングを一つのスマートなナノミセルに詰めることで、研究者らは抑制的な腫瘍近傍を持続的な免疫防御を支える環境へと変える協調的な働きかけを作り出しました。臨床応用に到るにはさらに多くの検証が必要ですが、この戦略は原発腫瘍と転移腫瘍の両方を長期にわたり抑えるために免疫環境を再構築する将来の治療法の青写真を提供します。
引用: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
キーワード: 乳がん免疫療法, ナノ医療, 腫瘍微小環境, マクロファージの再プログラム, 樹状細胞の活性化