Clear Sky Science · de
Programmierbare Nanomicelle schalten myeloide Immunität um für dauerhafte Kontrolle von primärem und metastasiertem Brustkrebs
Ein neuer Weg, das Immunsystem im Kampf gegen Brustkrebs zu unterstützen
Die meisten Krebsbehandlungen zielen darauf ab, Tumorzellen direkt zu zerstören. Viele Tumoren überleben jedoch, indem sie die körpereigenen Immunzellen stillumdrehen und zu Verbündeten machen. Diese Studie beschreibt ein winziges, programmierbares Arzneimittel, das darauf abzielt, diese Zellen wieder in Krebsbekämpfer zurückzuverwandeln und so eine langanhaltende Kontrolle aggressiver Brustkrebserkrankungen zu ermöglichen, die sich in andere Organe ausgebreitet haben.
Warum Brustkrebs so schwer zu heilen sein kann
Brustkrebs ist die bei Frauen am häufigsten diagnostizierte Krebserkrankung; seine tödlichste Eigenschaft ist die Neigung zur Ausbreitung, besonders in die Lunge. Eine Subgruppe, der triple-negative Brustkrebs, ist besonders schwer zu behandeln, weil ihr die gängigen Hormon- und Wachstumsfaktorziele fehlen. Selbst moderne Immuntherapien, die den PD-L1 „Schild“ der Tumorzellen blockieren, helfen nur einem Teil der Patientinnen und verlängern oft nicht das Überleben. Ein wesentlicher Grund ist die Mikroumgebung des Tumors — das unmittelbare Umfeld von Zellen und Molekülen um den Krebs herum — in dem viele Immunzellen so umprogrammiert sind, dass sie anti-tumorale Angriffe unterdrücken statt zu unterstützen.
Der verborgene Einfluss der Unterstützerzellen rund um Tumoren
Unter diesen umgebenden Zellen spielen zwei Typen myeloider Zellen eine überproportionale Rolle: dendritische Zellen und Makrophagen. Unter gesunden Bedingungen fungieren dendritische Zellen als Wachposten, nehmen verdächtige Moleküle auf und präsentieren sie T-Zellen, um eine gezielte Immunantwort auszulösen. Makrophagen können entweder Entzündungen fördern (M1-ähnlich) und dabei helfen, Bedrohungen zu beseitigen, oder beruhigend wirken und die Gewebereparatur unterstützen (M2-ähnlich). In Brusttumoren von Patientinnen und Mausmodellen fanden die Autorinnen und Autoren weniger reife dendritische Zellen und eine Fülle von M2-ähnlichen Makrophagen. Diese „Friedenswächter“-Makrophagen standen im Zusammenhang mit schlechterer T‑Zell‑Infiltration und ungünstigeren Verläufen, was nahelegt, dass eine Rückprogrammierung dieser Zellen zu Kämpfern stärkere und länger anhaltende anti-tumorale Immunantworten eröffnen könnte.
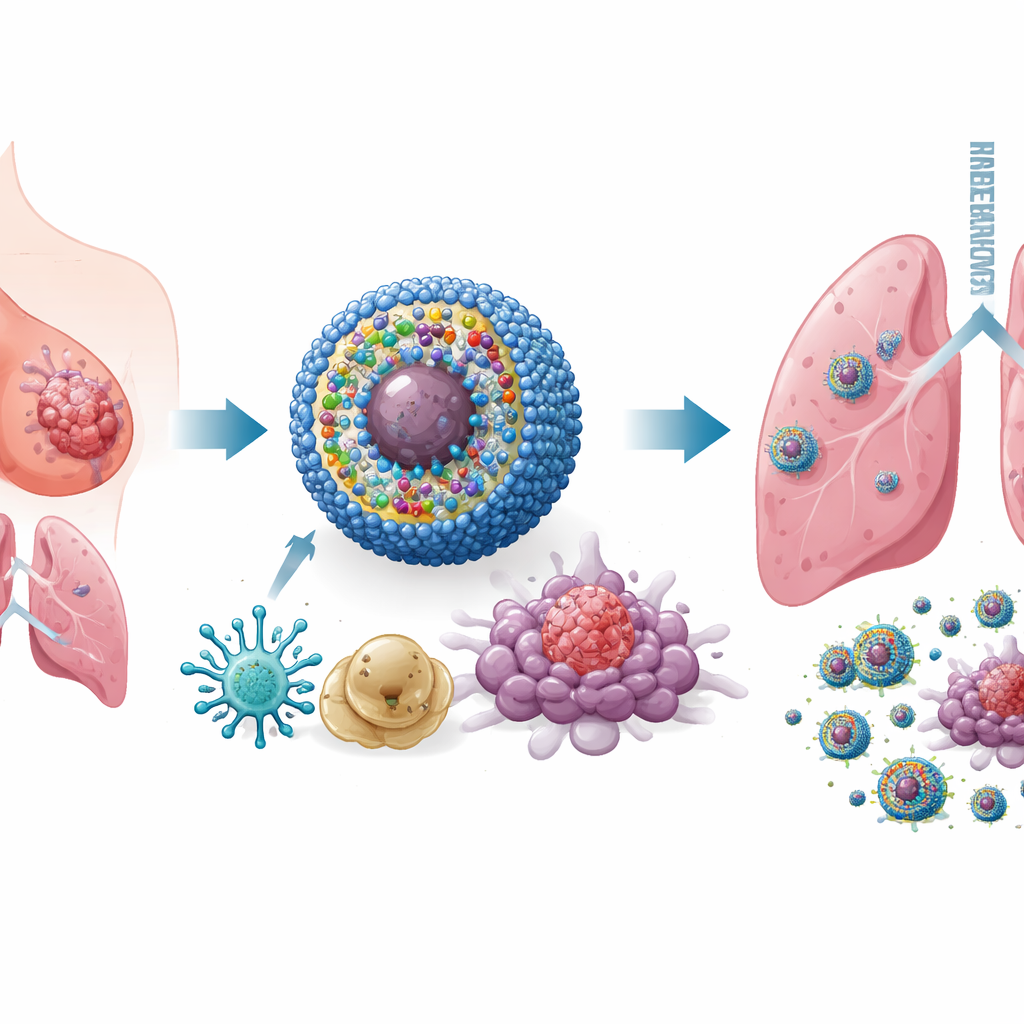
Entwurf einer intelligenten, multifunktionalen Nanomedizin
Um dieses Problem anzugehen, entwickelten die Forschenden ein nanoskaliges Transportsystem namens IPANP — winzige kugelförmige Micellen, die im Blutkreislauf zirkulieren und sich in Tumoren anreichern. Jede Nanomicelle trägt drei Komponenten: Erstens einen lichtaktivierbaren Farbstoff (IR825), der bei Beleuchtung mit nahinfrarotem Licht von außen reaktive Moleküle erzeugt, die Tumorzellen stressen und abtöten, sodass sie für das Immunsystem besonders sichtbar werden. Zweitens einen Antikörper gegen PD‑L1, der eine molekulare Bremse entfernt, mit der Tumoren T‑Zellen abschalten. Drittens ein kurzes genetisches Fragment (antagomiR‑182), das ein MicroRNA, miR‑182, blockiert, das in tumorfördernden Makrophagen hochreguliert ist. Der Träger reagiert auf die chemisch reaktive Umgebung im Tumor und setzt seine Fracht überwiegend dort frei, wo sie benötigt wird, wodurch die Belastung gesunden Gewebes begrenzt bleibt.
Unterdrückerzellen in Angreifer verwandeln
In Zellkulturen und mehreren Mausmodellen von Brustkrebs, einschließlich schwer zu behandelnder triple-negativer und spontaner Tumorsysteme, bewirkte IPANP in Kombination mit schonendem nahinfraroten Licht mehr als nur Tumorverkleinerung. Der lichtaktivierbare Farbstoff ließ Krebszellen auf eine immunogen wirkende Weise absterben und setzte Gefahrenalarmen frei, die dendritische Zellen zur Reifung anregten und ihnen ermöglichten, Tumorfragmente effizienter T‑Zellen zu präsentieren. Gleichzeitig hob die Blockade von miR‑182 in Makrophagen eine Hemmung eines wichtigen Erkennungswegs (TLR4/MYD88/NF‑κB) auf und bewegte sie vom M2‑ähnlichen, tumorfördernden Zustand hin zu einem M1‑ähnlichen, entzündungsfördernden Zustand. Als sich diese beiden myeloiden Zelltypen umstellten, strömten mehr Killer‑T‑Zellen in die Tumoren, wurden aktiver und zeigten weniger Erschöpfungszeichen. Das Ergebnis war eine starke Kontrolle der Primärtumoren, deutliche Verringerungen von Lungenmetastasen und verlängertes Überleben der behandelten Tiere.
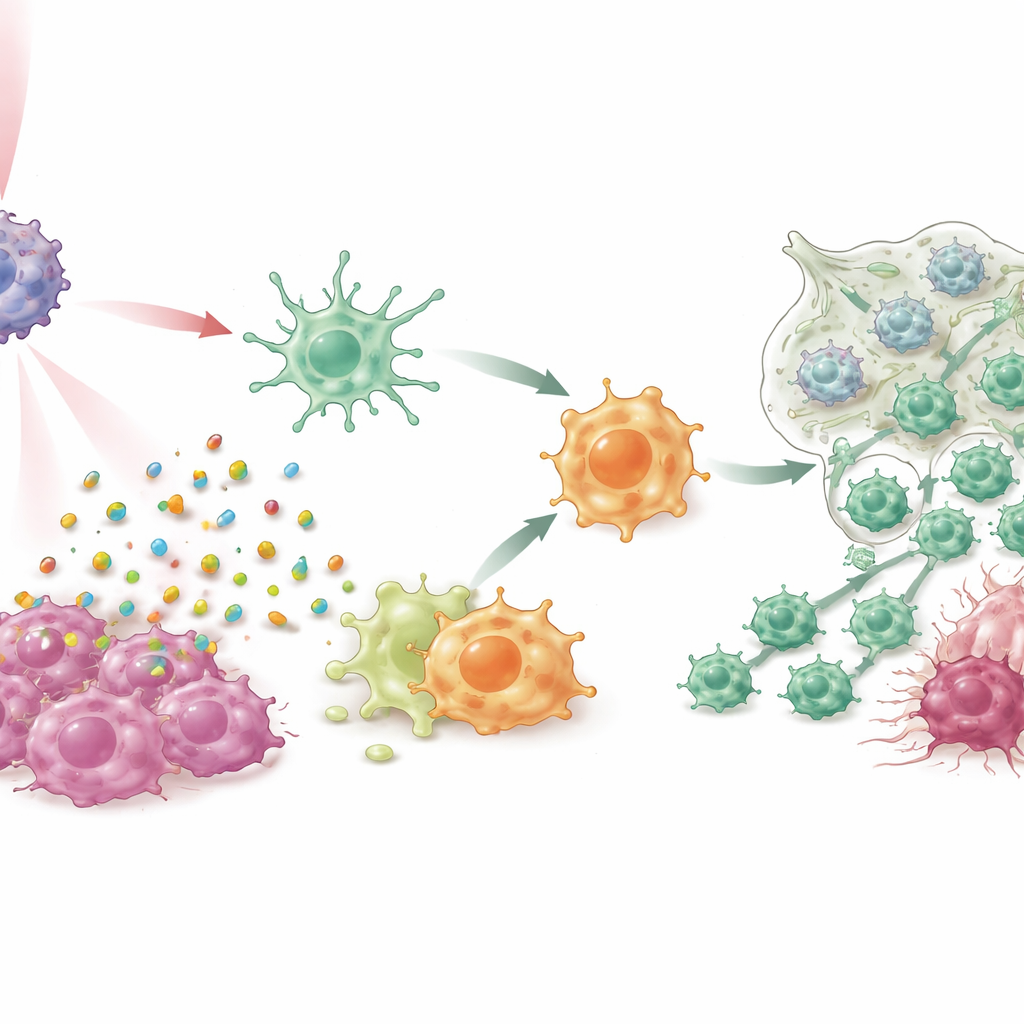
Dauerhafter Schutz und Anzeichen für echten Praxisnutzen
Bemerkenswerterweise waren Mäuse, deren Tumoren durch IPANP und Licht beseitigt worden waren, geschützt, als die Forschenden Monate später versuchten, neue Tumoren zu transplantieren — ein Hinweis auf die Bildung immunologischen Gedächtnisses ähnlich dem einer Impfung. Das Team testete den Ansatz außerdem an frisch entfernten Brustkrebsproben von Patientinnen, die als kleine Gewebestücke lebensfähig gehalten wurden, und in patientenabgeleiteten Tumorimplantaten in humanisierten Mäusen. In diesen Modellen trieb die Behandlung erneut dendritische Zellen und Makrophagen in aktivere, anti-tumorale Zustände, reduzierte wachstumsfördernde Signale, steigerte nützliche entzündungsfördernde Moleküle, erhöhte die Präsenz von Killer‑T‑Zellen und verursachte Tumorzellsterben — und das bei guter Sicherheit in Langzeitstudien an Tieren.
Was dies für die künftige Krebsbehandlung bedeuten könnte
Diese Arbeit zeigt, dass es möglich sein könnte, aggressive Brustkrebserkrankungen nicht nur durch direkte Angriffe auf Tumorzellen zu behandeln, sondern auch durch die Umerziehung der sie umgebenden Immunzellen. Indem Licht‑aktivierte Therapie, Checkpoint‑Blockade und genetische Umprogrammierung in einer intelligenten Nanomicelle kombiniert wurden, erzeugten die Forschenden einen koordinierten Impuls, der eine unterdrückende Tumorumgebung in eine solche verwandelte, die dauerhafte Immunabwehr unterstützt. Obwohl vor einer klinischen Anwendung noch weitreichende Tests nötig sind, bietet der Ansatz ein Konzept für künftige Therapien, die das Immunumfeld umgestalten, um sowohl Primär‑ als auch metastatische Tumoren langfristig unter Kontrolle zu halten.
Zitation: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
Schlüsselwörter: Immuntherapie bei Brustkrebs, Nanomedizin, Tumormikroumgebung, Umpolung von Makrophagen, Aktivierung dendritischer Zellen