Clear Sky Science · es
Nanomicelas programables reconectan la inmunidad mieloide para el control duradero del cáncer de mama primario y metastásico
Una nueva forma de ayudar al sistema inmunitario a combatir el cáncer de mama
La mayoría de los tratamientos contra el cáncer se centran en matar directamente las células tumorales, pero muchos tumores sobreviven al transformar discretamente las propias células inmunitarias del cuerpo en aliadas. Este estudio describe una medicina diminuta y programable que pretende volver a convertir esas células en luchadoras contra el cáncer, ofreciendo un control duradero de los cánceres de mama agresivos que se han diseminado a otros órganos.
Por qué el cáncer de mama puede ser tan difícil de curar
El cáncer de mama es el cáncer más diagnosticado en mujeres, y su rasgo más letal es su tendencia a metastatizar, especialmente a los pulmones. Un subtipo, el cáncer de mama triple negativo, es especialmente difícil de tratar porque carece de los objetivos hormonales y de factores de crecimiento comunes. Incluso las inmunoterapias modernas que bloquean el “escudo” PD-L1 en las células tumorales solo benefician a una fracción de pacientes y a menudo no prolongan la supervivencia. Una razón principal es el microambiente del tumor—el vecindario inmediato de células y moléculas alrededor del cáncer—que está repleto de células inmunitarias que han sido reprogramadas para suprimir, en lugar de apoyar, los ataques antitumorales.
La influencia oculta de las células de apoyo alrededor de los tumores
Entre estas células circundantes, dos tipos de células mieloides juegan un papel desproporcionado: las células dendríticas y los macrófagos. En condiciones sanas, las dendríticas actúan como centinelas, captando moléculas sospechosas y presentándolas a los linfocitos T para desencadenar un ataque inmunitario dirigido. Los macrófagos pueden apoyar la inflamación (tipo M1) y ayudar a eliminar amenazas, o bien calmar la respuesta y promover la reparación tisular (tipo M2). En tumores de mama de pacientes y modelos murinos, los autores encontraron menos células dendríticas maduras y una abundancia de macrófagos de tipo M2. Estos macrófagos “pacificadores” se asociaron con menor infiltración de linfocitos T y peores resultados, lo que sugiere que si los científicos pudieran reconvertir estas células en combatientes, podrían desbloquear respuestas inmunitarias más potentes y duraderas contra el cáncer.
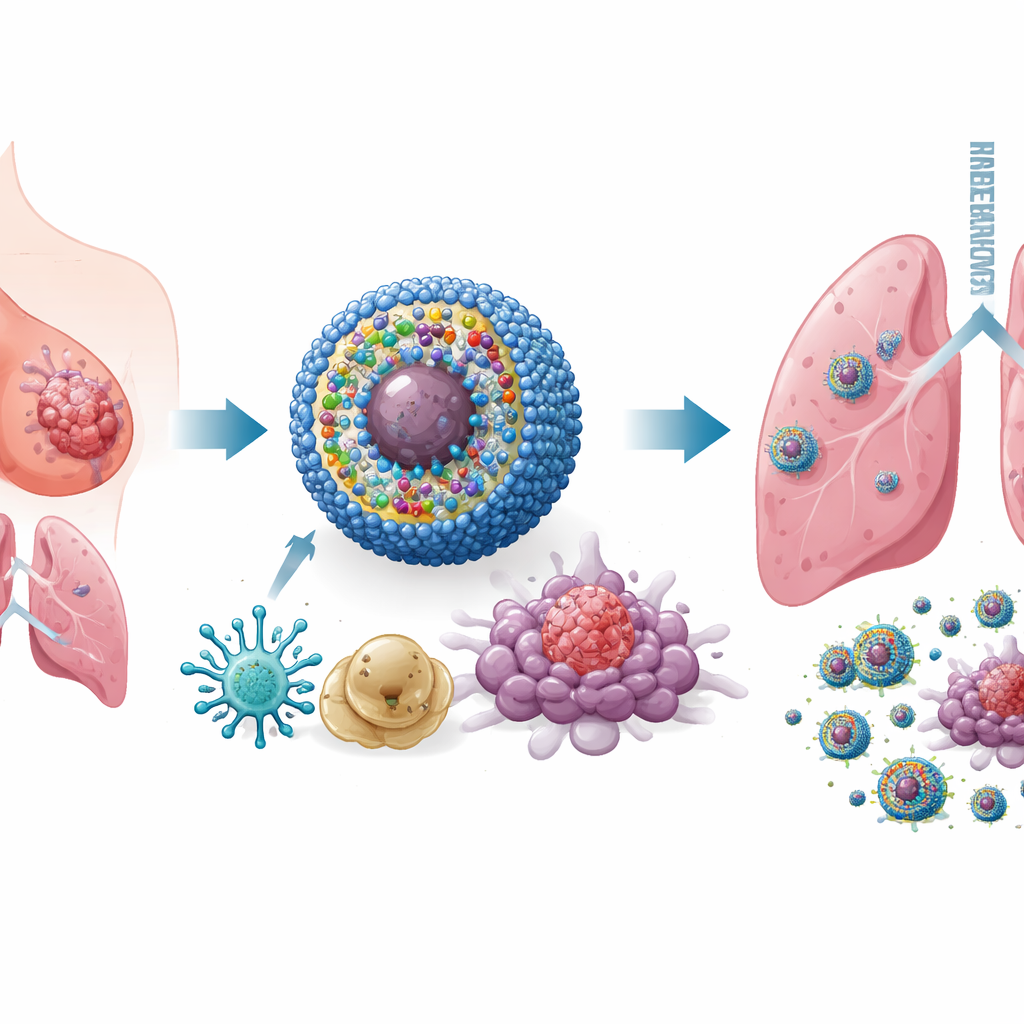
Diseñando una nanomedicina inteligente y multifunción
Para abordar este problema, los investigadores construyeron un sistema de entrega a nanoescala que denominan IPANP—pequeñas micelas esféricas que circulan por el torrente sanguíneo y se acumulan en los tumores. Cada nanomicela lleva tres componentes. Primero, un tinte activado por luz (IR825) que, al iluminarse con luz infrarroja cercana desde fuera del cuerpo, genera moléculas reactivas que estresan y matan las células tumorales de un modo que las hace altamente visibles para el sistema inmunitario. Segundo, un anticuerpo contra PD-L1, que ayuda a quitar un freno molecular que los tumores usan para apagar a los linfocitos T. Tercero, un fragmento corto de material genético (antagomiR-182) que bloquea un microARN, miR-182, presente en niveles altos en macrófagos promotores del tumor. El transportador es sensible al entorno químicamente reactivo dentro de los tumores, por lo que libera su carga principalmente donde se necesita, limitando la exposición a tejidos sanos.
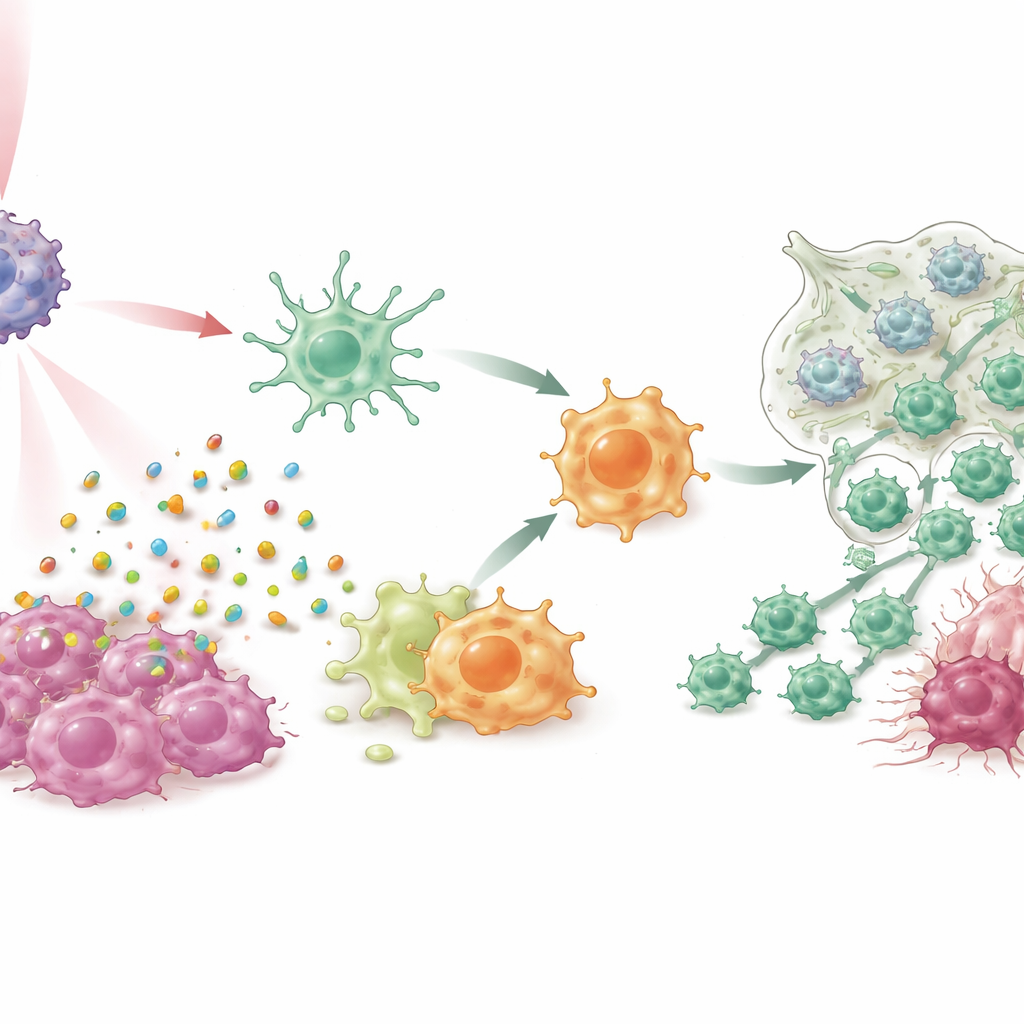
Convertir células supresoras en atacantes
En cultivos celulares y en múltiples modelos murinos de cáncer de mama, incluidos los difíciles triple negativos y sistemas de tumores espontáneos, IPANP combinado con luz suave en el infrarrojo cercano hizo más que reducir tumores. El tinte activado por luz provocó que las células cancerosas murieran de forma “inmunogénica”, liberando señales de peligro que impulsaron la maduración de las células dendríticas y la presentación más eficiente de fragmentos tumorales a los linfocitos T. Al mismo tiempo, bloquear el miR-182 en los macrófagos levantó un freno sobre una vía sensora clave (TLR4/MYD88/NF-κB), empujándolos desde el estado tipo M2, que apoya al tumor, hacia un estado tipo M1, inflamatorio. A medida que estos dos tipos de células mieloides cambiaron de función, más linfocitos T citotóxicos inundaron los tumores, se volvieron más activos y fueron menos propensos a apagarse por agotamiento. El resultado fue un control sólido de los tumores primarios, reducciones marcadas de las metástasis pulmonares y una supervivencia prolongada en los animales tratados.
Protección duradera y señales de promesa real
De forma llamativa, los ratones cuyos tumores fueron eliminados por IPANP y luz estuvieron protegidos cuando los investigadores intentaron reimplantar nuevos tumores meses después, lo que indica la formación de memoria inmunitaria similar a la creada por una vacuna. El equipo también probó el enfoque en muestras frescas de cáncer de mama extraídas de pacientes, mantenidas vivas como pequeños fragmentos de tejido, y en injertos tumorales derivados de pacientes en ratones humanizados. En estos contextos, el tratamiento volvió a empujar a las células dendríticas y a los macrófagos hacia estados más activos y antitumorales, redujo señales que promueven el crecimiento, aumentó las moléculas inflamatorias beneficiosas, incrementó la presencia de linfocitos T citotóxicos y provocó la muerte de células tumorales—todo ello mostrando además buena seguridad en estudios animales a largo plazo.
Lo que esto podría significar para el futuro del tratamiento del cáncer
Este trabajo muestra que puede ser posible tratar cánceres de mama agresivos no solo atacando las células tumorales directamente, sino reeducando las células inmunitarias que las rodean. Al combinar terapia activada por luz, bloqueo de puntos de control y reprogramación genética en una sola nanomicela inteligente, los investigadores crearon un impulso coordinado que convirtió un vecindario tumoral supresor en uno que favorece una defensa inmunitaria duradera. Aunque se necesita mucha más investigación antes de que esta estrategia pueda llegar a los pacientes, ofrece un modelo para futuros tratamientos que remodelen el entorno inmunitario para mantener bajo control a largo plazo tanto los tumores primarios como las metástasis.
Cita: Yang, J., Chang, D., Li, Y. et al. Programmable nanomicelles rewire myeloid immunity for durable control of primary and metastatic breast cancer. Nat Commun 17, 4082 (2026). https://doi.org/10.1038/s41467-026-70859-5
Palabras clave: inmunoterapia del cáncer de mama, nanomedicina, microambiente tumoral, reprogramación de macrófagos, activación de células dendríticas