Clear Sky Science · zh
通过药物门控的光激活工程可编程CAR与抗原配对
教免疫细胞更聪明地猎杀
许多人听说过CAR T细胞——一种将患者自身免疫细胞重编程以攻击肿瘤的个体化癌症治疗方法。这类疗法在某些血液癌症中效果显著,但对实体肿瘤(如乳腺、前列腺或肺部)一直面临挑战。本研究描述了一种既能增强又能约束CAR T细胞的新方法,使其更好地识别多样的肿瘤细胞,同时尽量保护健康组织。
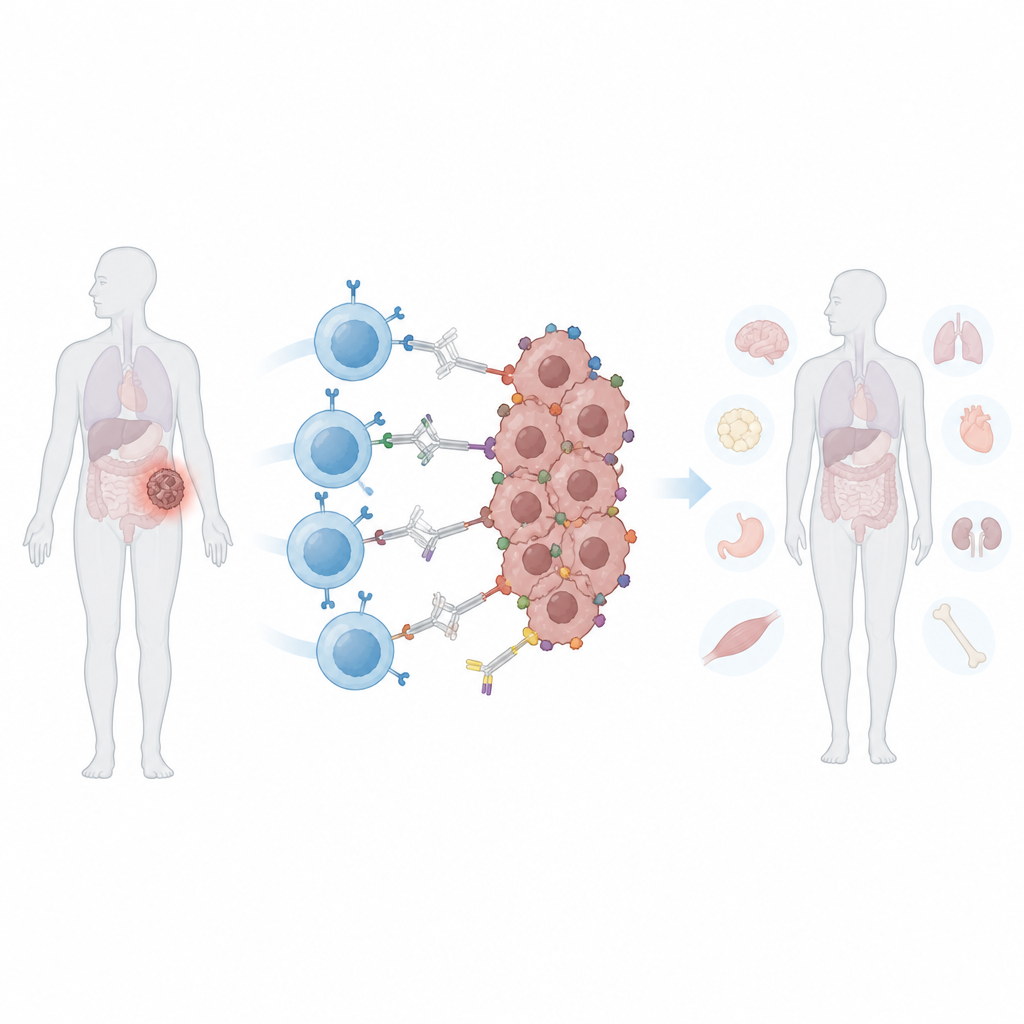
不断变形的肿瘤带来的挑战
传统的CAR T细胞被设计为识别癌细胞表面的特定分子“标志”。实体肿瘤常通过两种方式躲避这种攻击。首先,它们可以丢失或降低该标志——称为抗原逃逸——使部分细胞存活并使肿瘤复发。其次,同一肿瘤内的不同细胞可能展示不同的标志,这就是异质性问题。扩展CAR T识别更多标志可以有所帮助,但也增加了它们攻击共享这些标记的正常组织的风险。一旦常规CAR T细胞输注进入体内,它们就处于持续激活状态,当出现副作用时,医生难以随时调低或关闭其活性。
可用于多种肿瘤的通用插头
研究人员构建了一种“不直接结合肿瘤细胞”的“可编程”CAR。它识别一种安全且颜色鲜艳的蛋白——藻红蛋白(phycoerythrin,PE),这类蛋白常用于食品和实验检测。他们将源自人体的小型结合域(称为PEbody)工程化地连接到CAR上,使其能够附着到携带该蛋白标签的任何抗体上。通过选择注入哪种带PE标签的抗体,医生原则上可以将同一批CAR T细胞定向到不同的癌症标志,依次或同时针对多个标志。在体外试验中,这些携带PEbody的CAR T细胞在提供相应带标抗体时能有效杀死白血病和多种实体肿瘤细胞系,并且在第一个标志丧失后可重新定向到新的标志。
药物与光的安全开关
为提高安全性,团队增加了分层控制系统,使他们仅在需要的时间和位置打开CAR表达。他们使用了一个两部分的遗传开关,首先对常用药物他莫昔芬(tamoxifen)响应,然后对蓝光响应。只有同时接收到两种信号的T细胞会激活重组酶,从而永久翻转并开启CAR基因。这种“药物门控的光激活”将强效的CAR活性限制在被照亮的肿瘤区域。在细胞培养中,只有同时接受他莫昔芬和光照的T细胞其CAR水平和肿瘤杀伤显著上升,而处于黑暗或未给药的细胞则保持静默。在小鼠体内,同一系统仅在接受光照的一侧肿瘤中驱动了强烈的基因激活,未受光照的一侧活动几乎可以忽略。
肿瘤内的训练中心
更进一步,研究人员将肿瘤感知与肿瘤杀伤分离开来。他们使用了第二种工程化受体,称为synNotch,使PEbody CAR仅在T细胞遇到一种特殊标志——在肿瘤细胞上放置的截短版CD19——时被开启。该标志并非自然存在,而是通过同一药物与光系统在局部诱导产生。只有接受光信号的肿瘤细胞开始展示这一训练标志。当synNotch T细胞到达时,这些被标记的细胞就充当“训练中心”,激活大量T细胞并使其获得PEbody CAR。一旦被训练,这些T细胞便能利用针对常见肿瘤标志(如PD-L1或PSMA)的PE标记抗体攻击更广泛的肿瘤群体,即便这些被攻击的细胞从未表达过训练标志。
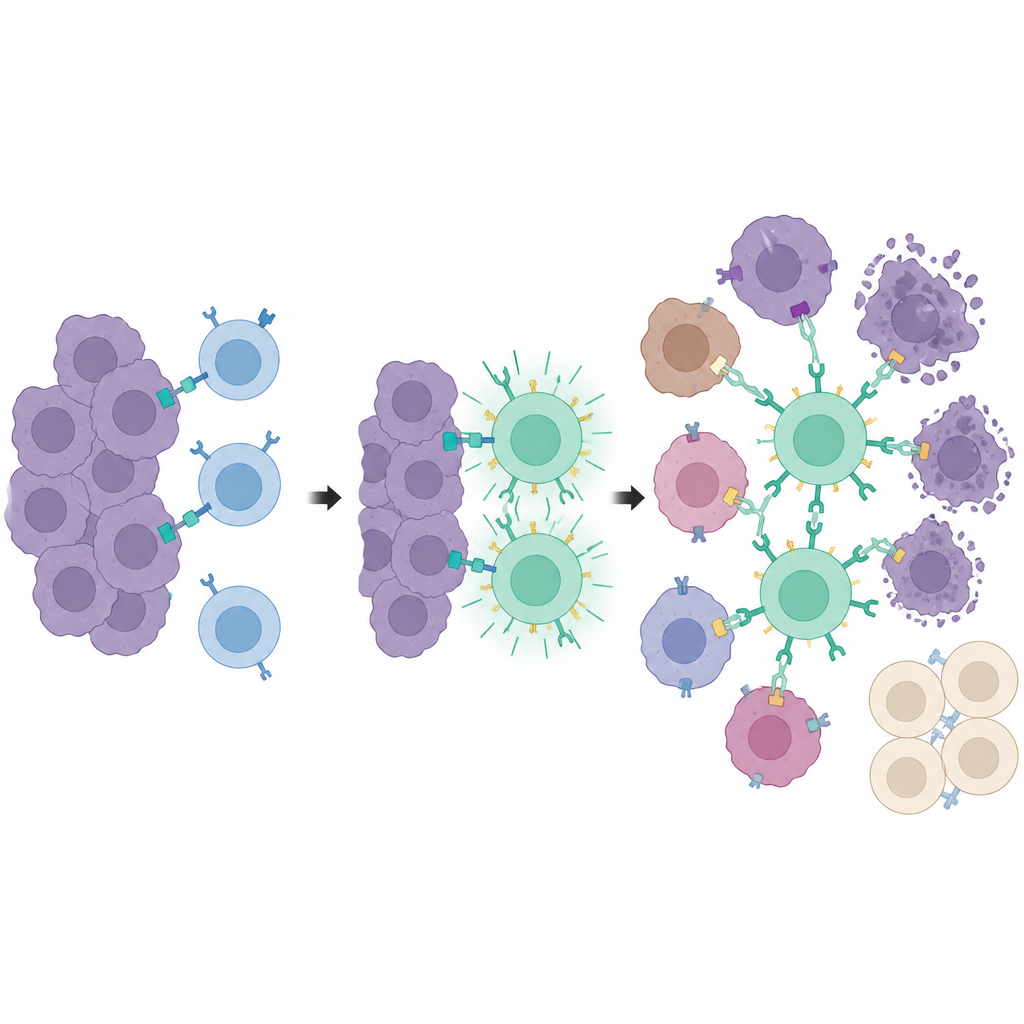
局部攻击并保护远端组织
在几种乳腺癌和前列腺癌的小鼠模型中,药物、光与synNotch相结合的系统在被照亮的部位产生了强烈的肿瘤控制效果。接受他莫昔芬和光照处理、随后给予可编程T细胞和PE标记抗体的肿瘤,比同一动物中未照光的肿瘤明显缩小或生长更慢。重要的是,T细胞在体内循环但只有在被光激活的肿瘤内才完全激活,从而限制了对携带相同表面标记的其他器官的损害。与针对PSMA标记的常规CAR T治疗相比,该新策略在实现相似肿瘤控制的同时伴随较少的体重下降、更低的炎症信号和减轻的肝损伤迹象。
这对未来癌症治疗意味着什么
对普通读者来说,关键思想是:研究人员构建了一种通用且可重写的CAR T系统,内置局部安全锁。带标抗体的选择决定了要靶向的肿瘤特征,因此医生可能在癌症演化时调整治疗,而无需重新构建T细胞。与此同时,药物与光以及训练中心的设计有助于确保全部T细胞的攻击力只在肿瘤内部释放,而不会在共享这些标记的健康组织中被触发。尽管在将该方法用于患者之前仍需大量工作,这项研究为针对复杂实体肿瘤的更安全、更灵活的细胞疗法勾勒出了一种可行蓝图。
引用: Huang, Z., Limsakul, P., Wu, Y. et al. Engineering programmable CAR and antigen pairing via drug-gated light activation. Nat Commun 17, 4252 (2026). https://doi.org/10.1038/s41467-026-70855-9
关键词: CAR T细胞, 实体肿瘤, 光遗传学, 抗原逃逸, 合成免疫疗法